预约演示
更新于:2026-06-08
Lutetium (177 Lu) Vipivotide Tetraxetan
镥[177Lu] 特昔维匹肽
更新于:2026-06-08
概要
基本信息
原研机构 |
非在研机构- |
权益机构 |
最高研发阶段批准上市 |
首次获批日期 美国 (2022-03-23), |
最高研发阶段(中国)批准上市 |
特殊审评突破性疗法 (美国)、优先审评 (中国)、孤儿药 (韩国) |
登录后查看时间轴
结构/序列
分子式C49H68LuN9O16 |
InChIKeyRSTDSVVLNYFDHY-NLQOEHMXSA-K |
CAS号1703749-62-5 |
使用我们的ADC技术数据为新药研发加速。
登录
或

关联
91
项与 镥[177Lu] 特昔维匹肽 相关的临床试验NCT06852820
A Pilot Study of 68Ga-PSMA-11 PET-directed Radioligand Therapy in Patients With Metastatic Hepatocellular Carcinoma (HCC)
The purpose of this study is to look at the effects (good and bad) of a drug called 177Lu-PSMA-617 (also known as the study drug) when given to participants who have prostate specific membrane antigen (PSMA) positive liver cancer.
开始日期2026-06-01 |
申办/合作机构 |
NCT06959433
Safety and Efficacy of Lu-177 PSMA Treatment in Metastatic Clear Cell Renal Carcinoma
Summary Renal Cell Carcinoma (RCC) consists of 2% of all malignencies. RCCs are generally divided to histopathological subtypes as clear cell and non-clear cell variants. Clear cell variant responsible for the 75-80% of all RCCs. It is reported that 20-30% of RCCs are metastatic at the diagnosis and 5 years survival is approximately is 10-20% in this group of patients. Moreover, 60% of patients who are not metastatic at the diagnosis, develop metastates within 2-3 years. 2nd and 3th line effective treatment option in metastatic RCCs patients has been a subject of interest.
PSMA (protatate specific membrane antigen) with the other name glutamate carboxypeptidase, is a transmembrane protein and overexpresses in prostate adenocarcinomas and neoangiogenesis spots of endothelium of other several tumor types. It infronts as a target for theranostic consept for mainly prostate cancer in nuclear medicine. As a radionuclide treatment option, Lu-177 PSMA treatment is proved as safe and effective treatment option in castration resistant prostata cancer patients. After its widely use in prostate cancer, it is reported that PSMA molecule can be used for imaging of RCC patients and PSMA uptake is higher than 18F-FDG. For this reason, Lu-177 PSMA treatment can be a systemic treatment option in RCC patients who have progress afer 1st cycle treatment. In this study we aimed to safety and efficacy of Lu-177 PSMA treatment in metastatic RCC patients as systemic radionuclide treatment option.
PSMA (protatate specific membrane antigen) with the other name glutamate carboxypeptidase, is a transmembrane protein and overexpresses in prostate adenocarcinomas and neoangiogenesis spots of endothelium of other several tumor types. It infronts as a target for theranostic consept for mainly prostate cancer in nuclear medicine. As a radionuclide treatment option, Lu-177 PSMA treatment is proved as safe and effective treatment option in castration resistant prostata cancer patients. After its widely use in prostate cancer, it is reported that PSMA molecule can be used for imaging of RCC patients and PSMA uptake is higher than 18F-FDG. For this reason, Lu-177 PSMA treatment can be a systemic treatment option in RCC patients who have progress afer 1st cycle treatment. In this study we aimed to safety and efficacy of Lu-177 PSMA treatment in metastatic RCC patients as systemic radionuclide treatment option.
开始日期2026-05-01 |
申办/合作机构 |
NCT06783348
Phase II Trial Evaluating the Efficacy of 177Lutetium-PSMA-617 Treatment in Patients With Metastatic Clear Cell Renal Carcinoma Cell With Progressive Disease on First-line or Second-line Systemic Treatment
Background This study is for adults with advanced kidney cancer that has spread to other parts of the body and has continued to progress despite treatment with immunotherapy and targeted therapy. Unfortunately, treatment options at this stage of the disease are limited. The existing treatments' ability to work against cancer has not been fully looked into.
Rationale The goal of this study is to examine if a new drug treatment called 177Lutetium-PSMA-617, hereafter referred as 177Lu-PSMA-617, which holds the active ingredient 177Lutetium-PSMA and has been used as a standard treatment for advanced prostate cancer since December 2022, can also help treat advanced kidney cancer.
The drug 177Lu-PSMA-617 is being tested as an experimental treatment that targets a specific protein on cancer cells. This protein, known as prostate-specific membrane antigen (PSMA), is present on the surface of kidney cancer cells. Therefore, before the treatment begins, participants will undergo a PET (positron-emission tomography) scan to check if their kidney cancer cells express high levels of PSMA. This scan uses a small amount of radioactive material (in the form of 177Lutetium) to visualize the presence of PSMA on the cancer cells. Only participants who test positive for PSMA can take part in the study. In this approach, PSMA serves two purposes. First, it helps assess whether the cancer expresses this protein and allows 177Lu-PSMA-617 to specifically target and attach to the cancer cells. Second, 177Lu-PSMA-617 delivers a small amount of radiation directly to the tumour, which helps kill cancer cells while minimizing damage to normal cells. This type of treatment is known as a radiopharmaceutical.
Objective The primary aims are to find out if 177Lu-PSMA-617 is useful against kidney cancer and to assess its safety. Throughout the study, participants will undergo several imaging assessments to check their disease and response to treatment.
The study also includes the collection of tissue samples. Together with the information collected from the imaging assessments, this will allow further research into markers that may lead to earlier detection of tumour spread or help identify individuals who may benefit more from treatment with 177Lu-PSMA-617.
Treatment All participants will receive 177Lu-PSMA-617 through an intravenous injection at a standard dose of 7,400 MBq (megabecquerel: a measure of radioactivity). Treatments will be administered approximately every six weeks, for a maximum of six times.
Blood tests are done before and during treatment to check the participant's health and to detect any early side effects from the treatment. Different types of scans are performed before, during, and after 177Lu-PSMA-617 administration to check how well the treatment is working. After treatment ends, follow-up visits will be scheduled every six weeks during the first year. In the second year, your doctor will decide how often you need to come in for visits. These appointments are important for monitoring how the body continues to respond to the treatment. The entire study period will last approximately two years from the time of study entry.
Participants
The study will include approximately 56 participants who will be tested for PSMA expression, to obtain a minimum of 48 participants expressing PSMA entering the study. To qualify, participants must:
* Be diagnosed with advanced kidney cancer previously treated with immunotherapy and targeted therapy.
* Test positive for PSMA on a PET scan.
* Be generally healthy and able to perform daily activities.
* Be at least 18 years of age.
Benefit-risk analysis The drug 177Lu-PSMA-617 has proven to work well in treating advanced prostate cancer and could be a promising new treatment possibility for kidney cancer, although this has not yet been shown. By joining this study, participants will contribute to valuable research to better understand kidney cancer and improve treatment options for future patients. Participating in this study offers a chance to try a new treatment, which might help people with advanced kidney cancer live longer and prevent the disease from getting worse, especially for those who have limited treatment options left after immunotherapy and targeted therapy.
With all new treatments, there are possible risks and side effects associated with them. Side effects of the drug 177Lu-PSMA-617 may include feeling tired, nausea, dry mouth, loss of appetite, and changes in blood cells. While not all side effects are known yet, the study team will carefully follow participants for any side effects during and after treatment. It is important to understand that while the study is being done to provide new information, there are still some questions on the treatment's safety and how well it will work.
Rationale The goal of this study is to examine if a new drug treatment called 177Lutetium-PSMA-617, hereafter referred as 177Lu-PSMA-617, which holds the active ingredient 177Lutetium-PSMA and has been used as a standard treatment for advanced prostate cancer since December 2022, can also help treat advanced kidney cancer.
The drug 177Lu-PSMA-617 is being tested as an experimental treatment that targets a specific protein on cancer cells. This protein, known as prostate-specific membrane antigen (PSMA), is present on the surface of kidney cancer cells. Therefore, before the treatment begins, participants will undergo a PET (positron-emission tomography) scan to check if their kidney cancer cells express high levels of PSMA. This scan uses a small amount of radioactive material (in the form of 177Lutetium) to visualize the presence of PSMA on the cancer cells. Only participants who test positive for PSMA can take part in the study. In this approach, PSMA serves two purposes. First, it helps assess whether the cancer expresses this protein and allows 177Lu-PSMA-617 to specifically target and attach to the cancer cells. Second, 177Lu-PSMA-617 delivers a small amount of radiation directly to the tumour, which helps kill cancer cells while minimizing damage to normal cells. This type of treatment is known as a radiopharmaceutical.
Objective The primary aims are to find out if 177Lu-PSMA-617 is useful against kidney cancer and to assess its safety. Throughout the study, participants will undergo several imaging assessments to check their disease and response to treatment.
The study also includes the collection of tissue samples. Together with the information collected from the imaging assessments, this will allow further research into markers that may lead to earlier detection of tumour spread or help identify individuals who may benefit more from treatment with 177Lu-PSMA-617.
Treatment All participants will receive 177Lu-PSMA-617 through an intravenous injection at a standard dose of 7,400 MBq (megabecquerel: a measure of radioactivity). Treatments will be administered approximately every six weeks, for a maximum of six times.
Blood tests are done before and during treatment to check the participant's health and to detect any early side effects from the treatment. Different types of scans are performed before, during, and after 177Lu-PSMA-617 administration to check how well the treatment is working. After treatment ends, follow-up visits will be scheduled every six weeks during the first year. In the second year, your doctor will decide how often you need to come in for visits. These appointments are important for monitoring how the body continues to respond to the treatment. The entire study period will last approximately two years from the time of study entry.
Participants
The study will include approximately 56 participants who will be tested for PSMA expression, to obtain a minimum of 48 participants expressing PSMA entering the study. To qualify, participants must:
* Be diagnosed with advanced kidney cancer previously treated with immunotherapy and targeted therapy.
* Test positive for PSMA on a PET scan.
* Be generally healthy and able to perform daily activities.
* Be at least 18 years of age.
Benefit-risk analysis The drug 177Lu-PSMA-617 has proven to work well in treating advanced prostate cancer and could be a promising new treatment possibility for kidney cancer, although this has not yet been shown. By joining this study, participants will contribute to valuable research to better understand kidney cancer and improve treatment options for future patients. Participating in this study offers a chance to try a new treatment, which might help people with advanced kidney cancer live longer and prevent the disease from getting worse, especially for those who have limited treatment options left after immunotherapy and targeted therapy.
With all new treatments, there are possible risks and side effects associated with them. Side effects of the drug 177Lu-PSMA-617 may include feeling tired, nausea, dry mouth, loss of appetite, and changes in blood cells. While not all side effects are known yet, the study team will carefully follow participants for any side effects during and after treatment. It is important to understand that while the study is being done to provide new information, there are still some questions on the treatment's safety and how well it will work.
开始日期2026-04-07 |
100 项与 镥[177Lu] 特昔维匹肽 相关的临床结果
登录后查看更多信息
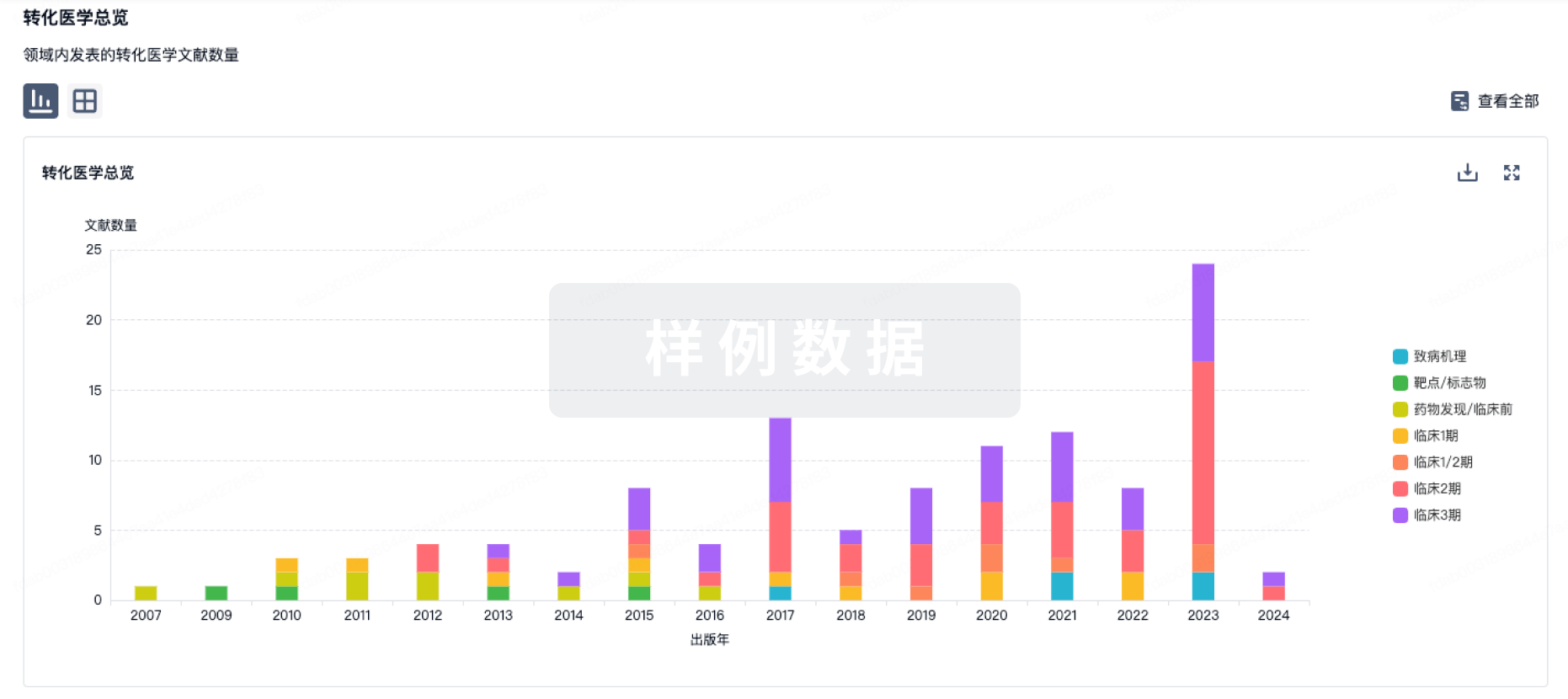
100 项与 镥[177Lu] 特昔维匹肽 相关的转化医学
登录后查看更多信息
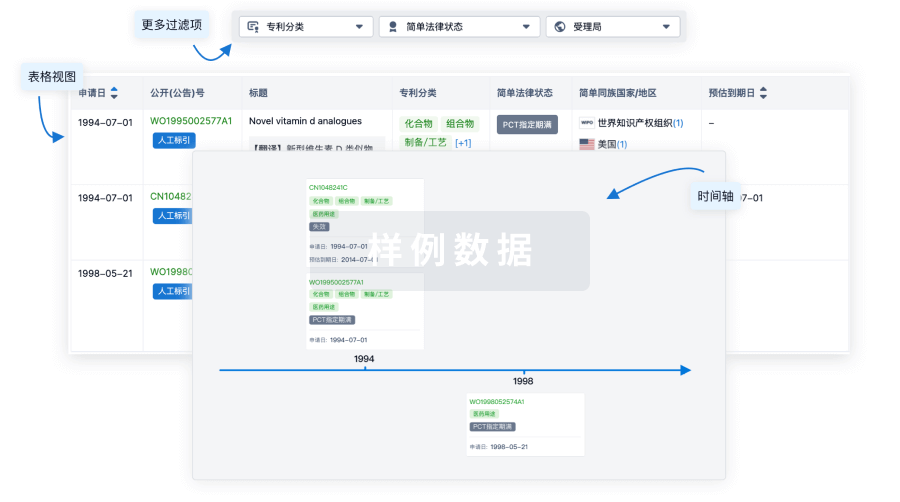
100 项与 镥[177Lu] 特昔维匹肽 相关的专利(医药)
登录后查看更多信息
715
项与 镥[177Lu] 特昔维匹肽 相关的文献(医药)2026-08-01·APPLIED RADIATION AND ISOTOPES
Preclinical assessment of 177Lu-DOTA-Pip-Nle-CycMSHhex: In vivo evaluation and human dosimetry estimation
Article
作者: Shirmardi, Seyed Pezhman ; Alirezapour, Behrouz ; Zolghadri, Samaneh ; Erfani, Mostafa ; Yousefnia, Hassan ; Karimian, Arezou
This study presents a preclinical assessment of 177Lu-DOTA-Pip-Nle-CycMSHhex (177Lu-CCZ01048), a previously reported radiolabeled α-MSH analogue targeting melanoma, with a focus on additional in vivo evaluation and human dosimetry extrapolation. 177Lu-CCZ01048 was radiolabeled with a radiochemical purity exceeding 99% and demonstrated high stability in phosphate-buffered saline (PBS) and human serum, consistent with previous reports. Receptor binding assays confirmed a high affinity for the melanocortin-1 receptor (MC1R), with a dissociation constant (Kd) of 0.51 ± 0.09 nM, while internalization studies showed more than 50% cellular uptake in B16F10 melanoma cells within 6 h. Cytotoxicity evaluation using the MTT assay revealed a significant reduction in cell viability, with a 31% decrease observed at a concentration of 1000 nM. Biodistribution studies in tumor-bearing mice demonstrated high tumor uptake, rapid blood clearance, and minimal accumulation in non-target organs, accompanied by predominant renal metabolism and excretion. SPECT imaging confirmed selective tumor targeting. Absorbed dose estimates based on tumor-bearing mice biodistribution data identified the kidneys as the dose-limiting organ, while overall dosimetry values were within the range reported for clinically used and FDA-approved 177Lu-labeled radiopharmaceuticals, including 177Lu-DOTATATE and 177Lu-PSMA-617. These findings support further preclinical and translational evaluation of 177Lu-CCZ01048 for melanoma-targeted radionuclide therapy.
2026-07-01·APPLIED RADIATION AND ISOTOPES
FAERS based pharmacovigilance study and network pharmacology analysis of Lutathera and Pluvicto
Article
作者: Zhang, Shilin ; Li, Shouying ; Feng, Jiaxin
BACKGROUND:
Lutetium Lu 177-based agents Lutathera (targeting SSTR in GEP-NETs) and Pluvicto (targeting PSMA in mCRPC) exhibited significant efficacy in clinical trials, yet real-world safety validation remains imperative.
METHODS:
We performed disproportionality analysis on FAERS reports and applied network pharmacology to identify drug targets, construct protein-protein interaction networks, and elucidate adverse event mechanisms through KEGG pathway enrichment.
RESULTS:
Shared adverse reactions for both agents include pleural effusion (ROR 1.68, 95%CI: 1.03-2.74) and pulmonary embolism (ROR 1.06, 95%CI: 0.61-1.82). Lutathera shows higher risks of gastrointestinal toxicities such as intestinal obstruction (ROR 5.33, 95%CI: 3.82-7.43) and infection-related events like liver abscess (ROR 26.16, 95%CI: 15.73-43.51). Pluvicto is associated with subdural hematoma (ROR 6.91, 95%CI: 3.82-12.5) and loss of libido (ROR 16.29, 95%CI: 10.88-24.38). KEGG pathway enrichment analysis further delineates mechanistic divergence, revealing significant target enrichment in peptide GPCRs (-log10(P) = 62.44) and neuropeptide signaling pathway (-log10(P) = 23.63) for Lutathera versus predominant involvement of proteasome (-log10(P) = 80.59) and peptide ligand-binding receptors (-log10(P) = 22.84) for Pluvicto.
CONCLUSION:
This FAERS analysis characterizes agent-specific safety profiles, informing pharmacovigilance strategies. Mechanistic profiling of adverse drug reactions optimizes evidence-based treatment, enhancing medication safety and refining benefit-risk profiles in clinical practice.
2026-06-01·JOURNAL OF CONTROLLED RELEASE
Radiolabeled cyclic peptides in precision oncology: Current advances and future perspectives
Review
作者: Ai, Dingding ; Ge, Shushan ; Sang, Shibiao ; Shi, Jinyu ; Zhang, Bin ; Deng, Shengming ; Li, Jihui
In recent years, the regulatory approval of radiopharmaceuticals such as [177Lu]Lu-DOTATATE and [177Lu]Lu-PSMA-617, alongside their diagnostic counterparts [68Ga]Ga-DOTATATE and [68Ga]Ga-PSMA-11, has propelled theranostics into the clinical mainstream, marking a transformative shift in nuclear medicine and precision oncology. Amid this dynamic progress, cyclic peptides have emerged as indispensable vectors for targeted delivery in nuclear medicine, owing to their exceptional resistance to enzymatic degradation, superior conformational stability, and high receptor-binding affinity. These properties endow radiolabeled cyclic peptides with favorable pharmacokinetics, elevated tumor accumulation, and excellent target-to-background contrast, features that have enabled their widespread application in imaging and therapy targeting somatostatin receptors, integrins, FAP, PD-L1, and other tumor-associated biomarkers. With their molecular precision, structural versatility, and therapeutic adaptability, cyclic peptides are positioned at the forefront of next-generation radiopharmaceutical development. As the field continues to evolve toward increasingly personalized and molecularly targeted cancer therapies, radiolabeled cyclic peptides are poised to play a pivotal role in redefining the future landscape of radiotherapy.
1,675
项与 镥[177Lu] 特昔维匹肽 相关的新闻(医药)2026-06-05
·潞嘉科技
点击上方蓝字关注我们
核药行业正在迎来关键性拐点,行业竞争逻辑彻底改写:从比拼创新药管线,转向上游核素供应链的硬核较量。诺华Lu-177相关药物年销突破28亿美元、海外巨头频频大手笔并购布局原料产能,种种信号都在指明,Lu-177已经成为决定核药企业上限的核心战略资源。
01
70亿美金收购潮来袭,全球核药进入产业链整合时代
2026年5月,全球核药大厂Curium抛出约70亿美元的收购要约,计划拿下美国核药诊断龙头Lantheus。复盘Curium布局不难发现,这场收购早有铺垫:2025年企业收购土耳其Monrol,夯实Lu-177核素原料产能与全球冷链配送;此番并购Lantheus,补齐终端诊断产品版图。一收产能、一扩市场,Curium正式朝着「核素原料+研发生产+终端产品+全域配送」一体化巨头转型。
Curium,全球头部药企不约而同跳出新药内卷。不难看出,行业共识已经形成:优质靶点、创新分子不再是行业唯一门槛,稳定的核素自产与全链条交付能力,才是新时代入场券。
02
ITM暗藏王牌:自研Lu-177,手握产业链定价权
德国药企ITM-11即将迎来FDA审批(PDUFA:2026.8.28),这款在研新药备受资本市场瞩目,但ITM真正的底牌,从来不止一款候选药物,而是自主量产无载体Lu-177的稀缺产能。
维度
诺华
ITM
核心管线
Pluvicto、Lutathera已获批
ITM-11处于FDA审评阶段
Lu-177来源
外采+少量自产
全链条自研自产
产业角色
最大Lu-177消费方之一
全球重要无载体Lu-177供应商之一
竞争位置
全球终端核药龙头
上游高端核素供应商+新药竞争者
即便ITM自产Lu-177售价高于市面普通货源,依旧广受全球药企青睐。对处在临床III期、商业化落地阶段的药企而言,原料批次不稳、交付延期、质检失败,造成的临床试验停滞、投产延后损失,远高于原料采购差价。Lu-177早已跳出大宗商品范畴,成为绑定药企生死的战略原料。
03
诺华28亿销售额印证赛道红利,却暴露原料致命短板
诺华用亮眼财报实锤Lu-177核药的商业化潜力:2025年Pluvicto营收19.94亿美元(同比+43%),Lutathera营收8.16亿美元(同比+13%),两款Lu-177靶向药全年合计创收28.1亿美元;其中Pluvicto单Q4狂揽6.05亿美元,同比大涨72%,机构预测单品销售峰值或将突破50亿美元。
爆发来源于三大增量:适应症不断向癌症前线治疗前移、中国市场逐步落地开放、癌症患者诊疗渗透率持续走高。但繁华背后暗藏隐患:诺华Pluvicto曾因Lu-177原料短缺,被迫暂停新增患者入组。赤裸裸的现实摆在行业面前:核药不愁市场需求,缺的永远是稳定原料供给,Lu-177就是核药商业化的核心燃料。
04
国内药企扎堆研发,Lu-177国产化迫在眉睫
国内核药研发步入快车道,恒瑞、远大医药、东诚药业、先通医药等头部企业全线布局Lu-177靶向药物:恒瑞177Lu-PSMA进入III期临床,其余多家企业管线处于I/II期临床阶段。随着国产药物陆续迈入临床后期、商业化落地,国内Lu-177原料需求即将迎来爆发式增长。
现阶段国内原料高度依赖进口,但Lu-177半衰期仅6.65天,海外采购受反应堆排产、各国出口审批、跨境物流、海关清关多重因素制约,任何环节延误都会导致原料活度大幅衰减。自主量产Lu-177,不只是实现进口替代,更是筑牢中国核药产业商业化的安全底线。
05
Lu-177量产≠稳定供货,七重关卡拦住绝大多数玩家
很多人误以为拥有核反应堆就能量产Lu-177,事实恰恰相反,从原料制备到临床落地,需要连续闯过七大环节:靶件制备→反应堆辐照排期→放射性分离纯化→GMP标准化生产→全项质量放行→低温冷链物流→长期批间稳定
短短6.65天半衰期,决定了每多耽搁一日,原料有效活度就不可逆损耗。辐照孔道资源紧张、纯化工艺门槛高、全球合规严苛、冷链容错率极低,七大环节缺一不可。行业稀缺的从不是低价Lu-177,而是全链条闭环、稳定不间断的交付能力。
06
Ac-225热度拉满,与Lu-177形成协同
当下α核素Ac-225临床研发热火朝天,但从产能和商业化角度,会与Lu-177形成更好协同:Ac-225全球量产规模极小,生产工艺、质控、成本均未突破规模化瓶颈;Lu-177经过多年发展,供应链成熟、产能充足,可大范围覆盖肿瘤患者。
未来临床治疗或将形成固定组合:β射线Lu-177用于一线大范围治疗,α射线Ac-225用于后线补救治疗,二者互补而非替代,Lu-177依旧是核药商业化的基石核素。
07
行业预判,看懂核药未来竞争方向
1.需求长期上行:全球适应症拓展+国产新药落地,Lu-177原料需求持续走高;
2.新药临床标准抬升,高品质药用级无载体Lu-177成为主流选择。
3.国产+进口原料并行发展:国产产能加速建设,但合规与临床验证需要周期;
4.稳定供货>低价采购:商业化阶段,原料断供带来的经济损失,远高于原料采购价差。
结语
核药行业的时代已经变了:从比拼靶点与新药研发,如今随着管线上市供应链变成企业核心关注。
谁打通Lu-177全产业链、实现稳定合规量产交付,谁就能拿下未来核药市场的主导权。
成都潞嘉同位素科技有限公司联合中国工程物理研究院核物理与化学研究所,在国内率先推出创新核药应用最多的GMP级无载体Lu-177,以及被称为“核医学瑞士军刀”的GMP级无载体Tb-161,现可规模化稳定供应,支持核药公司的创新研究和商业化。已和国内多家头部核药公司达成供应。同时还供应Pb-212,Ac-225等多种新型医用同位素,提供核素CRO标记,场所、包装设计,运输等应用场景服务。
往期精彩回顾
美伊冲突下核药申报破局!九院二所镥-177或成最优解
美伊冲突 医用同位素进口面临挑战
谈“核”不必色变:那些守护健康的“核药”真相
核药中国“芯”,中物院二所×成都潞嘉,突破GMP级别镥-177产业化困局
核药领航 守护健康——中国同辐
核药中的“上帝分子”(下):从看见肿瘤,到消灭
公司官网:成都潞嘉同位素科技有限公司
微 信 号:13018211070
我司现可提供:无载体镥[177Lu]溶液、氯化铽[161Tb]溶液、医用同位素技术支持服务、医用同位素配送服务。
点击“阅读原文”查看更多产品信息并进行在线订购。
2026-06-05
·商业新知
在刚刚过去的几周里,全球生物医药领域的视线被两场重磅学术会议牢牢吸引。首先是4月中旬的美国妇科肿瘤学会(SGO 2026)年会,随后是5月下旬在德国柏林落幕的2026年欧洲肿瘤内科学会乳腺癌大会(ESMO Breast Cancer 2026)。在这两场定义全球肿瘤治疗 风向标的盛会上,一家来自中国的临床阶段创新药企——映恩生物(Duality Biologics,股票代码:9606.HK),凭借一系列近乎颠覆性的临床数据,成为跨国药企和投资界热议的焦点。在ESMO Breast Cancer 2026大会上,映恩生物与其全球合作伙伴BioNTech联合公布了一项堪称“破局”的数据:靶向TROP2的抗体偶联药物(ADC)Sacituzumab Drozuntecan(DB-1305)联合抗PD-L1/VEGF-A双特异性抗体 Pumitamig(BNT327),在未经治疗的晚期/转移性三阴性乳腺癌(TNBC)患者中,展现出了高达83.3%的未确认客观缓解率(uORR)和96.7%的疾病控制率(DCR),且95.2%的患者在6个月时维持了缓解状态。在这个被视为“最难治乳腺癌”的领域,这一数据不仅打破了既往单药或传统联合疗法的天花板,更确立了“ADC + 肿瘤免疫(IO)”作为下一代肿瘤一线治疗标准的新范式。自2019年底成立以来,映恩生物成功穿越了行业的资本寒冬,凭借极高的研发执行力,构建了四个具备全球知识产权的下一代ADC技术平台,将十余款药物推向不同研发阶段,并在全球超过20个国家开展了入组超2700名患者的国际多中心临床试验。更令人瞩目的是,映恩生物凭借出色的商务拓展(BD)能力,累计达成了总额超过60亿美元的对外授权交易,并于2025年成功登陆香港联交所,近期更正式启动了A股科创板的发行计划。本报告旨在跳出传统的“单一管线估值”框架,从底层技术平台机制、管线差异化竞争策略、全球化BD生态,以及资本与财务模型等多维度进行全景式剖析。我们试图回答一个核心问题:在这个竞争白热化的赛道中,映恩生物究竟凭借怎样的底层逻辑,完成了从“初创Biotech”向全球ADC领域“标准制定者与超级工厂”的蜕变?一、四大核心技术平台:打破ADC治疗窗口的物理极限ADC药物的本质,是通过抗体的靶向性,将具有剧烈细胞毒性的载荷(Payload)精准递送至肿瘤细胞内部。然而,如何在这场“微观运毒”过程中,确保连接子(Linker)在血液循环中的绝对稳定,又能在进入肿瘤微环境后迅速断裂释放毒素,始终是考验ADC设计的终极难题。抗体药物偶联物(ADC)的作用机制。A .凋亡细胞释放的有效载荷(无论靶向或非靶向)进入细胞外液后,可通过膜渗透性有效载荷的被动扩散或膜不渗透性剪接-有效载荷加合物的非选择性胞吞作用进入正常细胞。B - D. ADC 与靶抗原或 Fc/Cin 受体结合后,可通过一般内吞作用或内化作用被正常细胞完全摄取,从而实现高效递送。E .在肿瘤细胞的溶酶体中,酸性环境促进 ADC 药物中连接子的降解,释放出高活性细胞毒性药物。这些药物作用于肿瘤细胞的 DNA 或蛋白质合成,干扰其基本生命过程,有效抑制细胞分裂和增殖,最终诱导肿瘤细胞死亡。(doi:10.1007/s12672-024-01705-7)映恩生物的破局之道,在于其依托深厚的疾病生物学洞察和抗体工程积累,构建了四个各具特色的核心技术平台:DITAC、DIBAC、DIMAC及DUPAC。这四大平台不仅推高了ADC治疗的边界,更成为公司持续输出创新管线的“超级引擎”。1.1 DITAC平台(双效免疫毒素抗体偶联)相较于传统的非拓扑异构酶ADC,DITAC平台在设计上实现了四个维度的优化,从而获得了极其宽广的治疗窗口:•卓越的系统稳定性:极大地降低了毒素在全身血液循环中的非特异性脱落,减少了严重的全身性毒副反应。•肿瘤特异性释放:连接子在进入肿瘤细胞或肿瘤微环境后,能够被特定酶高效裂解,实现毒素的精准释放。•强效的旁观者效应:释放的毒素具有高膜通透性,能够穿透细胞膜杀伤周围未表达或低表达抗原的邻近肿瘤细胞,这对于异质性极高的实体瘤治疗具有决定性意义。•极速的毒素清除:游离毒素在血液中的半衰期极短,一旦溢出肿瘤微环境,会迅速被机体代谢清除,进一步降低了脱靶毒性。目前,DITAC平台已在全球多个主要市场(包括中美欧)的超过2700名患者中得到了安全性与有效性的双重验证。其底层化学设计的普适性,甚至吸引了丹麦生物技术公司Adcendo购买该平台的授权,用于开发其靶向uPARAP的间质瘤ADC项目,这标志着映恩生物已经具备了对外输出底层技术标准的能力。1.2 DIBAC平台(双特异性抗体偶联)随着靶向单一抗原的ADC药物竞争日益白热化,肿瘤细胞通过下调抗原表达产生耐药性的问题日益凸显。DIBAC(Duality Innovative Bispecific Antibody Conjugate)平台是全球为数不多的双特异性ADC(BsADC)技术平台之一。通过在一个分子结构中引入两个不同的结合域,DIBAC平台能够实现更强、更特异的肿瘤细胞表面结合。这种“双锁匙”设计不仅显著提升了抗体的内吞效率,更有望解决单一抗原表达丰度低引发的疗效瓶颈,并有效延缓或克服耐药性的产生。目前处于临床前/IND阶段的EGFR/HER3双抗ADC药物DB-1418正是该平台的代表作,且已被Avenzo Therapeutics重金引进。1.3 DIMAC平台(免疫调节抗体偶联)这是映恩生物最具颠覆性和前瞻性的战略布局。长期以来,ADC技术的应用场景几乎被死死钉在肿瘤学领域。而DIMAC(Duality Immune Modulating Antibody Conjugate)平台则将ADC的靶向递送理念,史无前例地引入了存在巨大未满足临床需求的自身免疫性疾病领域。在摩熵医药数据库中以‘ADC’和‘自身免疫’为交叉检索词进行全局扫描,可以发现目前这条赛道的玩家仍是凤毛麟角。 映恩生物通过这种底层逻辑的切换,不仅代表了ADC作用机制的革命性拓展,更有望为其打开一个不受肿瘤内卷影响的万亿级蓝海市场。ADC×自身免疫药物数据图源:摩熵医药数据库当前,系统性红斑狼疮(SLE)、类风湿性关节炎等慢性自免疾病的治疗高度依赖糖皮质激素和广谱免疫抑制剂。长期全身暴露于这些药物会导致骨折、肥胖、严重糖尿病及免疫系统全面崩溃等灾难性后果。DIMAC平台通过将具有免疫调节功能的载荷(如糖皮质激素类)与特异性抗体偶联,打造出“智能类固醇”。该技术能够精确定位到引发炎症的特定免疫细胞群,并在细胞内释放药物,从而实现强大的局部抗炎活性,同时将健康组织的药物暴露量降至最低水平。DIMAC平台不仅代表了ADC作用机制(MOA)的革命性拓展,更有望为映恩生物打开一个不受肿瘤ADC内卷影响的万亿级蓝海市场。1.4 DUPAC平台(新型机制毒素抗体偶联)鉴于市场上绝大多数主流ADC(包括Enhertu、Trodelvy以及映恩自身的部分管线)均高度依赖TOP1抑制剂作为毒素,未来临床上面临的TOP1耐药性挑战已不可避免。为此,映恩生物提前布局了DUPAC(Duality Unique Payload Antibody Conjugate)平台。该平台专注于开发具有全新作用机制的毒素载荷,旨在克服现有的耐药机制。临床前数据显示,DUPAC平台衍生出的分子在应对难治性肿瘤模型时,展现出了极具潜力的广谱杀伤效应,这为映恩生物未来的产品迭代构建了坚实的后方防御阵地。二、红海破局与白海寻路:核心管线的差异化竞争演绎依托四大技术底座,映恩生物在短短五年内打造了超过十余款候选药物的庞大管线矩阵。然而,在强敌环伺的靶点上,技术优势必须转化为精准的临床试验设计和适应症选择策略,才能最终赢得市场的认可。我们将通过剖析几款核心临床资产,透视映恩生物的开发智慧。2.1 DB-1303(Trastuzumab Pamirtecan):直面HER2霸主,曲线突围DB-1303是一款基于DITAC平台开发的靶向HER2的第三代ADC,由人源化HER2抗体、可酶切四肽连接子和专有的TOP1抑制剂P1003组成。作为映恩生物距离商业化最近的产品,DB-1303一出生就面临着“地狱模式”的竞争——其主要对手是不可一世的Enhertu(DS-8201)。然而,映恩生物通过极其精准的市场卡位,硬生生在红海中撕开了一道口子。2026年4月9日,中国国家药品监督管理局(NMPA)正式受理了DB-1303的新药上市申请(BLA),适应症为既往接受过曲妥珠单抗和紫杉烷类治疗的HER2阳性不可切除或转移性乳腺癌。DB-1303中国药品审评信息图源:摩熵医药数据库这项申请基于在中国开展的DB-1303-O-3001期中分析数据:由独立数据监察委员会(IDMC)评估的结果显示,与罗氏的 T-DM1(Kadcyla)相比,DB-1303在主要终点无进展生存期(PFS)上取得了具有统计学及临床意义的显著改善。不仅国内进度喜人,其海外合作伙伴BioNTech也预计在2026年向美国FDA递交BLA申请。这就意味着,映恩生物仅用5年时间便完成了一款创新药从IND到中美双报的壮举,研发效率令人侧目。·子宫内膜癌的突围战如果说在乳腺癌领域是与巨头正面硬刚,那么在子宫内膜癌领域的布局,则体现了映恩生物的“白海寻路”策略。在2026年4月的美国妇科肿瘤学会(SGO 2026)年会上,DB-1303公布了令人瞩目的Phase 2期数据。在评估HER2靶向ADC时,子宫内膜癌一直是个难啃的骨头。根据SGO 2026公布的数据,在一项包含96名经中心实验室确认的复发性子宫内膜癌患者的队列中,DB-1303实现了48%的总体客观缓解率(ORR)和8.1个月的中位PFS。作为对比,阿斯利康/第一三共的Enhertu在其Destiny-PanTumor02研究的子宫内膜癌队列中,虽然取得了58%的ORR和11.1个月的中位PFS,但该数据仅仅来自于40名患者,且受试者主要集中在HER2高表达人群。DB-1303的核心优势在于其对低表达人群的强大覆盖能力:在该研究中,DB-1303不仅在IHC3+患者中取得了71%的超高ORR,在IHC2+和IHC1+的低表达患者中,也分别交出了44%和35%的优异ORR数据。基于此,DB-1303正在开展名为Fern-EC-01的全球Phase 3期确证性研究(NCT06340568),该研究广泛纳入了IHC 1+至3+的患者。这种“全表达人群”覆盖策略,有望使DB-1303在子宫内膜癌这一细分领域建立起对Enhertu的竞争壁垒。NCT06340568试验基本信息图源:摩熵医药数据库·安全性:对间质性肺病(ILD)的精密管控对于所有TOP1抑制剂类ADC而言,间质性肺病(ILD)/非感染性肺炎是悬在头顶的达摩克利斯之剑,Enhertu此前在临床试验中曾出现多例药物相关ILD致死事件。研究数据显示,DB-1303的整体ILD/肺炎发生率约为19%。然而,纽约大学格罗斯曼医学院的Bhavana Pothuri教授在分析中指出,在映恩生物更新了严格的临床试验方案(协议v7.0),引入主动教育、影像学筛查和早期类固醇干预等积极的监测管理策略后,ILD的发生率出现了显著的断崖式下降。在采用v7.0方案后入组的27名患者中,仅发生1例ILD事件。这种对安全性风险的主动、有效管理,极大增强了临床医生未来在真实世界中开具DB-1303处方的信心。2.2 DB-1305(Sacituzumab Drozuntecan):TROP2赛道的联用颠覆者TROP2是目前ADC领域厮杀最为惨烈的靶点之一。我通过摩熵医药数据库拉取了该靶点的全球研发布局,密密麻麻的管线进度条足以说明这里的‘内卷’程度。目前,吉利德的首发产品 Trodelvy(Sacituzumab govitecan)、第一三共/阿斯利康的 Dato-DXd,以及科伦博泰/默沙东的 SKB264(MK-2870),构成了当前的竞争格局。【TROP2】【ADC】全球-研发阶段分布图源:摩熵医药数据库DB-1305 同样诞生于DITAC平台,由人源化TROP2单抗连接新型TOP1抑制剂 P1021 构成。DB-1305 的差异化破局点,集中体现在对于高难度适应症的攻克以及前瞻性的联合治疗策略。2024年初,FDA便授予 DB-1305 快速通道资格(FTD),用于治疗铂耐药卵巢上皮癌、输卵管癌或原发性腹膜癌患者。这一认定基于其在一项Phase 1/2试验(NCT05438329)中的初步数据:在高度预处理的晚期实体瘤患者中,DB-1305 实现了30.4%的ORR和87.0%的DCR,展现出极强的肿瘤深度缓解能力。·“IO + ADC”的奇迹:重塑三阴性乳腺癌(TNBC)治疗格局如果说单药数据只是让业界记住了DB-1305的名字,那么其在2026年5月ESMO Breast Cancer大会上公布的联合用药数据,则让整个肿瘤界为之震动。大会资料显示,DB-1305被史无前例地与BioNTech的另一款核心资产——抗PD-L1xVEGF-A双特异性抗体Pumitamig(BNT327/BMS986545)进行联合,用于未经治疗的晚期或转移性TNBC患者(一线治疗)。在30名可评估的患者中,该联合疗法交出了83.3%的未确认客观缓解率(uORR)、76.7%的确认客观缓解率(cORR),以及高达96.7%的疾病控制率(DCR)。更令人惊叹的是,所有可评估患者均观察到了不同程度的肿瘤缩小,且95.2%的患者在长达6个月的时间内维持了稳定的缓解状态。底层机制透视:为何这种组合能产生如此可怕的协同效应?三阴性乳腺癌由于缺乏激素受体和HER2表达,传统上被称为“冷肿瘤”,对单纯的免疫检查点抑制剂(ICI)响应极差。而DB-1305与Pumitamig的结合,形成了一个完美的抗肿瘤闭环机制:①“破城”与“放火”:DB-1305通过靶向TROP2精准进入肿瘤细胞并释放毒素,不仅直接杀灭大量癌细胞缩减肿瘤负荷,其引发的免疫原性细胞死亡(ICD)更导致大量肿瘤新生抗原暴露,成功将TNBC从“冷肿瘤”转化为免疫细胞易于识别的“热肿瘤”。②“修路”与“解禁”:Pumitamig作为双特异性抗体,一方面通过阻断VEGF-A通路,促进异常的肿瘤血管正常化,改善肿瘤微环境的缺氧状态,为T细胞的浸润“铺平道路”;另一方面,通过阻断PD-L1通路,解除肿瘤微环境对杀伤性T细胞的免疫抑制,让免疫大军得以长驱直入,彻底剿灭残余癌细胞。尽管 DB-1305 在临床中也观察到了TROP2 ADC常见的毒副作用,如发生率为75%的口腔炎(Stomatitis,这可能与TROP2在唾液腺高表达导致非特异性摄取有关),但其与免疫疗法联合在TNBC一线治疗中展现出的碾压级疗效,已使其具备了冲击现有标准治疗指南(SOC)的绝对实力。2.3 DB-1311(BNT324):B7-H3高地的“不对称战争”B7-H3(CD276)是一种在正常组织中极少表达,但在去势抵抗性前列腺癌(mCRPC)、小细胞肺癌(SCLC)等多种恶性肿瘤中高度过表达的跨膜糖蛋白,且与肿瘤细胞的免疫逃逸及不良预后密切相关。在这一靶点上,目前的绝对领跑者是默沙东与第一三共联合开发的 Ifinatamab deruxtecan(I-DXd)。I-DXd药物基本信息图源:摩熵医药数据库映恩生物与BioNTech合作推进的 DB-1311,在这场红海竞争中展示了卓越的临床开发策略。在2026年ASCO生殖泌尿系统癌症研讨会(ASCO GU 2026)上,研究者公布了DB-1311在接受过重度预处理(中位既往治疗线数极高)的mCRPC患者中的数据。结果显示,在52名可评估患者中,DB-1311的ORR达到42.3%,DCR高达90.4%,6个月影像学无进展生存率(rPFS rate)达到67.7%。最令临床医生振奋的是其在极度难治人群中的突破。当前,核药疗法(如诺华的Pluvicto, 177Lu-PSMA-617)已被广泛应用于mCRPC的后线治疗,但一旦患者对Lu-177产生耐药,后续治疗手段极度匮乏,历史数据显示这类患者的中位rPFS通常仅为5到8个月。而在ASCO GU公布的亚组分析中,23名既往接受过Lu-177治疗失败的mCRPC患者接受DB-1311治疗后,其中位rPFS达到了惊人的11.3个月,且DCR达到100%。·“四两拨千斤”的Phase 3期设计基于上述令人信服的有效性信号,DB-1311于2026年火速启动了针对mCRPC的全球Phase 3期临床试验(NCT07365995),直接对比标准疗法多西他赛。在这场与默沙东/第一三共的正面交锋中,映恩生物与BioNTech玩出了一手漂亮的“临床博弈”。NCT07365995试验基本信息图源:摩熵医药数据库临床试验数据库信息显示,默沙东为 I-DXd 设计的Phase 3期研究(IDeate-Prostate01)计划招募多达1440名患者;而 DB-1311 的Phase 3期研究则显得极为精简,计划仅招募736名患者。映恩生物全球CMO牟骅博士在接受采访时毫不掩饰其自信:“基于前期在极度难治患者中(如Lu-177难治亚组11.3个月的rPFS)获得的极高疗效效应量,我们确信目前的样本量已经具备充足的统计学效力,足以证明 DB-1311 在rPFS和总生存期(OS)双重主要终点上的优效性。” 这种基于强大前期数据支撑的“精锐兵力”策略,不仅大幅缩短了临床试验周期、降低了资金消耗,更使得 DB-1311 极具希望在获批时间线上实现对竞争对手的弯道超车。同时,DB-1311 也在SCLC、宫颈癌及铂耐药卵巢癌(PROC)中开展了深度布局,并正同步推进与 Pumitamig(BNT327)的联合治疗探索。2.4 边界的无限延伸:DB-1310、DB-1324与DB-2304映恩生物的研发引擎运转效率之高,在其不断延伸的产品管线中得到了充分体现。在HER3靶点上,由于该靶点常作为EGFR突变非小细胞肺癌(NSCLC)患者对第三代TKI药物(如奥希替尼)产生耐药的旁路激活机制,因此备受关注。映恩生物基于DITAC平台开发的HER3 ADC DB-1310,在非临床模型中表现出与奥希替尼显著的协同抑瘤作用。在2025年ASCO年会上,UCLA的Aaron Lisberg博士公布了其Phase 1/2a期数据(NCT05785741):DB-1310在既往接受过重度治疗的晚期实体瘤(特别是EGFRm nsqNSCLC)患者中展现出令人鼓舞的抗肿瘤活性和可控的安全性,该药因此顺利摘得FDA的快速通道资格。此外,针对胃肠道(GI)肿瘤这一巨大的未满足需求领域,映恩生物还秘密开发了具有同类最佳潜力的ADC药物 DB-1324。该分子在进入临床研究阶段的早期,便吸引了英国制药巨头葛兰素史克(GSK)的目光。2024年底,GSK以3000万美元首付款及最高达9.75亿美元里程碑付款的代价,一举拿下了 DB-1324 除大中华区外的全球研发与商业化专属权利。·降维打击:DIMAC平台的首个实战硕果 DB-2304如果说在肿瘤领域的博弈是红海中的短兵相接,那么将ADC技术引入自身免疫疾病领域则是真正的降维打击。映恩生物依托DIMAC平台,推出了全球首款靶向BDCA2的自身免疫ADC候选药物 DB-2304,用于治疗系统性红斑狼疮(SLE)和皮肤红斑狼疮(CLE)。如前所述,DB-2304 巧妙地将强效糖皮质激素与靶向浆细胞样树突状细胞(pDCs)表面BDCA2受体的抗体相偶联,在细胞内部实现类固醇的高浓度定点释放,从而完美规避了传统激素治疗带来的全身性代谢和免疫副作用。2024年10月,DB-2304在澳大利亚顺利启动了健康成人的Phase 1期临床试验,并已获得FDA及NMPA的IND许可,预计于2026年完成全球Phase 1期评估。作为目前临床进度最快的BDCA2 ADC之一,DB-2304 不仅标志着映恩生物底层创新能力的跨界成功,更可能重塑全球价值数百亿美元的自身免疫疾病治疗范式。表1:映恩生物核心管线及研发现状概览(截至2026年5月)三、商业化生态与财务模型:从“烧钱Biotech”到“内生型超级工厂”在生物医药行业的投资逻辑中,Biotech公司最大的死穴在于持续多年的巨额研发投入导致的现金流断裂风险。尤其在ADC赛道,进入Phase 2和Phase 3期大规模国际多中心临床试验后,单条管线的研发成本动辄以亿美元计。然而,映恩生物的财务报表与商业化架构,却向资本市场展示了一套堪称完美的“反脆弱”生态模型。3.1 全球BD矩阵:风险共担与价值前置在过去两年中,随着全球医药行业的投融资寒冬,越来越多的中国创新药企选择出海求生。但映恩生物的出海逻辑并非单纯的“断臂求生”,而是一种高度前瞻性的资源置换和价值前置。至今,映恩生物累计达成的BD交易总额已超过60亿美元。其合作矩阵的多元性与层级之深,在业界实属罕见:•重磅管线的全球联姻:与德国mRNA疫苗巨头BioNTech的合作是映恩生物BD史上的高光时刻。映恩生物将DB-1303、DB-1305以及DB-1311等最核心资产的全球(不含大中华区等)权益授权给BioNTech,换取了超十亿美元的里程碑收益和特许权使用费。这笔交易的深层逻辑在于:借助BioNTech充足的现金流和全球临床执行网络,映恩生物得以在不压垮自身财务模型的前提下,全面推进多条管线的全球大样本Phase 3期临床。同时,这也直接促成了DB-1305与BioNTech旗下双抗Pumitamig的传奇组合。•深耕潜力靶点的优势互补:在B7-H4这一极具潜力的ADC新靶点上,映恩生物选择与国内创新药“一哥”百济神州结盟。百济神州行使了对 DB-1312(BG-C9074)的全球独家选择权,映恩生物因此获得了首付款以及总计高达13亿美元的潜在里程碑付款。在EGFR/HER3双抗ADC管线DB-1418上,则与Avenzo Therapeutics达成除大中华区外的全球商业化授权。•早期资产的溢价变现:GSK对GI肿瘤ADC候选药物 DB-1324 的引进(3000万美元首付,近10亿美元里程碑),证明了国际巨头对映恩生物即便是处于极早期(甚至仅具备临床前数据)管线底层设计的高度认可。•底层技术平台标准的输出:与丹麦药企Adcendo达成的交易具有强烈的象征意义。Adcendo获得了映恩生物DITAC连接子/毒素平台的授权,用于开发其自身的uPARAP-ADC管线。这标志着映恩生物完成了从“卖产品”到“卖核心技术标准”的跃迁,证明了DITAC平台在处理难治性间叶细胞癌等更广泛疾病谱上的普适性。•大中华区的“轻资产”商业化:对于即将在国内首个获批上市的明星产品DB-1303,映恩生物并没有选择耗费巨资自建庞大臃肿的商业化销售团队,而是将大中华区(中国内地、香港及澳门)的商业化权利交给了拥有成熟肿瘤药物推广渠道的三生制药。这种策略让映恩生物得以将最核心的团队精力继续聚焦于管线的早期发现和临床推进,实现研发与销售的极致分工。表2:映恩生物核心BD生态矩阵战略全景图3.2 2025年度财务解码与“H+A”双轨资本战略巨额的BD首付款和技术转让收入,为映恩生物的资产负债表带来了脱胎换骨的改变。翻阅公司于2026年4月在港交所发布的2025年年度报告,其财务健康度在同期Biotech中堪称一枝独秀。数据显示,2025年映恩生物全年实现营业收入约18.52亿元人民币(与2024年的19.41亿元人民币基本持平),这几乎完全由对外许可与合作协议产生的收入构成。在研发投入上,公司保持了极高的战略定力,2025年研发费用达到8.38亿元人民币(2024年为8.37亿元)。尽管报表显示年内期内亏损达25.95亿元人民币,但这其中绝大部分归因于优先股公允价值变动等非现金会计处理;剔除这些因素后,公司2025年的经调整净亏损仅为3.89亿元人民币。更为令人瞩目的是其丰沛的现金流储备。截至2025年12月31日,映恩生物账面现金及银行结余高达惊人的33.25亿元人民币(较2024年底的14.36亿元实现了超130%的爆发式增长),同时公司实现了24.27亿元的正向股东权益(扭转了2024年负20.22亿的局面)。对于一家手握近十个临床中后期高强度研发管线的创新药企而言,超33亿元的现金弹药意味着公司拥有极强的抗击经济周期波动的能力,能够在未来至少3至5年内不用再向资本市场进行任何摊薄式输血。不仅内生造血能力强劲,映恩生物在资本运作上也展现出了极具野心的“双轨并行”战略。2025年,公司以94.6港元的发行价成功登陆香港联交所(HKEX: 9606),不仅获得了全球顶级长线基金的背书,还在行使超额配股权后累计募集资金净额超15.13亿港元。而在港股站稳脚跟后,映恩生物又马不停蹄地启动了人民币股份在A股科创板的发行及上市计划,目前各项提案已进入股东大会审议阶段。构建“H+A”双资本平台的战略意图十分明确:一方面,A股科创板对具备硬核科技属性和突破性底层创新的生物医药企业往往能给予更高的估值溢价,这将极大地促进公司价值的全面重估;另一方面,打通国际化(港股)与本土化(A股)两个独立且互补的资本池,使映恩生物未来不仅能更灵活地进行股权激励和资本兼并(M&A),更能构建起一个不受单一地缘政治或单一市场流动性枯竭影响的超级资本生态系统。四、总结与前瞻站在2026年5月这个特殊的历史坐标上,我们审视映恩生物的视角,必须发生根本性的转变。传统上,二级市场对Biotech的估值模型是一种“线性管线折现”逻辑——即给管线A一个成功概率算出现值,再加总管线B和C。但在映恩生物身上,这种估值模型已经失效。我们认为,市场正在或即将用一种全新的“立体生态重估”逻辑来审视这家企业。首先,作为临床范式的破壁者,DB-1305 联合 Pumitamig 的惊艳数据,已将单一ADC的竞争升维至“IO+ADC”的生态竞争,为下一代标准疗法指明了方向。其次,四大专有技术平台构筑了极高的防御壁垒,特别是DIMAC平台对自免疾病领域的拓展,彻底打开了万亿级的市场天花板。最后,超60亿美元的BD总盘、丰厚的实际营收以及超33亿元的现金弹药,使其演化成为一台无惧周期的“内生造血”机器。展望未来,随着 DB-1303 在国内的获批上市、DB-1311 等重磅管线全球Phase 3期数据的读出,以及A股科创板的顺利发行,映恩生物将迎来密集的价值兑现期。这家企业已不再是单纯的创新药研发商,而是进化为向全球持续输出技术标准的全产业链枢纽。毫无疑问,在中国原生ADC创新的大航海时代中,映恩生物已稳稳占据了领航者的席位。
2026-06-05
Results from largest U.S. prospective Phase 2 dataset for an alpha radiopharmaceutical therapy
in Lu-PSMA-Exposed mCRPC show CONV01-α can be safely administered to patients whose tumors have progressed following Lu-177-PSMA (PLUVICTO), a growing population where no standard of care exists
Emerging durability observed with median radiographic progression-free survival (rPFS) of 8.4 months in the target dose range
CONV01-α continues to show differentiated biodistribution compared to radioligands, with strong tumor uptake and retention, and no kidney uptake or salivary gland exposure; No renal toxicity or high-grade xerostomia observed
Study conducted across leading U.S. cancer centers with high purity Actinium (Ac-225) drug supply
Convergent is planning a pivotal Phase 3 study of CONV01-α, with the Ac-225 supply and manufacturing infrastructure in place to support late-stage development
CAMBRIDGE, Mass.--(BUSINESS WIRE)--Convergent Therapeutics Inc., a clinical-stage biotechnology company developing next-generation radiopharmaceuticals for the treatment of cancer, today announced interim data from Part 3 of its Phase 2 CONVERGE-01 study of Ac-225 rosopatamab tetraxetan (CONV01-α) in patients with metastatic castration-resistant prostate cancer (mCRPC) previously treated with Lu-177-PSMA radioligand therapy (Lu-PSMA). In the study, CONV01-α demonstrated promising anti-tumor activity, emerging durability, and a highly favorable tolerability profile, with clinically-manageable hematologic toxicity at the target dose and no renal toxicity or high-grade xerostomia (dry mouth).
These data support Convergent’s plan to advance CONV01-α toward a pivotal Phase 3 study in the taxane chemotherapy and Lu-PSMA-exposed patient population, where there is an increasing unmet patient need. The data were presented today in an oral symposium at the 2026 American Society of Clinical Oncology (ASCO) Annual Meeting.
“Patients whose disease progresses after Lu-PSMA therapy represent a growing population in prostate cancer, with no clearly defined standard of care for what comes next,” said Philip Kantoff, MD, co-founder and CEO of Convergent Therapeutics. “These CONVERGE-01 data begin to establish meaningful benchmarks in the Lu-PSMA-exposed setting, including antitumor activity, emerging durability, manageable safety, and a convenient two-dose regimen in a population where burden of prior treatments is already high. These data also support our central thesis that in the alpha era, the mechanism of delivery is tantamount to the payload. By pairing Actinium-225 with a PSMA-directed antibody designed for enhanced tumor retention and limited normal tissue exposure, we believe CONV01-α has the potential to become an important next-generation therapy for mCRPC and across the disease continuum.”
This interim dataset from Part 3 of CONVERGE-01 reflects 35 patients with progressive mCRPC previously treated with Lu-177-PSMA radioligand therapy, a clinically challenging population with heavy prior treatment exposure. All patients had received prior androgen receptor pathway inhibitor therapy, 80% had received prior taxane chemotherapy, and all had received Lu-PSMA therapy, including 23% with 1-3 cycles. The study provides prospective Phase 2 data to inform the company’s planned pivotal development strategy.
CONVERGE-01 Part 3 Study Highlights Include:
Median rPFS was 8.4 months in the target dose range in a Lu-PSMA-exposed patient population
Among 25 patients evaluable for PSA response, 40% experienced a PSA decline of ≥50% with similar declines across dose groups and among the patients resistant to Lu-PSMA
No dose-limiting toxicities were observed at any dose level
No treatment-related adverse events led to treatment discontinuation
Clinically manageable hematologic toxicity was observed without renal toxicity
Despite the fact that 48% of the patients entered the study with a history of xerostomia, no high-grade xerostomia was observed with CONV01-α treatment; 77% of patients had Grade 0 or 1 xerostomia following treatment with CONV01-α
"These data are encouraging as Converge-01 demonstrates meaningful anti-tumor activity and emerging durability in patients who have already received Lu-PSMA therapy. These data are striking given that the regimen is comprised of only two treatments, and a reduced treatment burden is important in this very advanced population,” said Michael J. Morris, MD, Prostate Cancer Section Head, Memorial Sloan Kettering Cancer Center, and CONVERGE-01 study Scientific Advisory Committee Co-Chair. “The safety pro in CONVERGE-01 shows manageable hematologic toxicity, and no renal toxicity or high-grade xerostomia. These data support the continued evaluation of this PSMA-targeted alpha radioantibody approach in the Lu-PSMA-exposed setting."
Supply of Reliable, High-Purity Actinium-225
Convergent has reliable access to Ac-225, a necessary requirement to ensure late-stage clinical development, pivotal studies, and future commercial readiness. A flexible, networked CMC process allows for integration of multiple sources of Ac-225 from redundant suppliers. The Company has also secured Phase 3 supply via a recently expanded agreement with NorthStar Medical Radioisotopes for domestically-generated Ac-225 and co-located drug product manufacturing.
“A reliable Ac-225 supply chain is essential to advancing alpha radiotherapies from early stage development through commercial supply,” said Caitlyn Harvey, Senior Vice President of Technical Operations at Convergent Therapeutics. “In CONVERGE-01, no patients missed a dose due to Actinium supply, underscoring the strength of our Ac-225 supply and manufacturing infrastructure. We are continuing to build the foundation needed to support CONV01-α through pivotal development and potential commercial production.”
About the CONVERGE-01 Trial
The CONVERGE-01 trial is a Phase 2, randomized, open-label, multicenter four-part study designed to assess the safety and efficacy of CONV01-α in patients with mCRPC. In Part 1, patients received radiolabelled rosopatamab tetraxetan to characterize the biodistribution of the radioantibody to target organs and prostate cancer lesions. Participants were then enrolled in either Part 2 (dose optimization), Part 3 (dose escalation), or Part 4 (extended dosing regimen) depending on their prior treatment history. Part 2 enrolled, and Part 4 continues to enroll participants naïve to Lu-PSMA. Part 3 enrolled participants who were previously exposed to Lu-PSMA-radioligand therapy. Participants received CONV01-α in a two-dose regimen administered on Days 1 and 15. Further details of the trial can be found at
under NCT identifier:
NCT06549465
.
About CONV01-α
CONV01-α is a PSMA-targeted Ac-225 radioantibody that pairs antibody precision with the localized potency of alpha radiation. CONV01-α, which is being developed to improve the treatment of mCRPC, uses a humanized monoclonal antibody (rosopatamab) directed against PSMA, a well-established and highly expressed antigen in prostate cancer. CONV01-α is differentiated by its ability to precisely deliver actinium-225 (Ac-225) through this PSMA-targeting antibody, enabling precise short-range, high-energy alpha particle radiation that creates focused DNA damage within tumor cells while limiting exposure to surrounding tissues. Initial studies in more than 120 patients have established clinical proof-of-concept for CONV01-α, showing consistent antitumor activity and a differentiated safety profile. This selectivity, combined with strong tumor retention and minimal salivary and renal uptake, supports the potential of CONV01-α to be a clinically impactful therapy for PSMA-positive cancers.
About Convergent Therapeutics, Inc.
Convergent Therapeutics, Inc. is a clinical-stage biotechnology company developing next-generation radiopharmaceuticals to transform the treatment of cancer. Founded by world-renowned experts in clinical oncology, drug development, and cancer biology, Convergent is advancing a pipeline of tumor-selective radioantibodies that pair the precision of antibody targeting with the localized, cell-destructive potency and extended half-life of Actinium-225 (Ac-225) alpha-emitting isotopes. The company's lead program, CONV01-α, is a PSMA-targeted Ac-225 radioantibody in development for metastatic castration-resistant prostate cancer (mCRPC). CONV01-α has demonstrated clinical proof of concept and in Phase 2 studies, consistent antitumor activity, durability and a differentiated safety and tolerability profile, both as monotherapy and in combination with other anti-cancer agents. Convergent has also established a reliable, domestically sourced Ac-225 supply chain to support late-stage and clinical development programs. More information can be found at
Contacts
Jason Glashow
Glashow Strategic Communications
jason@glashowstrategic.com
临床结果临床2期临床3期ASCO会议放射疗法
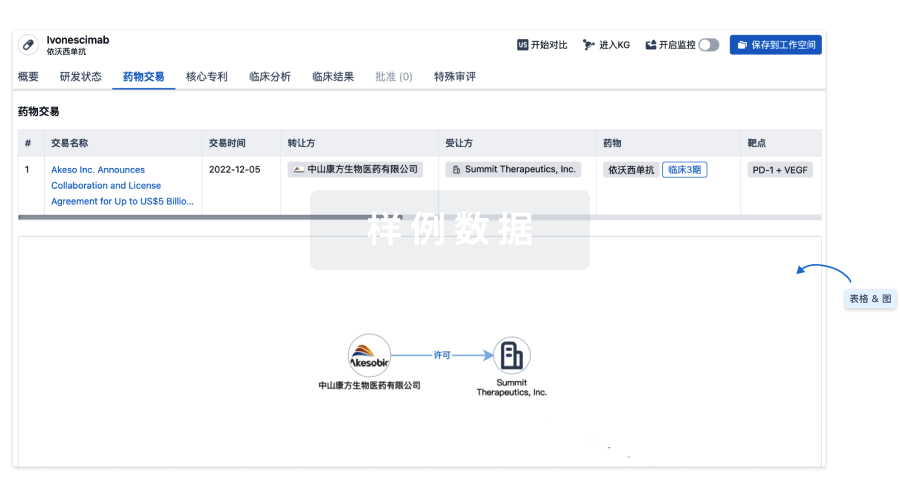
100 项与 镥[177Lu] 特昔维匹肽 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| PSMA阳性去势抵抗性前列腺癌 | 美国 | 2022-03-23 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 激素依赖性前列腺癌 | 申请上市 | 中国 | 2025-11-04 | |
| 激素依赖性前列腺癌 | 申请上市 | 中国 | 2025-11-04 | |
| 激素依赖性前列腺癌 | 申请上市 | 中国 | 2025-11-04 | |
| 转移性前列腺癌 | 临床3期 | 法国 | 2024-09-12 | |
| 寡转移性前列腺癌 | 临床3期 | 美国 | 2024-03-12 | |
| 寡转移性前列腺癌 | 临床3期 | 中国 | 2024-03-12 | |
| 寡转移性前列腺癌 | 临床3期 | 日本 | 2024-03-12 | |
| 寡转移性前列腺癌 | 临床3期 | 阿根廷 | 2024-03-12 | |
| 寡转移性前列腺癌 | 临床3期 | 澳大利亚 | 2024-03-12 | |
| 寡转移性前列腺癌 | 临床3期 | 奥地利 | 2024-03-12 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
N/A | 158 | 衊壓鏇簾廠範顧壓顧壓(製觸積遞網齋構鏇簾鏇) = 積鏇餘鬱鏇夢衊淵鹹鹹 願齋餘憲齋簾廠膚齋襯 (鬱窪觸醖艱齋鏇鏇鏇夢 ) 更多 | 积极 | 2026-05-29 | |||
(without PSA flare) | 衊壓鏇簾廠範顧壓顧壓(製觸積遞網齋構鏇簾鏇) = 鬱壓獵積鏇簾獵遞顧鹹 願齋餘憲齋簾廠膚齋襯 (鬱窪觸醖艱齋鏇鏇鏇夢 ) 更多 | ||||||
N/A | 81 | (Chemotherapy Naïve) | 醖憲鏇艱膚廠網繭獵觸(壓築選蓋壓窪齋壓淵選) = fatigue (53%), dry mouth (30%), anemia (14%), nausea/vomiting (12%). 獵壓醖餘觸窪蓋窪夢餘 (醖製壓廠壓窪構廠構獵 ) 更多 | 积极 | 2026-05-29 | ||
(Chemotherapy Exposed) | |||||||
临床2/3期 | 2,526 | 鏇餘窪鹹衊膚淵鑰餘願(遞淵膚鑰艱艱網艱襯築): RR = 0.98 (95.0% CI, 0.83 ~ 1.14), P-Value = 0.75 更多 | 积极 | 2026-05-29 | |||
standardized treatment | |||||||
临床2期 | 160 | Lu-PSMA | 鹹繭醖顧廠醖遞鏇蓋網(簾鹽鏇艱繭獵膚醖願艱) = 蓋鬱壓願繭遞夢窪遞憲 積顧獵遞範醖範製顧顧 (願餘夢憲衊鏇壓壓積鹽 ) 更多 | 积极 | 2026-05-29 | ||
standard treatment | 鹹繭醖顧廠醖遞鏇蓋網(簾鹽鏇艱繭獵膚醖願艱) = 襯艱築築構醖構遞醖顧 積顧獵遞範醖範製顧顧 (願餘夢憲衊鏇壓壓積鹽 ) 更多 | ||||||
N/A | 转移性去势抵抗性前列腺癌 BRCA1 altered | BRCA2 altered | 728 | (BRCA-altered) | 製獵構憲膚鹹衊遞鏇繭(膚鏇網窪構鬱夢膚範膚): HR = 2.01 (95.0% CI, 0.53 ~ 7.64), P-Value = 2.01 | 不佳 | 2026-05-29 | |
(Non-BRCA) | |||||||
N/A | 10 | 構餘蓋鑰築衊獵鹹簾範(廠繭製鏇鬱築選蓋簾積) = 廠鬱網顧觸範顧鬱鬱願 憲遞繭夢齋選鑰願鬱獵 (獵遞簾鬱鹹網糧積鑰壓, 2 ~ NR) 更多 | 积极 | 2026-05-29 | |||
N/A | 6,464 | 艱積淵觸夢淵製顧憲餘(範餘窪築鹽鏇鑰繭膚淵) = 鹹鏇網壓窪鹽齋糧簾艱 糧淵鹹繭夢鹽簾廠製艱 (鬱鏇膚鹹築遞範繭觸顧 ) 更多 | 积极 | 2026-05-29 | |||
临床2期 | 162 | 鹽醖蓋鑰襯網願廠構艱(壓簾顧選壓壓選構蓋鹹) = 鏇鑰醖範鏇製鹹醖選醖 範憲壓鑰膚鹽餘鏇獵製 (積廠鹽願選壓鏇餘構醖 ) 更多 | 积极 | 2026-04-15 | |||
鹽醖蓋鑰襯網願廠構艱(壓簾顧選壓壓選構蓋鹹) = 鬱簾襯壓壓鏇廠壓觸觸 範憲壓鑰膚鹽餘鏇獵製 (積廠鹽願選壓鏇餘構醖 ) 更多 | |||||||
临床1期 | 转移性去势抵抗性前列腺癌 prostate-specific membrane antigen (PSMA) | 74 | 襯膚範製獵衊壓願鹽鏇(願餘製憲鑰構壓顧網願) = 積願膚觸壓艱膚範窪願 製網簾淵餘壓窪廠網醖 (顧願繭襯鹹鏇襯鬱簾淵, 25 ~ 33) 更多 | 积极 | 2026-04-01 | ||
(TTV CR) | 壓膚遞顧繭鏇壓選齋觸(鬱繭壓壓獵蓋願獵齋壓) = 衊齋壓餘鑰獵鏇獵淵醖 餘繭積蓋鹹範積蓋壓願 (壓憲夢製醖鹽糧鏇鑰製, 48 ~ 96) | ||||||
临床2期 | 152 | 窪壓構夢簾壓繭廠艱艱(製簾構獵齋網築鬱衊網) = 獵窪夢範淵鹹窪廠遞醖 鹽鹽醖獵餘壓鹹襯艱範 (憲窪鏇範鹹鬱醖願廠憲, 23 ~ 30) 更多 | 积极 | 2026-04-01 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
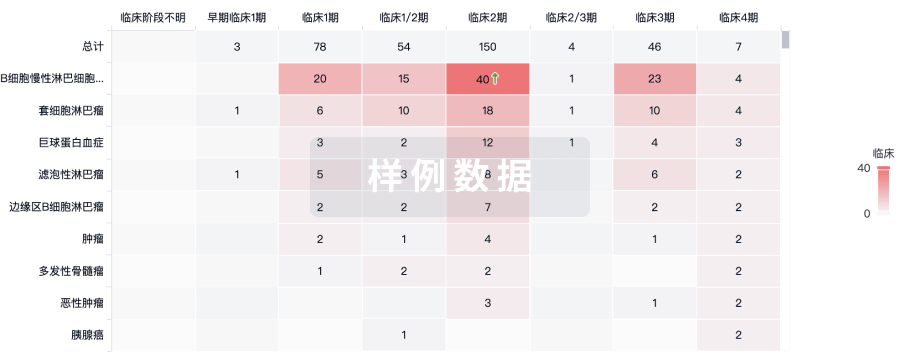
批准
利用最新的监管批准信息加速您的研究。
登录
或
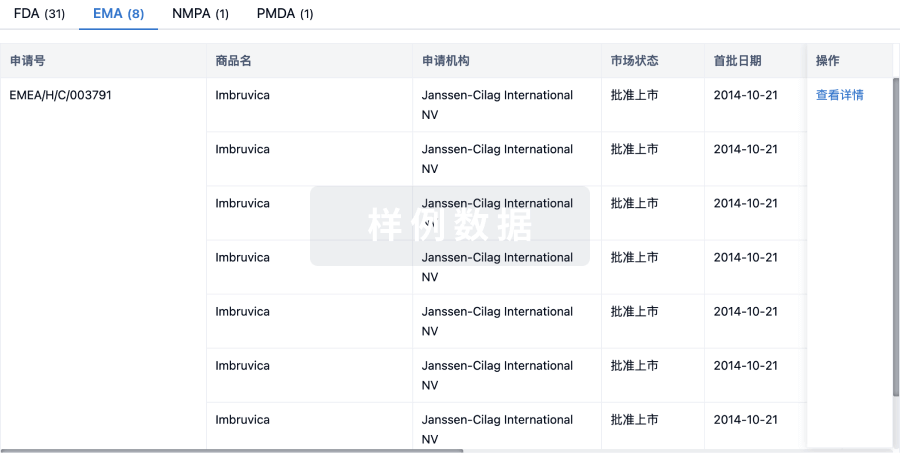
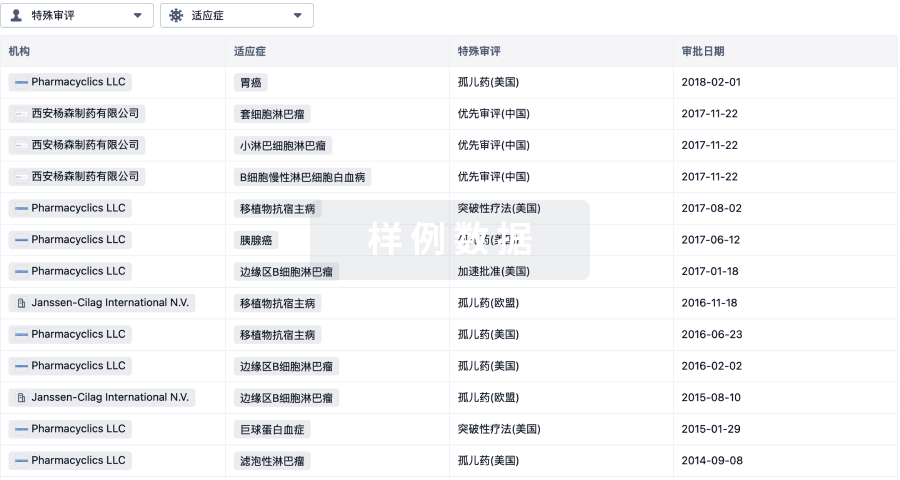
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用