双抗+双抗!康方AK104+AK112联合疗法启动多项临床研究,针对胃癌和肝癌
2024年1 月 9 日,康方生物在 ClinicalTrials.gov 上登记启动了AK104(卡度尼利单抗)+ AK112(依沃西单抗)联合疗法的两项 II 期临床试验,分别针对一线胃及胃食管交界处癌(登记号:NCT06196697)、二线肝细胞癌(登记号:NCT06196775)。
卡度尼利单抗,是康方生物自主研发的PD-1/CTLA-4双特异性抗体新药,是全球首款获批的基于PD-1的双特异性抗体药物,也是全球首款获批的PD-1/CTLA-4双特异性抗体。该药于2022年6月获国家药监局批准上市,是我国首个获批上市的用于晚期宫颈癌治疗的肿瘤免疫药物,用于治疗既往接受过含铂化疗治疗失败的复发或转移性宫颈癌患者,填补了宫颈癌免疫治疗的市场空白。卡度尼利单抗注射液(开坦尼)在胃癌、肝癌、肺癌、宫颈癌、肾癌、食管鳞癌等多种恶性肿瘤上显示出较好的疗效和安全性。相关临床研究数据显示,卡度尼利单抗与抗PD-1单抗联合抗CTLA-4单抗的联合疗法相比,毒性显著降低,具有明显的安全性和疗效优势。
依沃西单抗是康方生物自主研发的全球首创PD-1/VEGF双特异性抗体,处于全球临床开发进度最快。基于康方生物独特的Tetrabody技术设计,依沃西可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,AK112作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路,从而增强抗肿瘤活性。目前依沃西单抗在国内已经有 1 项新药上市申请获 NMPA 受理(受理号:CXSS2300061),联合培美曲塞和卡铂用于经 EGFR 酪氨酸激酶抑制剂(EGFR-TKI)治疗后进展的 EGFR 突变的局部晚期或转移性非鳞 NSCLC 的治疗,有望在 2024 年 Q2 获批上市,成为全球首个肿瘤免疫+抗血管机制的双抗新药。
AK104 联合化疗一线治疗胃癌的 III 期临床 AK104-302 研究期中分析结果显示,卡度尼利联合化疗对比安慰剂联合化疗显著延长了全人群(无论 PD-L1 表达)患者的总生存期(OS),达到预设的优效性标准。且对于 PD-1 单抗联合化疗响应不佳的 PD-L1 低表达及阴性人群的治疗同样高效。这两款基于 PD-1 的双特异性抗体新药的联合应用,有望在现有以 PD-1/PD-L1 抑制剂为基石的免疫疗法的基础上,进一步提升免疫疗法的临床效果。在安全性方面,AK104 特异性结合 PD-1 和 CTLA-4 两个靶点、半衰期短,安全性良好可控。此前临床研究显示,卡度尼利在总体安全性上明显优于已上市的 CTLA-4 抑制剂,与已上市的 PD-1/PD-L1 抑制剂相当。此前,AK112 单药临床资料也表明,整体安全性与目前已上市的 PD-1/PD-L1 抑制剂相比更优或相当。因此,康方预期两者联用的安全性比其他 PD-1/PD-L1 抑制剂联合抗血管生成药物更优或相当。
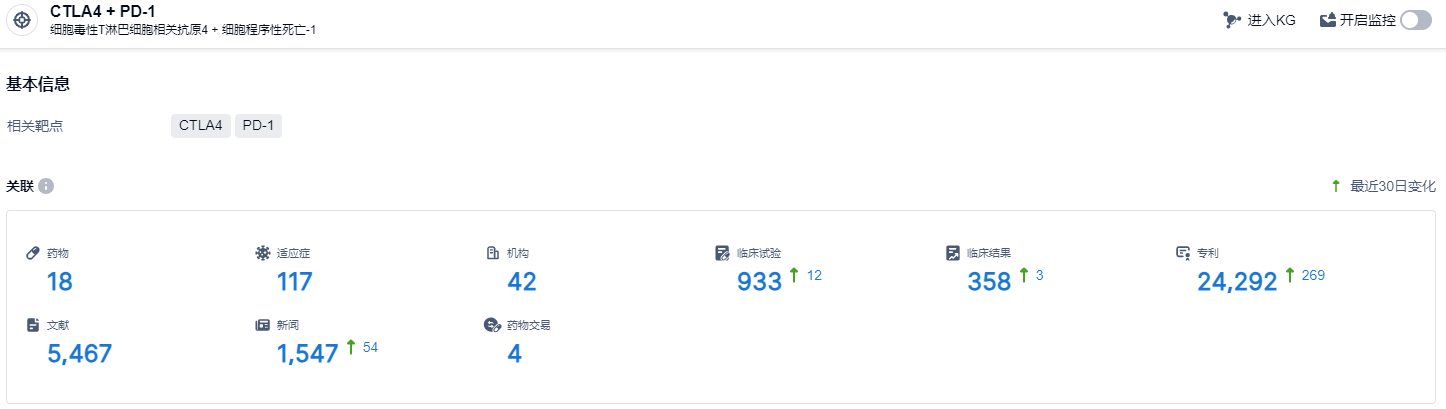
根据智慧芽新药情报库所披露的信息 (点击下方卡片直达 CTLA4 + PD-1靶点注册登录后可免费获得该靶点下的在研药物、适应症、研发机构、临床试验等详细信息),截止到 2024年1月12日,CTLA4 + PD-1靶点共有在研药物18个,包含的适应症有117种,在研机构42家,涉及相关的临床试验933件,专利多达24292件……AK104 + AK112是全球首个进入临床研究阶段的“双抗”+“双抗”联合疗法,两款基于PD-1的双特异性抗体新药的联合应用,有望在现有以PD-1/L1抑制剂为基石的免疫疗法的基础上,进一步提升免疫疗法的临床效果。