预约演示
更新于:2025-12-06

EQRx, Inc.
更新于:2025-12-06
概览
标签
肿瘤
化学药
疾病领域得分
一眼洞穿机构专注的疾病领域
暂无数据
技术平台
公司药物应用最多的技术
暂无数据
靶点
公司最常开发的靶点
暂无数据
| 排名前五的药物类型 | 数量 |
|---|---|
| 小分子化药 | 2 |
| 化学药 | 1 |
关联
3
项与 EQRx, Inc. 相关的药物作用机制 EGFR T790M抑制剂 [+2] |
在研机构 |
原研机构 |
在研适应症 |
最高研发阶段批准上市 |
首次获批国家/地区 中国 |
首次获批日期2020-03-17 |
靶点 |
作用机制 JAK1抑制剂 |
在研适应症 |
非在研适应症- |
最高研发阶段临床2期 |
首次获批国家/地区- |
首次获批日期- |
靶点 |
作用机制 PARP1抑制剂 |
在研机构 |
原研机构 |
在研适应症 |
非在研适应症- |
最高研发阶段临床前 |
首次获批国家/地区- |
首次获批日期- |
7
项与 EQRx, Inc. 相关的临床试验NCT05712941
A Multiregional, Randomized, Double-Blinded, Placebo-Controlled Phase 3 Study of Lerociclib With Letrozole, Versus Placebo in Combination With Letrozole, in Participants With Advanced/Metastatic or Recurrent, Grade 1 or Grade 2 Endometrioid Endometrial Carcinoma
This is a randomized, double-blinded, placebo-controlled Phase 3 clinical trial to compare the combination of lerociclib (administered at 150 mg twice a day (BID) with letrozole (administered at 2.5 mg once a day (QD) to that of placebo with letrozole (2.5 mg QD) in female participants with Grade 1 or Grade 2 (ie, low-grade histology) endometrioid endometrial cancer (EC) and advanced/metastatic or recurrent disease.
The study population will consist of female participants with endometrioid EC who are treatment-naïve in the advanced/metastatic setting (ie, the first-line [1L] population). Participants may have received prior adjuvant chemotherapy/chemoradiation for localized disease if the adjuvant therapy was administered ≥ 6 months prior. All participants must also be naïve to prior endocrine therapy for EC, and confirmed as medically postmenopausal to be eligible.
The study will comprise a Screening Period of up to 28 days in duration; a Study Treatment Phase; a Safety Follow-up Period spanning the time of study treatment discontinuation-including discontinuation due to confirmed disease progression, as applicable-through 28 days after the participant's last dose of any study intervention or the start of subsequent anticancer therapy (whichever occurs first); and a Survival Follow-up Period that will continue until the participant's death or until at least 50% of all study participants have died (whichever occurs first).
While receiving their randomized assigned study treatment, participants will undergo imaging assessments via computed tomography (CT) of the chest/abdomen/pelvis with contrast- or, if CT is medically contraindicated (eg, due to iodine allergy), via magnetic resonance imaging (MRI) with gadolinium-every 8 weeks for the first 12 months and then every 12 weeks thereafter.
The study population will consist of female participants with endometrioid EC who are treatment-naïve in the advanced/metastatic setting (ie, the first-line [1L] population). Participants may have received prior adjuvant chemotherapy/chemoradiation for localized disease if the adjuvant therapy was administered ≥ 6 months prior. All participants must also be naïve to prior endocrine therapy for EC, and confirmed as medically postmenopausal to be eligible.
The study will comprise a Screening Period of up to 28 days in duration; a Study Treatment Phase; a Safety Follow-up Period spanning the time of study treatment discontinuation-including discontinuation due to confirmed disease progression, as applicable-through 28 days after the participant's last dose of any study intervention or the start of subsequent anticancer therapy (whichever occurs first); and a Survival Follow-up Period that will continue until the participant's death or until at least 50% of all study participants have died (whichever occurs first).
While receiving their randomized assigned study treatment, participants will undergo imaging assessments via computed tomography (CT) of the chest/abdomen/pelvis with contrast- or, if CT is medically contraindicated (eg, due to iodine allergy), via magnetic resonance imaging (MRI) with gadolinium-every 8 weeks for the first 12 months and then every 12 weeks thereafter.
开始日期2023-04-18 |
申办/合作机构 |
NCT05493501
A Randomized, Three-Arm, Open-Label Phase 3b Clinical Trial of Aumolertinib, Versus Aumolertinib With Chemotherapy, Versus Osimertinib for Patients With Metastatic NSCLC and an EGFR Mutation (TREBLE)
Aumolertinib is a third-generation epidermal growth factor receptor (EGFR) tyrosine kinase inhibitor (TKI) that targets EGFR mutations. The reason for this study is to learn whether adding chemotherapy to a new investigational drug called aumolertinib helps to slow or stop cancer growth in people with EGFR mutation-positive, locally advanced or metastatic non-small cell lung cancer (NSCLC). The study will compare this new combination of drugs to osimertinib, given alone. Aumolertinib given alone will also be used in the study, and it will be looked at in comparison with osimertinib given alone.
This is a randomized, open-label study with 3 different groups that are listed below. "Randomized" means the study treatment participants take will be chosen by chance (decided at random by a computer). "Open-label" means that the participant, the study doctor, and the Sponsor will know which study treatment each participant is receiving.
Participants will be randomly assigned to one of the following 3 treatment groups:
* Group 1: Treatment with aumolertinib alone, taken orally (by mouth) as a pill once a day. Around 100 participants will be randomly assigned to this group.
* Group 2: Treatment with aumolertinib taken orally as a pill once a day, in combination with chemotherapy given intravenously (IV; through a needle placed in a vein) on the schedule provided by the study doctor. Around 200 participants will be randomly assigned to this group.
* Group 3: Treatment with osimertinib alone, taken orally as a pill once a day. Around 200 participants will be randomly assigned to this group.
Because there will be twice as many participants in Group 2 and Group 3 as in Group 1, the chance of a participant being randomly assigned to either of those groups is twice as likely as being assigned to Group 1.
Participants can continue to receive study treatment as long as they have not withdrawn consent, as long as they choose to continue to receive study treatment and are judged by their doctor to continue to receive clinical benefit from receiving the study treatment, and as long as no other study treatment and/or study discontinuation criteria are met .
This is a randomized, open-label study with 3 different groups that are listed below. "Randomized" means the study treatment participants take will be chosen by chance (decided at random by a computer). "Open-label" means that the participant, the study doctor, and the Sponsor will know which study treatment each participant is receiving.
Participants will be randomly assigned to one of the following 3 treatment groups:
* Group 1: Treatment with aumolertinib alone, taken orally (by mouth) as a pill once a day. Around 100 participants will be randomly assigned to this group.
* Group 2: Treatment with aumolertinib taken orally as a pill once a day, in combination with chemotherapy given intravenously (IV; through a needle placed in a vein) on the schedule provided by the study doctor. Around 200 participants will be randomly assigned to this group.
* Group 3: Treatment with osimertinib alone, taken orally as a pill once a day. Around 200 participants will be randomly assigned to this group.
Because there will be twice as many participants in Group 2 and Group 3 as in Group 1, the chance of a participant being randomly assigned to either of those groups is twice as likely as being assigned to Group 1.
Participants can continue to receive study treatment as long as they have not withdrawn consent, as long as they choose to continue to receive study treatment and are judged by their doctor to continue to receive clinical benefit from receiving the study treatment, and as long as no other study treatment and/or study discontinuation criteria are met .
开始日期2022-12-14 |
申办/合作机构 |
NCT05199610
An Open-Label, Single-Dose, Parallel-Group Study of the Pharmacokinetics and Safety of EQ143 in Participants With Severe Hepatic Impairment and in Matched Healthy Adults
Participants aged 18 to 75 years with severe hepatic impairment (Child-Pugh class C) who meet the full study eligibility criteria will be enrolled into the study. For each participant with severe hepatic impairment, a corresponding healthy participant will be enrolled who matches with regard to age, sex, and BMI. A single dose of 55-mg EQ143 tablet will be administered in the morning on Day 1, and participants will remain for 5 days (4 nights) in the study center for collection of blood samples and safety monitoring. Participants will attend outpatient follow-up visits on Days 5, 6, 8, and 9 for additional blood sampling and safety assessments. The study will measure and describe the concentrations of EQ143 and its metabolite (HAS-719) in plasma over the course of 9 days (including calculation of PK parameters), the degree of EQ143 and metabolite HAS-719 (and other metabolites, if applicable) binding to proteins in plasma, and the safety of administering a single dose of EQ143 in severely hepatically impaired and matched healthy participants
开始日期2022-03-30 |
申办/合作机构 |
100 项与 EQRx, Inc. 相关的临床结果
登录后查看更多信息
0 项与 EQRx, Inc. 相关的专利(医药)
登录后查看更多信息
5
项与 EQRx, Inc. 相关的文献(医药)2024-02-11·Journal of biomolecular structure & dynamics
Possible cerebroprotective effect of citronellal: molecular docking, MD simulation and
in vivo
investigations
Article
作者: Narala, Venkata Ramireddy ; Somasekhar, G ; D S N B K, Prasanth ; B S, Gowrishankar ; Sampath, A ; Pasala, Praveen Kumar ; Alluril, Ramesh ; Vamshi, G ; Kumar, Pankaj ; Challa, Madhusudhana Chetty ; Dammalli, Manjunath
This study focused on molecular docking, dynamic simulation, and in vivo approaches to examine the molecular interactions between citronellal (CT) and neurotoxic proteins. In silico studies of CT were performed using proteins involved in the pathophysiology of stroke, such as interleukin-6 (IL-6), interleukin-12 (IL-12), TNF-α, and nitric oxide synthase (NOS), to determine the binding affinity based on their interactions. The docking results of CT revealed that, among the targets, NOS had a better binding energy of -6.4 Kcal/mol. NOS showed good hydrophobic interactions: TYR A, 347; VAL A, 352; PRO A, 350; TYR A, 373 amino acids. Interactions with IL-6, TNF-α, and IL-12 resulted in lower binding affinities of -3.7, -3.9 and -3.1 Kcal/mol. Based on molecular dynamics simulations of 100 ns, the binding affinity of CT (-66.782 ± 7.309 kJ/mol) was well complemented, and NOS stability at the docked site was confirmed. In in vivo studies, cerebral stroke was induced by occlusion of the bilateral common carotid arteries for 30 min and reperfusion for 4 h. CT treatment protected the brain by decreasing cerebral infarction size, increasing GSH(p < 0.001***), decreasing MPO (p < 0.001***), MDA (p < 0.001***), NO production (p < 0.01**), and AChE (p < 0.001***) compared to stroke rats. Histopathological examination revealed that CT treatment reduced the severity of cerebral damage. The investigation concluded that CT strongly binds to NOS, as observed in molecular docking and dynamic simulation studies, which are involved in nitric oxide production, leading to cerebral damage, and CT treatment reduces NO production and oxidative stress parameters, and increases antioxidants via inhibition of NOS function.Communicated by Ramaswamy H. Sarma.
2024-02-01·Coronaviruses
Polyherbal Syrup for Coronavirus Infection: Formulation and Evaluation
作者: Kotta, Kranthi Kumar ; Kadiri, Sunil Kumar ; Gouru, Sampath Ayyappa
Background::
SARS-CoV-2 emerged in Wuhan in December 2019, and after that, it
spread quickly around the world. The virus could spread to millions of individuals since there were
no particular treatments or preventative measures. The COVID-19 infection is often treated with
current drugs such as Remdesivir, steroids, tocilizumab, favipiravir, and ivermectin. However, the
immunosuppressive effects of these medicines might worsen COVID-19 symptoms and put the lives
of immunocompromised individuals in peril. Thus, it is important to sustain a robust immune system
when undergoing therapy for COVID-19. Herbal treatment has the potential to accomplish this objective.
Objective::
The current investigation involves the preparation of polyherbal syrup containing various
medicinal plants such as ephedra, diascorea, ginger, echinacea, garlic, rhubarb, and glycyrrhiza for
the effective control of the COVID-19 infection.
Methods::
All varieties of the individual plant powders (200 g) were treated to a 7 day maceration in
aqueous ethanol (70:30) in a percolator at room temperature with intermittent vigorous shaking at
room temperature and storage of the extract in a dark room. The mixture was run through a muslin
cloth and then a Whatman qualitative grade 1 filter paper to produce the filtrate. The filtrate was
evaporated to a thick paste-like consistency at 370 °C under decreased pressure in a rota evaporator
connected to a vacuum pump. After that, each individual extract was collected and kept in airtight
jars at 4°C. According to the Indian Pharmacopoeia, simple syrup (66.67% w/v) of polyherbal extract
was prepared. The oral administration of polyherbal syrup was carried out at varied doses of 0.5
ml, 1 ml, and 1.5 ml to infected golden Syrian hamsters from the 7th day for one week after infection
reached its peak.
Results::
When compared to the infection control group, the results revealed that the viral load was
significantly reduced by 79.1% when treated with polyherbal syrup. A histological examination of
the infected hamster lung on days 7, 10, and 13 demonstrated that polyherbal syrup significantly
decreased viral load in a dose-dependent manner.
Conclusion::
It is inferred that the polyherbal syrup formulation demonstrates efficacy in the prevention
of COVID-19 infection during its first stages and may serve as a potential contender for SARSCoV-
2 due to its immunomodulatory properties.
2023-12-31·Journal of immunotoxicology
Current approaches to evaluate the function of cytotoxic T-cells in non-human primates
Review
作者: Molinier, Brigitte ; Piche, Marie-Soleil ; Rubio, Daniel ; Kamperschroer, Cris ; Frank, Brendon ; Newsome, Courtni ; Weinstock, Daniel ; Lebrec, Hervé ; Collinge, Mark ; Freebern, Wendy ; Genell, Caroline ; Mitchell-Ryan, Shermaine
Cytotoxic T-lymphocytes (CTL) are a subset of T-cells that play a critical role in protecting against intracellular infections and cancer, and have the ability to identify and kill infected or transformed cells expressing non-self peptides associated with major histocompatibility (MHC) Class I molecules. Conversely, aberrant CTL activity can contribute to immune-related pathology under conditions of overwhelming infection or autoimmunity. Disease-modifying therapeutics can have unintended effects on CTL, and a growing number of therapeutics are intended to either suppress or enhance CTL or their functions. The susceptibility of CTL to unintended effects from common therapeutic modalities underscores the need for a better understanding of the impact that such therapies have on CTL function and the associated safety implications. While there are reliable ways of quantifying CTL, notably via flow cytometric analysis of specific CTL markers, it has been a greater challenge to implement fit-for-purpose methods measuring CTL function in the context of safety studies of therapeutics. This review focuses on methods for measuring CTL responses in the context of drug safety and pharmacology testing, with the goals of informing the reader about current approaches, evaluating their pros and cons, and providing perspectives on the utility of these approaches for safety evaluation.
293
项与 EQRx, Inc. 相关的新闻(医药)2025-12-04
·药时空
在生物医药创新生态中,女性创始人正扮演着日益重要的角色。尽管2025年全球风险投资环境从2021年的峰值回落,但女性创始的生物制药公司依然展现出强大的韧性与吸引力。根据PitchBook数据分析,自2008年以来,拥有女性创始的生物制药公司已通过3375笔交易,累计贡献641亿美元的风险投资资金。
12月3日,BioSpace回顾了过去20年中,风险投资(VC)融资规模最大的五家由女性参与的创始生物制药公司,本文将回顾其高光融资时刻,并探讨它们后续的发展轨迹与行业启示。
一、融资格局:从疫情峰值回归理性稳定
2025年,女性创始的生物制药公司融资活动显示出企稳迹象。截至2025年,女性创办的生物制药公司已通过203笔交易获得了48亿美元的资金。这一数字虽远低于2021年127亿美元(412笔交易)的历史峰值,但反映了后疫情时代整个生物制药行业风险投资从狂热回归理性的普遍趋势。
从数据来看,女性创办生物药企的VC融资呈现三大特征:
一是地域集中,美国的波士顿-剑桥地区和旧金山-奥克兰两大生物科技枢纽是绝对的资本聚集地,分别斩获244亿美元(759笔交易)和163亿美元(618 笔交易);
二是阶段均衡,在融资轮次分布上,早期、晚期和天使轮融资基本持平,覆盖企业全生命周期;
三是联合创办为主,女性与男性联合创办的生物药企募资达564亿美元(2866 笔交易),纯女性创办企业募资77亿美元(509笔交易)。
二、五大顶级融资案例:高光时刻与后续征程
BioSpace回顾了自2008年以来排名前五的企业以及这些公司目前的状况,深刻刻画了女性创始人在生物制药领域的影响力与创业历程。
1.EQRx:雄心勃勃的“平价药”梦想与转折
融资情况:2021年1月B轮融资5.7亿美元(历史最高单轮纪录)
创始人:Alexis Borisy、Melanie Nallicheri、Robert Forrester、Susan Hager、Peter Bach 和 Sandra Horning
发展轨迹:作为女性创办生物药企的最大单笔VC融资案例,EQRx在2021年1月完成5.7亿美元B轮融资。公司以“开发既创新又负担得起的药物”的宏伟使命而备受关注,并于2021年8月通过特殊目的收购公司(SPAC)的形式上市,募资18亿美元,累计融资达19.7亿美元。
但临床现实却击碎了美好预期:核心抗体药物sugemalimab临床试验受挫,公司被迫调整管线、放弃低成本目标,员工规模腰斩,最终在2023年8月被Revolution Medicines收购,所有资产终止并退回合作伙伴,曾经的募资巨头以黯然退场告终。
2.Neumora:神经疾病领域的坚守与挑战
融资情况:2021年A轮融资5亿美元
创始人:Paul Berns、Kristina Burow、Robert Nelsen、Mike Poole、Morgan Sheng 和 Carol Suh
发展轨迹:2021 年 ,聚焦神经科学的Neumora完成5亿美元A轮融资,成为当年第四大生物药企 VC 融资案例。公司凭借与安进(Amgen)的合作,专注于神经退行性疾病疗法开发。其累计融资9.87亿美元,包括2023年9月2.5亿美元的IPO。
然而,其发展之路布满荆棘:2024年4月,其精神分裂症资产因临床前安全信号被FDA暂停试验;2025年1月,抗抑郁药物navacaprant三期试验失败,公司被迫推迟研发时间表至 2026年。目前,Neumora正等待阿尔茨海默病候选药NMRA-511的关键数据,有望成为扭转局面的核心。
3.Lyell Immunopharma:攻克细胞疗法难题的持久战
融资情况:2020年3月C轮融资4.93亿美元
创始人:Rick Klausner、Crystal Mackall 和 Stan Riddell
发展轨迹:Lyell致力于通过解决T细胞耗竭和持久性问题,开发下一代CAR-T疗法。2020年3月,公司完成4.93亿美元C轮融资;2021年6月,完成4.25亿美元的IPO。
但细胞疗法赛道竞争激烈,Lyell的发展并非一帆风顺:其与GSK的2.5亿美元合作仅维持数月便终止;2024年,其实体瘤CAR-T疗法LYL797因严重不良反应终止开发。随后公司收购了ImmPACT Bio,获得了双靶点CAR-T候选药物ronde-cel,现已启动2项关键试验。
4.Laronde:短暂闪耀的eRNA梦想与重组
融资情况:2021年B轮融资4.4亿美元
创始人:Avak Kahvejian、Noubar Afeyan、Nicholas Plugis、Erica Weinstein、Sophie Boer
发展轨迹:Laronde背靠Flagship Pioneering(Moderna孵化者),于2021年完成4.4亿美元B轮融资。公司主打Endless RNA(eRNA)平台,号称可编程合成任意蛋白,被视为“下一代mRNA”。
其试图复制Moderna的成功,但2023年6月被曝存在数据完整性问题,临床前数据无法复制,引发信任危机。随后,其砍掉两款核心项目,CEO等核心团队离职,最终在2023年10月被Flagship并入旗下的Senda Biosciences,整合为Sail Biomedicines,原有的eRNA项目虽得以保留,但至今尚未进入临床试验阶段。
5.BioNTech:mRNA技术引领,逆袭成行业巨头
融资情况:2019年1月融资4.25亿美元(非典型轮次)
创始人:Ugur Sahin、Özlem Türeci和Christoph Huber
发展轨迹:BioNTech在2019年1月完成4.25亿美元后期融资,投资方包括辉瑞风投(3.335 亿美元)和赛诺菲(0.915亿美元)。7月,公司进行了总额达到3.25亿美元的B轮融资。这些资金为公司后续研发奠定坚实基础。凭借新冠疫苗积累的资本与技术,BioNTech持续拓展管线,如今已在肿瘤、传染病等领域多点布局,从曾经的融资企业逆袭为行业巨头。
三、启示与展望:募资成功只是起点,持续创新与风险管控是关键
这五大顶级VC融资案例,展现了女性创办生物药企的机遇与挑战,也为行业带来深刻启示。
从成功要素来看,技术创新性与赛道前景是吸引资本的核心:BioNTech的mRNA技术、Laronde的新型RNA平台、Lyell的下一代CAR-T技术,均瞄准了高潜力领域;而EQRx的“平价创新药”愿景、Neumora的脑部疾病布局,也切中了未满足的临床需求。
但生物制药行业的高风险性决定了募资成功并非终点。巨额融资是重要的助推器,但并非成功的绝对保证。科学的严谨性、临床验证以及灵活的战略调整能力同样至关重要。
尽管面临挑战,女性创始人及其公司继续在生物制药领域做出不可忽视的贡献。资本流向的稳定化表明,投资者依然认可由女性领导的企业所带来的创新价值。随着更多女性创业者踏入这一领域,她们将继续推动科学边界,为应对全球健康挑战提供新的解决方案。
参考资料:Top 5 VC Raises by Women-Founded Biopharmas.BioSpace By Annalee Armstrong.December 3, 2025.
识别微信二维码,可添加药时空小编
请注明:姓名+研究方向!
并购
2025-12-03
iStock,
Vanz Studio
Venture capital flow to women-founded companies has stabilized in the post-pandemic environment.
BioSpace
looks back at five companies that have nabbed the most over the past two decades.
Biopharmas with women founders have contributed $64.1 billion in venture capital dollars across 3,375 deals since 2008, according to a
recent analysis by PitchBook
.
2025 has been a particularly good year for female-founded companies across all sectors, with $103.7 billion invested across 2,528 deals so far, according to PitchBook. Zeroing in on biopharma, the capital flow suggests that investment in female-founded companies is stabilizing in the post-pandemic environment. In 2025 so far, female-founded biopharmas have taken in $4.8 billion across 203 deals.
This is a significant drop from the peak in 2021, when $12.7 billion in venture capital was recorded for this category across 412 transactions. Since then, the numbers have declined as the sugar buzz wore off—a trend that is reflected across biopharma, regardless of the gender of the founders.
Much of the cash for women-founded biopharmas has centered in the U.S.’ two key biotech hubs: the Boston-Cambridge area, which saw $24.4 billion in investment across 759 total deals, and San Francisco-Oakland, where 618 deals netted $16.3 billion.
Investment rounds were split equally across early, late and angel rounds. Female-only founded companies took in $7.7 billion in 509 deals, compared to $56.4 billion over 2,866 deals for biopharmas co-founded by women and men.
The largest deal in the 16 years for which PitchBook has data was EQRx, which brought in $570 million in a series B in January 2021. The company, which has since gone out of business, had six founders including Melanie Nallicheri, Susan Hager and Sandra Horning.
Below,
BioSpace
looks back at the top five rounds since 2008 and where the companies are today.
EQRx
Deal Size:
$570 million
Round:
B
Founders:
Alexis Borisy, Melanie Nallicheri, Robert Forrester, Susan Hager, Peter Bach and Sandra Horning
After a massive fundraising push over three years that raised a total of $1.97 billion, the ending for EQRx was not happy.
The company
emerged with a big goal
: to develop medicines that were not just innovative, but affordable. EQRx jumped to the markets quickly through a special purpose acquisition company (SPAC) in August 2021, picking up another $1.8 billion in proceeds.
But the lofty goal quickly met with clinical reality. The biotech’s antibody sugemalimab stumbled in the clinic, leaving executives reeling. EQRx pivoted to two other candidates, then ditched the low-cost goal. The staff was slashed in half, and EQRx later
sold itself to Revolution Medicines
in August 2023, preserving $1 billion in capital for that company. All of EQRx’s assets were terminated and returned to partners.
Neumora
Deal Size:
$500 million
Round:
A
Founders:
Paul Berns, Kristina Burow, Robert Nelsen, Mike Poole, Morgan Sheng and Carol Suh
Believe it or not, a $500 million series A was not enough to earn Neumora the title of largest VC fundraise of 2021. Abogen’s whopping $700 million round nabbed that top slot. But that’s the nature of that year, when investors flocked to the sector buoyed by the hopeful innovation of COVID-19 vaccines that arrived at the end of 2020 to combat the pandemic.
Neumora was the fourth largest VC round of 2021—and that still
made waves in the sector
. The company emerged with the cash and a partnership with Amgen to develop therapies for neurodegenerative disorders. It has now raised a total of $987 million, including a $250 million IPO in September 2023, according to PitchBook data.
The path has not been a straight line for Neumore, however. In April 2024, the FDA
slapped a clinical hold
on the biotech’s schizophrenia asset as preclinical safety signals emerged.
But Neumora plowed on, unfortunately revealing a
Phase III failure
for the kappa opioid receptor (KOR) antagonist navacaprant in major depressive disorder in January this year. With two additional trials expected to readout for the drug this year, Neumora
changed things up
in March and pushed out the timeline to 2026.
After fielding all these challenges, Neumora is
now on the cusp
of releasing key Alzheimer’s disease data for NMRA-511. This could be the moment that $500 million seems worthwhile for investors.
Lyell Immunopharma
Deal Size:
$493 million
Round:
C
Founders:
Rick Klausner, Crystal Mackall and Stan Riddell
Lyell Immunopharma was ahead of the pandemic-influenced biotech funding curve with a massive $493 million series C round in March 2020. Since then, the company has continued to battle in the tough cell therapy space, using its influx of cash from various fundraising mechanisms to bring in new approaches to address the modality’s limitations.
Founded by a team of cell therapy experts, Lyell has promised to develop next generation CAR T cell therapies for blood cancer and solid tumors by addressing T cell exhaustion and durability. Riding the wave of biotechs heading for the public markets in 2021, Lyell pulled off a massive
$425 million IPO
in June. Lyell’s GSK-partnered T cell receptor therapy
hit the clinic
the next year, but the success was short lived as the Big Pharma
walked away
from the $250 million three-year partnership months later.
Continuing on, Lyell reported mixed Phase I data for the CAR T therapy LYL797 in solid tumors in June 2024. The results revealed strong response rates across patients, but a death and high rates of cytokine release syndrome marred the readout. The asset was
discontinued
in October 2024, just as Lyell bought ImmPACT Bio for $30 million in cash plus shares.
The heart of that deal was an autologous dual-targeting CD19/CD20 CAR T, now known as rondecabtagene autoleucel (ronde-cel). Lyell began a pair of pivotal trials for the candidate this year, including a head-to-head test pitting ronde-cel against approved CD19 CAR T cell therapies, including Bristol Myers Squibb’s Breyanzi or Gilead’s Yescarta.
Lyell also followed the biopharma trend and picked up a new CAR T cell candidate from China’s
Innovative Cellular Therapeutics
.
Laronde
Deal Size:
$440 million
Round:
B
Founders:
Avak Kahvejian, Noubar Afeyan, Nicholas Plugis, Erica Weinstein, Sophie Boer
This Flagship Pioneering–backed startup vowed to champion a new form of RNA medicines called Endless RNA upon
launch in 2021
. The company rode the success of Moderna—the star of Flagship’s portfolio—to a $440 million series B months after the public debut in July 2021.
But the journey was short lived. In June 2023,
STAT
published an expose on
data integrity issues
at the biotech. The company could not replicate the preclinical data that had underpinned the massive raise. Laronde cut two programs and many employees were forced to resign, including CEO Pablo Cagnoni.
Flagship folded the embattled biotech into another of its portfolio companies, Senda Biosciences, to form
Sail Biomedicines
in October 2023. That biotech is continuing the eRNA mission but has yet to enter the clinic.
BioNTech
Deal Size:
$425 million
Round:
N/A
Founders:
Ugur Sahin, Özlem Türeci and Christoph Huber
BioNTech’s story has been told over and over—the Pfizer-partnered pandemic savior developed one of the two COVID-19 vaccines that helped bring the world back from the crisis. This generated billions in revenue and has helped fuel the biotech’s next phase.
But step back to January 2019, when the German mRNA company raised a remarkable $425 million, and you’ll see that BioNTech always had big ambitions. This later-stage round involved just two pharma entities: Pfizer Ventures with $333.5 million in cash and Sanofi with $91.5 million, according to Pitchbook data.
The company followed that year with a more traditional series B in July that totaled
$325 million
. These fundraises primed the biotech to enter the first year of the pandemic fully charged and ready for some R&D.
.responsive-container {
display: flex;
flex-wrap: wrap;
border: 1px solid #ededed;
font-family: Helvetica, Arial, Sans-Serif;
padding: 20px 20px 10px 20px;
}
.column-left {
flex: 1;
max-width: 45%;
padding: 20px 20px 10px 20px;
}
.column-right {
flex: 2;
padding: 20px 20px 10px 20px;
}
@media (max-width: 768px) {
.column-left,
.column-right {
max-width: 100%;
flex: 100%;
padding: 10px 0;
}
}
Subscribe to BioPharm Executive!
Market insights, trending business and policy stories for biopharma leaders
hbspt.forms.create({
region: "na1",
portalId: "4413123",
formId: "7c139b3c-ff0b-44e0-bffe-f449801dca59",
onFormSubmitted: function($form, data) {
window.dataLayer = window.dataLayer || [];
window.dataLayer.push({
'event': 'GTMevent',
'event_name': 'newsletter_sign_up'
});
}
});
疫苗临床1期并购IPO临床结果
2025-12-01
Plus news about ALS Investment Fund, Q32 Bio, Akebia Therapeutics, Lynk Pharmaceuticals, Hemay Pharmaceutical and Valneva:
🤝 Angelini Ventures teams with European Investment Bank:
The Rome-based biotech investor and the EIB will each commit €75 million to seven to 10 startups over the next six years. Angelini is a CVC of the conglomerate Angelini Industries, which spans pharmaceuticals, consumer goods and industrial tech. The CVC launched in 2022 with €300 million in planned investments, which includes the €75 million announced Monday, an Angelini spokesperson confirmed. The investor has already doled out about €125 million into 22 startups, such as Chicago autoimmune biotech
Cour
, French ADC developer
Adcytherix
and Swiss and German radiopharma
Nuclidium
.
— Kyle LaHucik
💵 New radiopharma startup debuts with $40M:
The
seed financing
for the New Jersey biotech comes from NovaCapital, high net-worth individuals and Club Degli Investitori. Its parent company is Juniper Radiopharma. The startup didn’t disclose its pipeline.
— Kyle LaHucik
💰 More ALS funding:
Amsterdam-based ALS Investment Fund raised about $70 million for its third fund. The money comes from family offices, high net worth individuals in the US and Europe and some ALS nonprofit foundations, ALS-IF
said
in a blog post on Monday. The group aims to support up to seven startups at the Series A and B stages. The third fund has already backed Bloom Science,
QurAlis
,
VectorY
and ProJenX.
— Kyle LaHucik
📦 Q32 Bio sells complement inhibitor to Akebia:
Q32 Bio
receives
$12 million upfront for the program, called ADX-097. If everything pans out, Q32 can get another $580 million in milestone payments. Akebia said it
plans
to test ADX-097 in rare kidney diseases. —
Max Gelman
🇨🇳 Two more Chinese biotechs eye HKEX listing:
Lynk Pharmaceuticals
and
Hemay Pharmaceutical
have both filed for IPOs on the popular bourse. Hemay had tried earlier this year, but let its filing lapse after a six-month window of no activity. Lilly Asia Ventures-backed
Lynk
has multiple JAK inhibitors across all phases of clinical development and a handful of preclinical protein degraders and other I&I drug candidates. Lynk previously licensed a
JAK1 inhibitor to EQRx
, the US biotech that tried to upend the US drug price system with cheaper treatments from abroad.
— Kyle LaHucik
🇫🇷 Valneva downsizes French offices:
The company
said
it would close a site in Nantes, a city in the northwest of France. The move would allow it to “concentrate” French operations in Lyon, while “centralizing” R&D efforts in Vienna, Austria. The announcement came the same day as Valneva announced new
Phase 2 data
for its experimental Lyme disease vaccine. —
Max Gelman
疫苗临床2期IPO
100 项与 EQRx, Inc. 相关的药物交易
登录后查看更多信息
100 项与 EQRx, Inc. 相关的转化医学
登录后查看更多信息
组织架构
使用我们的机构树数据加速您的研究。
登录
或

管线布局
2026年06月08日管线快照
管线布局中药物为当前组织机构及其子机构作为药物机构进行统计,早期临床1期并入临床1期,临床1/2期并入临床2期,临床2/3期并入临床3期
临床前
1
1
临床2期
申请上市
1
4
其他
登录后查看更多信息
当前项目
| 药物(靶点) | 适应症 | 全球最高研发状态 |
|---|---|---|
甲磺酸阿美替尼 ( EGFR L858R x EGFR T790M x EGFR-Ex19del ) | 非小细胞肺癌 更多 | 申请上市 |
EQ-121 ( JAK1 ) | 类风湿关节炎 更多 | 临床2期 |
PARP1 inhibitor (EQRx) ( PARP1 ) | 肿瘤 更多 | 临床前 |
盐酸来罗西利 ( CDK4 x CDK6 ) | 晚期乳腺癌 更多 | 终止 |
舒格利单抗 ( PDL1 ) | 非小细胞肺癌 更多 | 终止 |
登录后查看更多信息
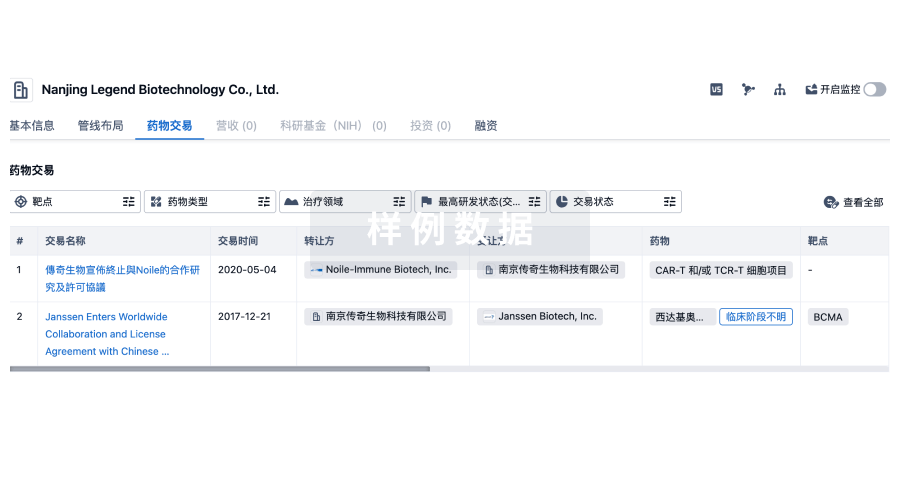
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
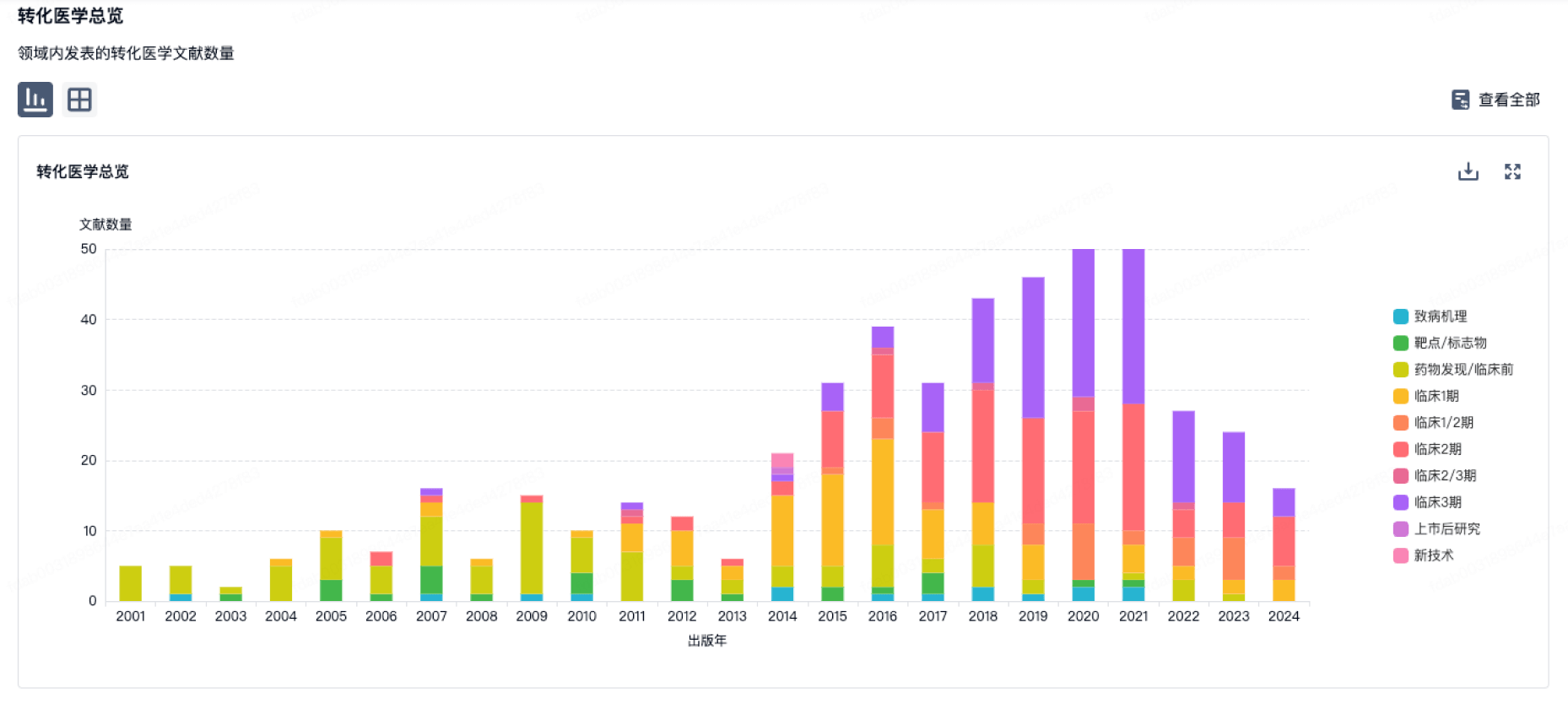
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
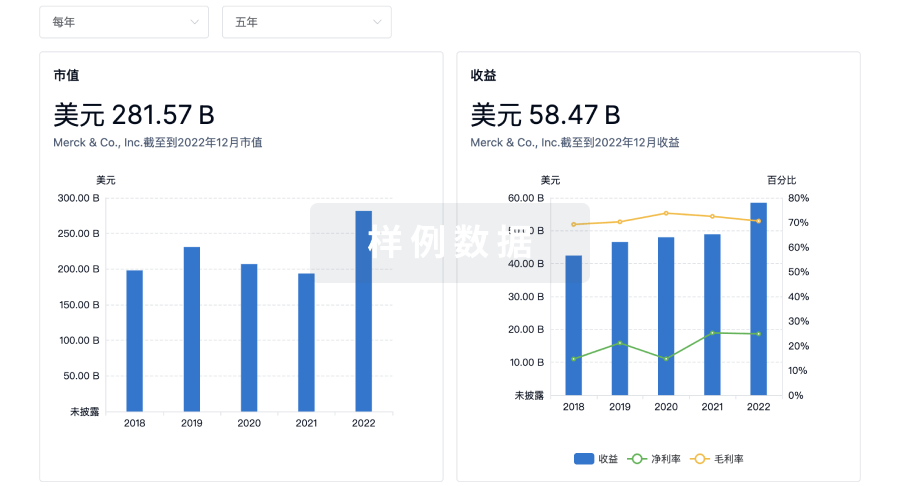
营收
使用 Synapse 探索超过 36 万个组织的财务状况。
登录
或
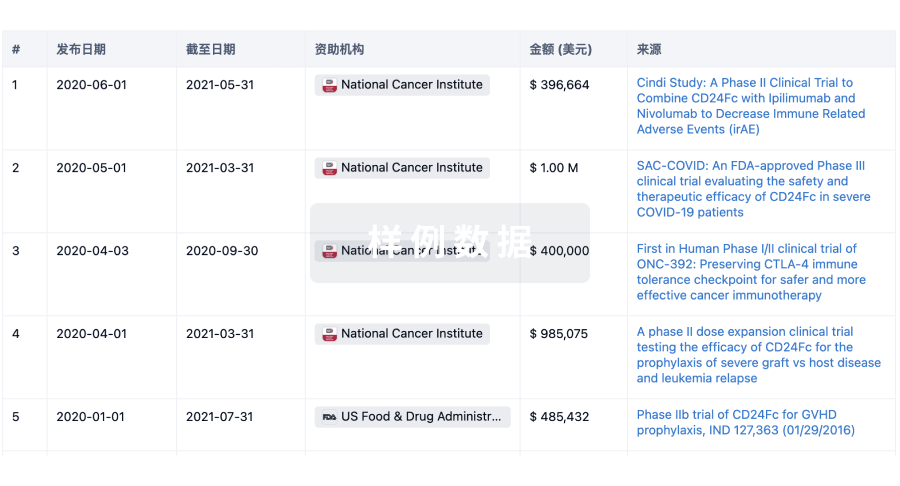
科研基金(NIH)
访问超过 200 万项资助和基金信息,以提升您的研究之旅。
登录
或
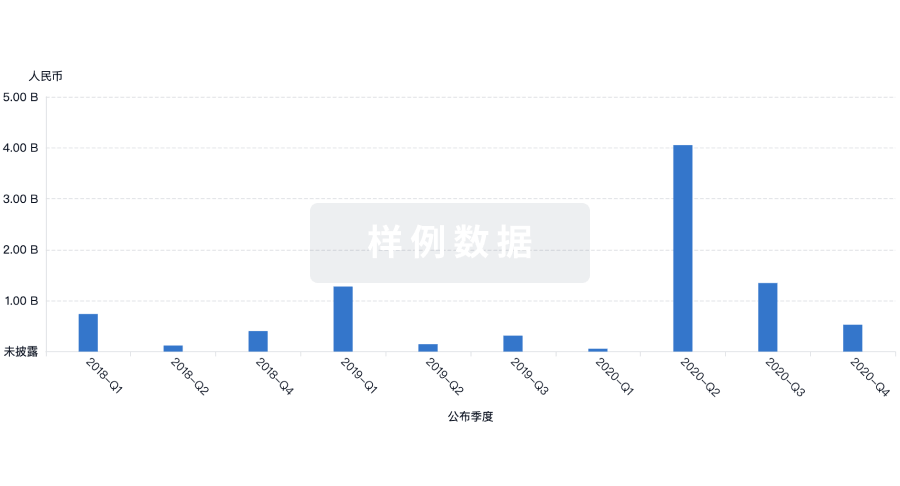
投资
深入了解从初创企业到成熟企业的最新公司投资动态。
登录
或
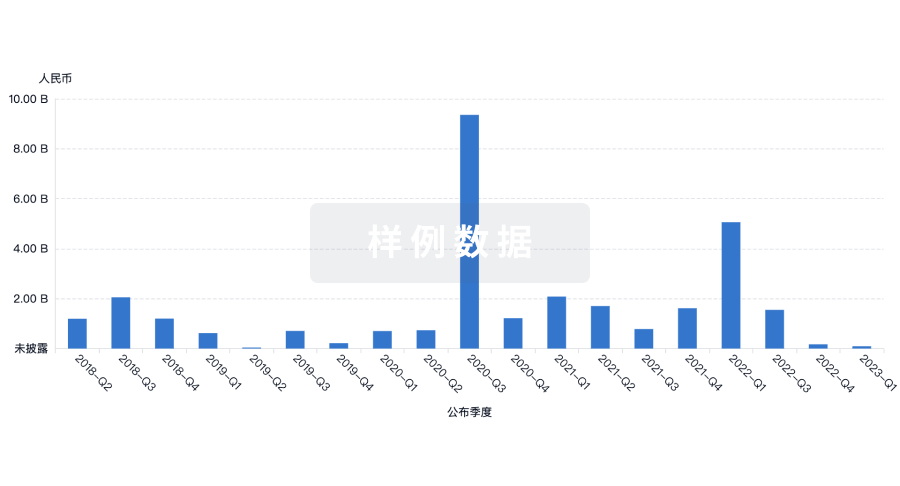
融资
发掘融资趋势以验证和推进您的投资机会。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用

