预约演示
更新于:2026-06-07
Chlorhexidine gluconate
葡萄糖氯己定
更新于:2026-06-07
概要
基本信息
权益机构- |
最高研发阶段批准上市 |
首次获批日期 日本 (1959-09-22), |
最高研发阶段(中国)批准上市 |
特殊审评孤儿药 (美国) |
登录后查看时间轴
结构/序列
分子式C34H54Cl2N10O14 |
InChIKeyYZIYKJHYYHPJIB-UUPCJSQJSA-N |
CAS号18472-51-0 |
关联
762
项与 葡萄糖氯己定 相关的临床试验NCT07609797
The Effects of Sodium Fluoride and Chlorhexidine Use on Salivary IL-6 and Matrix Metalloproteinase Levels in Children With Active Caries
This study aims to compare salivary IL-6, MMP-8, MMP-9, and TIMP-1 levels between healthy children and caries-active children, and to evaluate the effects of 5% sodium fluoride (NaF) varnish and 2% chlorhexidine (CHX) used in caries prevention on these biomarkers.
The study will be conducted at Alanya Alaaddin Keykubat University, Faculty of Dentistry, Department of Pediatric Dentistry. Informed consent will be obtained from children and their parents/guardians. Investigator calibration will be performed using Cohen's kappa method prior to data collection. Sample size was calculated assuming 80% power (1-β = 0.80), α = 0.05, and Cohen's d ≈ 0.8, resulting in 20 participants per group using G*Power 3.1 software.
Study groups: Group A: 5% NaF varnish. Group B: 2% CHX + 5% NaF varnish. Group C: Standard oral hygiene education (negative control). Group D: Caries-free children (biological reference; baseline saliva sampling only).
Saliva samples will be collected at T0 (baseline), T1 (30 minutes post-application), and T2 (1 month). Unstimulated whole saliva will be collected, centrifuged at 5,000 g for 10 minutes at 4°C, and stored at -80°C. IL-6, MMP-8, MMP-9, and TIMP-1 levels will be measured using CE-marked/FDA-approved human saliva ELISA kits.
The study will be conducted at Alanya Alaaddin Keykubat University, Faculty of Dentistry, Department of Pediatric Dentistry. Informed consent will be obtained from children and their parents/guardians. Investigator calibration will be performed using Cohen's kappa method prior to data collection. Sample size was calculated assuming 80% power (1-β = 0.80), α = 0.05, and Cohen's d ≈ 0.8, resulting in 20 participants per group using G*Power 3.1 software.
Study groups: Group A: 5% NaF varnish. Group B: 2% CHX + 5% NaF varnish. Group C: Standard oral hygiene education (negative control). Group D: Caries-free children (biological reference; baseline saliva sampling only).
Saliva samples will be collected at T0 (baseline), T1 (30 minutes post-application), and T2 (1 month). Unstimulated whole saliva will be collected, centrifuged at 5,000 g for 10 minutes at 4°C, and stored at -80°C. IL-6, MMP-8, MMP-9, and TIMP-1 levels will be measured using CE-marked/FDA-approved human saliva ELISA kits.
开始日期2026-05-15 |
申办/合作机构 |
NCT07611123
Effect of a Bioactive Mineral-Ionic Mouthrinse on Periodontal Soft Tissue Healing and Postoperative Pain After Tooth Extraction: A Double-Blind Randomized Clinical Trial
This randomized, double-blinded clinical trial was designed to evaluate the effects of a bioactive mineral-ionic mouthrinse (THERAVEX® Total Oral Care Plus) on postoperative healing and patient comfort following simple tooth extraction. Tooth extraction is one of the most common dental procedures and is frequently associated with postoperative pain, inflammation, and delayed soft tissue healing. Conventional mouthrinses such as chlorhexidine are widely used for their antimicrobial properties; however, alternative approaches aimed at supporting the physiological healing process are increasingly being investigated.
A total of 94 systemically healthy patients requiring simple tooth extraction were enrolled and randomly allocated into three parallel groups receiving either a bioactive mineral-ionic mouthrinse, chlorhexidine 0.12%, or normal saline as postoperative oral rinses. Participants and investigators were blinded to group allocation throughout the study period.
The primary objective of the study was to assess early soft tissue healing of the extraction socket using standardized clinical measurements of buccolingual (BL) and mesiodistal (MD) socket dimensions at different postoperative time points. Secondary objectives included the evaluation of postoperative pain using a visual analog scale (VAS), as well as clinical assessment of tissue response during the healing period.
The study aims to investigate whether a bioactive mineral-ionic oral rinse may serve as a supportive postoperative strategy for enhancing early wound healing and improving patient-reported comfort after dental extraction procedures
A total of 94 systemically healthy patients requiring simple tooth extraction were enrolled and randomly allocated into three parallel groups receiving either a bioactive mineral-ionic mouthrinse, chlorhexidine 0.12%, or normal saline as postoperative oral rinses. Participants and investigators were blinded to group allocation throughout the study period.
The primary objective of the study was to assess early soft tissue healing of the extraction socket using standardized clinical measurements of buccolingual (BL) and mesiodistal (MD) socket dimensions at different postoperative time points. Secondary objectives included the evaluation of postoperative pain using a visual analog scale (VAS), as well as clinical assessment of tissue response during the healing period.
The study aims to investigate whether a bioactive mineral-ionic oral rinse may serve as a supportive postoperative strategy for enhancing early wound healing and improving patient-reported comfort after dental extraction procedures
开始日期2026-04-28 |
申办/合作机构 |
NCT07453069
A Randomized, Double-blind, Three Arm, Multi-center Phase 2 Study to Investigate the Molecular Efficacy and Safety of FB301/Chlorhexidine Compared With FB301/Sham and Placebo/Sham in a Mock FET Cycle in Female Participants 18-40 Years of Age With Asymptomatic Vaginal Molecular Dysbiosis Planning to Undergo a Frozen Embryo Transfer (FET) Cycle
The goal of this clinical trial is to evaluate FB301 during a mock frozen embryo transfer (FET) cycle in pre-menopausal women aged 18 to 40 years with a prior failed FET and a defined vaginal bacterial imbalance (dysbiosis).
The main question it aims to answer is:
• Does treatment with FB301 during a mock FET cycle change the proportion of participants who meet the predefined vaginal bacterial threshold compared with placebo?
Researchers will compare:
* FB301 given after an initial vaginal cleansing with chlorhexidine (an antiseptic solution),
* FB301 given after an initial vaginal cleansing with saline (saltwater), and
* A placebo capsule given after an initial vaginal cleansing with saline to determine whether these approaches affect vaginal bacterial composition and pregnancy outcomes.
Participants will take study treatment for 15 days during a "mock" FET cycle. In a mock cycle, participants receive the hormones needed to prepare the uterus for embryo transfer, but no embryo is transferred. After completing the mock cycle, participants will proceed with their planned frozen embryo transfer and will be followed during pregnancy until birth.
Participants will:
* Undergo a vaginal cleansing before receiving the first dose of FB301 or placebo
* Provide vaginal swab samples at up to 5 study visits
* Attend the study centre for up to 8 visits and participate in up to 4 follow-up phone calls
* Complete a mock FET cycle before proceeding with their planned frozen embryo transfer cycle
Participants who become pregnant will be followed until birth.
The main question it aims to answer is:
• Does treatment with FB301 during a mock FET cycle change the proportion of participants who meet the predefined vaginal bacterial threshold compared with placebo?
Researchers will compare:
* FB301 given after an initial vaginal cleansing with chlorhexidine (an antiseptic solution),
* FB301 given after an initial vaginal cleansing with saline (saltwater), and
* A placebo capsule given after an initial vaginal cleansing with saline to determine whether these approaches affect vaginal bacterial composition and pregnancy outcomes.
Participants will take study treatment for 15 days during a "mock" FET cycle. In a mock cycle, participants receive the hormones needed to prepare the uterus for embryo transfer, but no embryo is transferred. After completing the mock cycle, participants will proceed with their planned frozen embryo transfer and will be followed during pregnancy until birth.
Participants will:
* Undergo a vaginal cleansing before receiving the first dose of FB301 or placebo
* Provide vaginal swab samples at up to 5 study visits
* Attend the study centre for up to 8 visits and participate in up to 4 follow-up phone calls
* Complete a mock FET cycle before proceeding with their planned frozen embryo transfer cycle
Participants who become pregnant will be followed until birth.
开始日期2026-04-15 |
申办/合作机构 |
100 项与 葡萄糖氯己定 相关的临床结果
登录后查看更多信息
100 项与 葡萄糖氯己定 相关的转化医学
登录后查看更多信息
100 项与 葡萄糖氯己定 相关的专利(医药)
登录后查看更多信息
6,253
项与 葡萄糖氯己定 相关的文献(医药)2026-10-01·Intensive and Critical Care Nursing
Effectiveness of chlorhexidine gluconate–impregnated dressings in preventing central line–associated bloodstream infection in a paediatric intensive care unit: A randomised controlled trial
Article
作者: Portero-Prados, Francisco Javier ; Pabón-Carrasco, Manuel ; Ponce-Blandón, José Antonio
OBJECTIVES:
To compare the effectiveness and dermatological safety of chlorhexidine gluconate (CHG)-impregnated dressings versus conventional transparent dressings in preventing central line-associated bloodstream infection (CLABSI) in paediatric patients admitted to a PICU.
METHODS:
A single-blind, randomised controlled trial with a 1:1 allocation ratio was conducted in a tertiary PICU. A total of 250 paediatric patients with a central venous catheter were included (125 per group). Patient characteristics, catheter-related variables, catheter dwell time and skin alterations were recorded. The primary outcome was CLABSI, defined according to CDC/NHSN criteria. Bivariate analyses and multivariable logistic regression were performed, including clinically relevant covariates related to catheter exposure, dressing type, and vaccination status. The trial was registered at ClinicalTrials.gov (NCT07175116).
RESULTS:
CLABSI incidence was significantly lower in the CHG group compared with the conventional dressing group (2.4% vs. 18.4%; p < 0.001). In multivariable analysis, CHG-impregnated dressings were independently associated with reduced CLABSI risk (OR = 0.15; 95% CI: 0.04-0.58). Longer catheter dwell time (OR = 1.13 per day; 95% CI: 1.04-1.22) and absence of complete vaccination (OR = 8.68; 95% CI: 2.48-30.47) were also associated with increased infection risk. Incomplete vaccination showed a similar trend without reaching statistical significance (OR = 6.48; 95% CI: 0.95-44.20). Skin alterations were more frequent in the CHG group (16.8% vs. 11.2%), predominantly in younger infants.
CONCLUSIONS:
CHG-impregnated dressings were associated with a significant reduction in CLABSI incidence in critically ill paediatric patients, although their use was linked to a modest increase in mild skin reactions.
IMPLICATIONS FOR CLINICAL PRACTICE:
CHG-impregnated dressings may be considered as part of a multifaceted infection prevention strategy, alongside appropriate catheter management, minimisation of catheter manipulation and proactive skin monitoring, with cautious and individualised use in infants.
2026-08-01·JOURNAL OF SURGICAL RESEARCH
Intra-Abdominal 0.05% Chlorhexidine Gluconate Lavage in Perforated Appendicitis
Article
作者: Keesari, Rohali ; Hwang, Rosa ; Dao, Duy T ; Kozlowski, Gabrielle ; Mudreac, Andrew ; Mattei, Peter
INTRODUCTION:
In August 2021, pediatric surgeons at our institution began using 0.05% chlorhexidine gluconate (CHG) solution in sterile water for intraoperative lavage during laparoscopic appendectomies. The goal of this study is to determine the efficacy of intraoperative lavage with 0.05% CHG in preventing surgical site infection (SSI) after appendectomy for pediatric perforated appendicitis.
METHODS:
The Electronic Medical Record was queried to identify patients aged <18 y who underwent laparoscopic appendectomy for perforated appendicitis between January 2018 and February 2025 at our institution. Demographics, preoperative laboratory values, and postoperative complications were compared between patients who did and did not receive 0.05% CHG lavage. Postoperative outcomes, including the rates of deep/organ-space SSI requiring a drainage procedure, inpatient readmission, return to operating room, and emergency department revisits, were compared between treatment and control groups with Firth logistic regression and inverse probability of treatment weighting.
RESULTS:
A total of 858 cases of laparoscopic appendectomy for perforated appendicitis were identified; 0.05% CHG lavage was used in 197 (23.0%). Postoperative drainage rate with and without 0.05% CHG lavage was 5.1% and 8.5%, respectively. Using Firth logistic regression and after adjustment for demographic variables and preoperative laboratory values, intraoperative 0.05% CHG lavage did not significantly impact the rate of deep/organ-space SSI requiring drainage procedure (adjusted odds ratio [OR]: 0.58, 95% confidence interval [CI: 0.29, 1.14]), inpatient readmission (OR: 1.40, 95% CI [0.77, 2.56]), return to the operating room (OR: 1.14, 95% CI [0.40, 3.29]), or emergency department revisit (OR: 1.19, 95% CI [0.71, 1.97]). Sensitivity analysis using inverse probability of treatment weighting was consistent with the primary Firth logistic regression analyses.
CONCLUSIONS:
A 0.05% CHG lavage during laparoscopic appendectomy for perforated appendicitis was associated with a low rate of deep/organ-space SSI requiring drainage (5%). However, it does not significantly alter postoperative outcomes. Prospective studies are needed to evaluate whether this solution lowers infectious complications.
2026-06-01·Infection prevention in practice
Effect of bathing with 2% chlorhexidine gluconate every other day on healthcare-associated infections in the medical intensive care unit
Article
作者: Yang, Hsing-Yu ; Yu, Pei-Jung ; Hsu, Shu-Fen ; Wu, Te-Yu
Background:
Healthcare-associated infections (HAIs) cause morbidity and mortality in patients at medical intensive care units (MICUs). However, current literature reports inconsistent findings on the effect of daily bathing with 2% chlorhexidine gluconate (CHG) on reducing HAIs and that the solution can cause skin harm. This study aimed to explore the effect of bathing with 2% CHG every 2 days on HAIs in the MICU.
Methods:
This study used a quasi-experimental design (experimental group) and a medical record review (control group). Patients in the control group were admitted to the MICU at a medical centre in Taiwan from March 2018 to February 2019 and used general soap for bathing every other day as part of the unit's routine. The experimental group was recruited from March 2019 to February 2020 and used 2% CHG wet wipes for bathing every other day. The study outcome was to compare the effects on HAIs, catheter-associated urinary tract infections (CAUTIs), central line-associated bloodstream infections (CLABSIs), and ventilator-associated pneumonia (VAP) between these two groups.
Results:
A total of 731 patients in the MICU participated in the study over 12 months. HAIs were significantly different between the experimental (5.9‰) and control (8.9‰) groups, and CAUTIs were also considerably different between the experimental (1.1‰) and control (5.2‰) groups. In contrast, CLABSIs and VAP did not show differences between these two groups.
Conclusions:
Bathing with 2% CHG every 2 days for 12 months was associated with reduced HAIs and CAUTIs in the MICU. However, strict aseptic procedures still should be followed during routine care.
23
项与 葡萄糖氯己定 相关的新闻(医药)2026-05-25
Drinking nitrate-rich beetroot juice may do more than support heart health — it could actually reshape the bacteria living in the mouth in ways that help lower blood pressure in older adults. In the largest study of its kind, researchers found that older people who drank concentrated beetroot juice twice daily for two weeks experienced noticeable blood pressure reductions, while younger adults did not.A simple beetroot juice routine may help explain one of the more surprising links in healthy aging: the connection between bacteria in the mouth and blood pressure.
Research from the University of Exeter found that older adults who drank nitrate rich beetroot juice twice a day for two weeks saw their blood pressure fall. The same effect did not appear in younger adults, even though beetroot juice also changed their oral microbiome.
The study, published in Free Radical Biology and Medicine, is the largest of its kind to examine how dietary nitrate affects the mouth bacteria, nitric oxide biology, and blood vessel responses of younger and older adults.
Why the Mouth Matters
Nitrate is found naturally in many vegetables and plays an important role in the body. Beetroot is especially rich in nitrate, but it is not the only option. Spinach, arugula, fennel, celery, and kale are also good dietary sources.
The key step happens before nitrate reaches the bloodstream. Certain bacteria in the mouth help convert nitrate from food into compounds that eventually support the production of nitric oxide. Nitric oxide helps blood vessels relax and function properly, which is important for healthy blood pressure regulation.
When the balance of oral bacteria shifts in the wrong direction, that nitrate to nitric oxide pathway may become less efficient. The Exeter team found evidence that beetroot juice changed the oral microbiome in older adults in a way that appeared to support this pathway.
A Two Week Beetroot Juice Test
The trial included 39 adults under age 30 and 36 adults in their 60s and 70s, recruited through the NIHR Exeter Clinical Research Facility. It was supported by the Exeter Clinical Trials Unit and funded through a BBSRC Industrial Partnership Award.
Participants completed two separate two week phases. In one phase, they drank regular doses of nitrate rich beetroot juice. In the other, they drank a placebo version of the juice with the nitrate removed. A two week "wash out" period separated the phases so the researchers could reset the conditions before testing the next drink.
The team then used bacterial gene sequencing to study which microbes were present in the mouth before and after each condition.
Older Adults Responded Differently
Both age groups showed significant changes in the oral microbiome after drinking nitrate rich beetroot juice. However, the changes were not the same in younger and older participants.
Among older adults, beetroot juice was linked to a notable drop in Prevotella, a group of mouth bacteria that the researchers described as potentially harmful in this context. At the same time, bacteria associated with health benefits, including Neisseria, became more abundant.
The older group also began the study with higher average blood pressure than the younger group. After the nitrate rich beetroot juice phase, their blood pressure fell. That reduction was not seen after the placebo drink, and it was not observed in the younger adults.
The Nitric Oxide Connection
The results point to a possible reason beetroot juice may be especially useful later in life. Older adults tend to produce less nitric oxide as they age, and reduced nitric oxide availability can affect blood vessel function.
Study author Professor Anni Vanhatalo, of the University of Exeter, said: "We know that a nitrate-rich diet has health benefits, and older people produce less of their own nitric oxide as they age. They also tend to have higher blood pressure, which can be linked to cardiovascular complications like heart attack and stroke. Encouraging older adults to consume more nitrate-rich vegetables could have significant long term health benefits. The good news is that if you don't like beetroot, there are many nitrate-rich alternatives like spinach, rocket, fennel, celery and kale."
The findings suggest that beetroot juice may not act only through the nutrients it delivers. It may also work by changing the tiny ecosystem in the mouth that helps unlock those nutrients.
Related Research Adds to the Picture
Follow up work and related studies have continued to strengthen the idea that oral bacteria are central to how nitrate affects the body.
A 2025 randomized, double blind, placebo controlled crossover study of 15 older adults with treated high blood pressure found that four weeks of nitrate rich beetroot juice selectively changed the oral microbiome, increasing Neisseria and decreasing Veillonella, while the intestinal microbiome did not significantly change. The same research program reported that nitrate intake affected nitrate metabolism but did not produce sustained improvements in blood pressure or vascular function in that treated hypertension group, showing that the response may depend on health status, medications, study design, and the bacteria present at baseline.
A 2026 pilot study also highlighted the importance of the mouth in nitrate biology. It found that chlorhexidine, an antiseptic mouthwash, disrupted nitrate processing and reduced gastric nitric oxide synthesis, while dietary nitrate supplementation partly preserved microbial function and nitric oxide related signaling during antiseptic use.
Other work has raised similar questions about antibacterial mouth rinses. A 2025 Scientific Reports study in rats found that a nitrate and antioxidant mouth rinse supported nitrate and nitrite reducing oral bacteria and was associated with lower blood pressure compared with chlorhexidine treatment. Because that study was conducted in animals, the findings cannot be directly applied to people, but they add to the broader evidence that oral bacteria can influence the nitrate pathway.
A Potential Nutrition Strategy for Healthy Aging
Co-author Professor Andy Jones, of the University of Exeter, said: "This study shows that nitrate-rich foods alter the oral microbiome in a way that could result in less inflammation, as well as a lowering of blood pressure in older people. This paves the way for larger studies to explore the influence of lifestyle factors and biological sex in how people respond to dietary nitrate supplementation."
The findings do not mean beetroot juice is a replacement for medication or other proven ways to manage blood pressure. However, they do suggest that nitrate rich vegetables could be a practical addition to a heart healthy lifestyle, particularly for older adults.
They also point to a more personalized future for nutrition. Two people can eat the same nitrate rich foods but respond differently, partly because their oral microbiomes may not process nitrate in the same way.
What Comes Next
The Exeter researchers say larger studies are needed to understand why some people respond more strongly than others. Future research may help reveal how lifestyle, sex, age, oral hygiene habits, and baseline microbiome differences shape the effects of dietary nitrate.
Dr. Lee Beniston FRSB, Associate Director for Industry Partnerships and Collaborative Research and Development at BBSRC, said:
"This research is a great example of how bioscience can help us better understand the complex links between diet, the microbiome and healthy aging. By uncovering how dietary nitrate affects oral bacteria and blood pressure in older adults, the study opens up new opportunities for improving vascular health through nutrition. BBSRC is proud to have supported this innovative partnership between academic researchers and industry to advance knowledge with real-world benefits."
Together, the evidence points to a striking idea: one path to healthier blood vessels may begin not in the heart, but in the mouth.
临床结果
2026-05-11
In the rapidly evolving healthcare and diagnostic industry, choosing a reliable medical consumables manufacturer is essential for ensuring product quality, testing accuracy, and patient safety. Hospitals, laboratories, diagnostic companies, and distributors worldwide are seeking trusted suppliers that offer high-quality products, stable production capacity, and flexible OEM/ODM services.
As a professional Chinese manufacturer of medical consumables, MEIDIKE GENE provides comprehensive specimen collection and laboratory consumable solutions for global customers.
MEIDIKE GENE, a brand of Medico Technology Co., Ltd., specializes in the research, development, and manufacturing of medical consumables and diagnostic sampling products. With years of industry experience, advanced production facilities, and strict quality management systems, the company supplies reliable products to customers in healthcare, diagnostics, biotechnology, pharmaceutical, and laboratory industries worldwide.
The company supports both OEM and ODM customization services, helping distributors, brands, laboratories, and medical institutions develop customized products and private-label solutions.
MEIDIKE GENE manufactures a wide range of specimen collection swabs designed for clinical diagnostics, microbiological testing, genetic testing, and laboratory sampling.
Main products include:
Flocked Swabs Foam Swabs Rayon Swabs Cotton Swabs Polyester Swabs
These swabs are widely used for:
Nasopharyngeal sampling Oropharyngeal sampling Cervical specimen collection DNA sample collection Environmental sampling Laboratory testing
To meet the growing demand for diagnostic testing and home sample collection, MEIDIKE GENE offers various specimen collection kits for different applications.
Virus Transport Medium (VTM) kits are designed for safe collection, transportation, and preservation of virus specimens.
Applications include:
Respiratory virus testing Influenza testing COVID-19 testing Molecular diagnostics
DNA collection kits provide convenient and non-invasive sample collection for genetic testing, forensic testing, and research applications.
HPV collection kits are specially designed for cervical screening and HPV testing. The kits can include cervical sampling brushes, collection tubes, and preservation solutions.
Saliva collection kits are suitable for:
Genetic testing DNA analysis Drug testing Research applications
Stool specimen collection kits are commonly used for microbiome research, gastrointestinal disease testing, and laboratory analysis.
Urine collection kits provide hygienic and secure sample collection for diagnostic and laboratory testing.
MEIDIKE GENE also manufactures infection prevention and skin preparation products, including:
Chlorhexidine Applicators Antiseptic Swabs Alcohol Wipes
These products are widely used in hospitals, clinics, surgical centers, and home healthcare environments for skin disinfection and infection control.
The cervical cytology brush is designed for gynecological sampling and cervical cell collection. The ergonomic design helps improve patient comfort and sample collection efficiency, making it suitable for cervical cancer screening and HPV testing.
MEIDIKE GENE provides high-quality Vacuum Blood Collection Tubes for clinical blood collection and laboratory analysis.
Available tube types include:
Serum Tubes EDTA Tubes Heparin Tubes Gel & Clot Activator Tubes Glucose Tubes
The tubes are manufactured under strict quality standards to ensure accurate and reliable laboratory results.
The company also offers various sample storage and transport solutions, including:
Sample Storage Tubes Flip-Top Desiccant Vial Plastic Cryo Tube Urine Specimen Collection Cup Stool Collection Cup
These products help ensure specimen integrity during transportation and storage.
As an experienced medical consumables manufacturer from China, MEIDIKE GENE operates advanced production facilities and cleanroom manufacturing environments to ensure product consistency and quality.
MEIDIKE GENE supports customized manufacturing solutions, including:
Private Label Packaging Customized Product Design Customized Packaging Brand Logo Printing Custom Sampling Kits
This makes the company an ideal partner for distributors, wholesalers, diagnostic brands, and healthcare companies.
MEIDIKE GENE products are manufactured under strict international quality standards and have obtained certifications including:
CE Certification FDA Certification ISO13485 Certification TGA Certification MDEL Certification
MEIDIKE GENE products are exported to many countries and regions worldwide, serving hospitals, laboratories, diagnostic centers, research institutions, and medical distributors.
If you are looking for a trusted medical consumables manufacturer with strong production capabilities, reliable quality, and professional OEM/ODM support, MEIDIKE GENE is your ideal partner.
Visit the official website to learn more about products and customization services: www.medicoswab.com
诊断试剂
2026-05-04
New BPEI preclinical data address treatment protocol, corneal biochemical environment, fungal resistance mechanism, MRSA biofilm inhibition, and enhanced cysticidal activity
KNOXVILLE, Tenn., May 04, 2026
(GLOBE NEWSWIRE)
-- Provectus Biopharmaceuticals, Inc. (“Provectus” or the “Company”) (OTCQB: PVCT), a clinical-stage biopharmaceutical company developing proprietary synthetic small molecule rose bengal sodium (“RBS”)-based medicines, notes that researchers from
Bascom Palmer Eye Institute
(“BPEI”) at the University of Miami will present four posters on rose bengal photodynamic antimicrobial therapy (“RB-PDAT”) at the
2026 Annual Meeting of the Association for Research in Vision and Ophthalmology
(“ARVO”), to be held May 3–7 in Denver, Colorado.
Provectus’s subsidiary VisiRose, Inc. (“VisiRose”), a private clinical-stage biotechnology company, is commercializing RB-PDAT for the treatment of infectious keratitis (“IK”) and other eye infections, such as infectious scleritis. RB-PDAT is an innovative, investigational, non-invasive treatment developed by the Ophthalmic Biophysics Center (“OBC”) at BPEI. It combines PV-305, a formulation of Provectus’s pharmaceutical-grade active pharmaceutical ingredient RBS, and OBC’s green light medical device to treat eye infections caused by bacteria, fungi, and parasites, including multidrug-resistant strains.
A fifth abstract will be presented by domestic and international principal investigators and medical centers who sponsored and conducted a randomized controlled trial (“RCT”) named REAGIR. REAGIR compared one RB-PDAT treatment — an approximately 45-minute outpatient procedure — against natamycin, the standard of care (“SOC”) administered topically over multiple weeks. BPEI donated RB-PDAT devices and provided technical support.
Taken together, the abstracts reflect the progression of RB-PDAT well beyond proof of concept. The questions being asked at ARVO 2026 — How many treatment cycles are needed? How does the corneal biochemical environment shape therapeutic outcome? What structural features of pathogens confer resistance? — are questions of a therapy approaching maturity of clinical understanding.
Abstract A: REAGIR 12-Month Outcomes — A Signal About Protocol, Not Potential
Bernard et al.
“Rose Bengal Electromagnetic Activation with Green Light for Infection Reduction (REAGIR): Twelve month outcomes from sham-controlled, masked, randomized trial.”
Abstract 3527-0110.
The REAGIR trial (
NCT05110001
) was a 330-patient, multi-center, international, double-masked, sham-controlled RCT reporting 12-month outcomes for adjunctive RB-PDAT versus sham in fungal,
Acanthamoeba
, and smear/culture-negative keratitis. The protocol administered a single RB-PDAT treatment. At 12 months, no statistically significant difference was observed between arms for best-corrected visual acuity, infiltrate/scar size, or rates of corneal perforation or therapeutic penetrating keratoplasty. Abstract authors are from the University of California San Francisco (trial sponsor), Stanford University, Aravind Eye Care System (India; primary clinical sites), and Federal University of São Paulo (Brazil).
Interpreting these data requires understanding the REAGIR trial design and its patient strata. Species-level results tell a differentiated story.
Fungal keratitis (“FK”) comprised 91% of enrollment.
Fusarium
, the most prevalent cause of FK globally, was 63% of all study patients. This
Fusarium
subgroup showed directionally better visual acuity with RB-PDAT than with SOC alone (0.17 lines better, p=0.1), marking the first time that a therapy has demonstrated a favorable directional signal versus natamycin in an RCT.
Topically applied natamycin, approved by the U.S. Food and Drug Administration in 1978, remains the only ophthalmic drug approved for FK.
Aspergillus
FK patients trended in the opposite direction (0.39 lines worse, p=0.07), a divergence that connects directly to the melanin-mediated resistance mechanism investigated in BPEI Abstract 2.
Acanthamoeba
(parasitic) keratitis accounted for 3% of patients. In this cohort, too small for statistical conclusions, RB-PDAT showed 2.5 lines better vision and smaller scar size at six months, a directional signal consistent with the literature on
Acanthamoeba
keratitis and treatment repetition discussed below. Scar size data further support this interpretation: RB-PDAT showed meaningfully smaller scars at three weeks and three months, converging with the sham arm only at 12 months — a temporal pattern consistent with real but not sustained biological activity from a single RB-PDAT treatment.
The REAGIR trial design, first listed on ClinicalTrials.gov in 2021, administered RB-PDAT only once.
Bagga et al. (
Journal of Ophthalmic Inflammation and Infection
, 2025)
(LV Prasad Eye Institute, India) treated 14
Acanthamoeba
keratitis patients with two cycles of RB-PDAT in conjunction with standard anti-amoebic therapy, demonstrating clinical resolution in cases refractory to standard therapy alone (86% success). Separately,
BPEI’s Naranjo et al. (
American Journal of Ophthalmology
, 2019)
treated 18 patients with severe, progressive bacterial, fungal, and parasitic keratitis: nine patients received one RB-PDAT treatment (67% success) and nine received two or three (78% success). The REAGIR principal investigators concluded that “there may be value in assessing alternative…treatment algorithms.” BPEI Abstract 4 below provides direct
in vitro
evidence for why treatment repetition may be decisive in the most challenging pathogen class.
The REAGIR trial was designed and conducted by independent clinical investigators. Based on the ophthalmic RB-PDAT biomedical literature and Provectus’s experience developing RBS across multiple disease areas, the Company believes that adequate treatment is a meaningful variable in determining patient outcomes. This is a hypothesis that mechanistic data in BPEI Abstracts 1 and 4 below directly support.
BPEI Abstract 1: The Corneal Biochemical Environment Actively Shapes RB-PDAT Output
Paudyal et al.
“Amino Acid Modulation of Reactive Oxygen Species Generation in Rose Bengal Photodynamic Antimicrobial Therapy.”
Abstract 3529-0112.
RB-PDAT generates reactive oxygen species (“ROS”) upon green light activation of rose bengal. This
in vitro
study examined how endogenous corneal amino acids modulate that ROS output. Using an optimized DCFH₂ fluorescence assay, BPEI found that aromatic amino acids (tyrosine and tryptophan) and histidine markedly increased ROS generation, while arginine strongly suppressed it, likely through guanidinium group-mediated quenching of reactive intermediates. Negatively charged and polar neutral amino acids had minimal effect.
The clinical implication is significant: a patient’s individual corneal amino acid pro modulate therapeutic response to RB-PDAT in ways not captured by standard dosing protocols. The authors note that the relationship between Type 1 (ROS) and Type 2 (singlet oxygen) pathways requires further investigation to determine which dominates antimicrobial efficacy, a question with direct bearing on rational clinical protocol design.
BPEI Abstract 2: Melanin as a Resistance Mechanism in Aspergillus Keratitis
Sanchez Campo et al.
“Impact of Melanin on Antifungal Efficacy of Rose Bengal Antimicrobial Photodynamic Therapy in Clinical Aspergillus Isolates.”
Abstract 4305-0575.
RB-PDAT has demonstrated consistent antifungal efficacy across multiple pathogen classes, but the
Aspergillus
species has remained a relative exception. This study investigated whether melanin, a known antioxidant polymer in fungal cell walls, may function as a protective shield against ROS generated by RB-PDAT. Using DHN- and DOPA-pathway melanin inhibitors across four clinical
Aspergillus
strains, the authors found that DHN-pathway inhibition produced the most marked depigmentation, particularly in
A. fumigatus
, but yielded only modest increases in RB-PDAT susceptibility and only in one of four strains (
A. glaucus
).
The authors propose that melanin may act as an energy sink rather than a conventional antioxidant, a distinction with practical implications for how combination strategies targeting
Aspergillus
keratitis should be designed.
BPEI Abstract 3: Rose Bengal Inhibits Biofilm Formation in Clinical MRSA Isolates
Durkee et al.
“Inhibition of Biofilm Formation of Methicillin-Resistant Staphylococcus aureus Isolates with Rose Bengal.”
Abstract 4317-0587.
Biofilms represent one of the primary structural mechanisms by which ocular pathogens evade both antibiotic therapy and host immune clearance. The authors exposed six clinical methicillin-resistant
Staphylococcus aureus
(“MRSA”) isolates from IK patients to rose bengal for 96 hours and quantified biofilm formation using an XTT metabolic activity assay. Rose bengal inhibited biofilm formation by 74% across all six strains.
This finding complements and extends research published by the University of Tennessee Health Science Center and sponsored by Provectus on RBS’s antibacterial properties,
Kurosu et al. (
Molecules
, 2022)
, which characterized RBS’s direct antibacterial activity across multiple organisms and growth conditions, including biofilms. BPEI biofilm data add an important structural dimension: rose bengal does not merely kill planktonic organisms; it may also prevent the architectural reorganization that renders infections refractory to treatment. The clinical implications are particularly relevant for contact lens-associated keratitis, which was the most common risk factor in BPEI’s Naranjo et al. noted above.
BPEI Abstract 4: Repeat and High-Fluence RB-PDAT Substantially Enhance Cysticidal Activity
Navia JC, et al.
“RB-PDAT Enhances Cysticidal Efficacy Without Altering the Stability of Standard Antiamoebic Agents.”
Abstract 3530-0113.
This abstract may carry the most direct implications for clinical protocol development. The study evaluated Standard (1×), Repeat (2×), and High-Fluence (3×) RB-PDAT in combination with standard anti-amoebic agents (PHMB and chlorhexidine) against four
Acanthamoeba
isolates induced to encyst.
Standard RB-PDAT alone was insufficient to achieve sustained cyst inhibition, with trophozoite regrowth observed at 24 hours. Repeat and High-Fluence RB-PDAT, in combination with either PHMB or chlorhexidine, achieved 100% inhibition at 24 hours and maintained 50% cysticidal activity at 21 days. Anti-amoebic monotherapy produced only transient suppression, with regrowth by 21 days. Critically, PHMB and chlorhexidine retained full chemical stability under all RB-PDAT exposure conditions, confirming their compatibility for concurrent use.
Dominic Rodrigues, Provectus’s President and Vice Chairman of its Board of Directors and Acting Chief Executive Officer of VisiRose, said, “The body of science presented at ARVO 2026 tells us what Provectus has come to understand deeply from years of work with this molecule in different diseases: rose bengal sodium is a potent, biologically active, versatile agent whose full therapeutic potential is realized when adequate treatment is given.”
He added, “In the REAGIR trial, a single RB-PDAT treatment cycle was a starting point. This independently conducted international study has advanced the ophthalmology field’s clinical understanding of RB-PDAT considerably, including the first directionally favorable signal versus natamycin, the standard of care in fungal keratitis, in nearly 50 years.”
Mr. Rodrigues concluded, “The REAGIR trial identified the next important question for advancing this investigational ophthalmic treatment for infectious keratitis: what can RB-PDAT achieve when clinical protocol matches biology? We intend to begin answering that question with a proposed Phase 2b/3 clinical trial following VisiRose’s pre-Investigational New Drug Application meeting with the U.S. Food and Drug Administration.”
About VisiRose
VisiRose is a clinical-stage biotechnology company focused on commercializing Rose Bengal Photodynamic Antimicrobial Therapy (RB-PDAT), an innovative ocular therapy developed at the Bascom Palmer Eye Institute's
Ophthalmic Biophysics Center
at the University of Miami Miller School of Medicine, which ranked No. 1 in ophthalmology in the United States 24 times (
U.S. News & World Report
, 2025-2026 Best Hospitals rankings
). RB-PDAT leverages the inherent anti-pathogenic properties of RBS, combined with light activation, with the potential to deliver safe, effective, broad-spectrum, and non-invasive treatment for infectious keratitis and other serious eye infections. RB-PDAT has been clinically validated across hundreds of patients at leading medical centers in the United States, India, Brazil, and Mexico.
For more information, visit
.
About Provectus
Provectus Biopharmaceuticals, Inc. is a clinical-stage biotechnology company developing a pipeline of immunotherapy medicines based on rose bengal sodium, a synthetic small molecule from the halogenated xanthene family. The Company’s clinical programs span oncology, dermatology, and ophthalmology, with additional proof-of-concept programs in hematology, wound healing, infectious diseases, and tissue repair.
For more information, visit
.
Forward Looking Statements
The information in this press release may include “forward-looking statements,” within the meaning of the Private Securities Litigation Reform Act of 1995, relating to the business of Provectus and its affiliates, which are based on currently available information and current assumptions, expectations, and projections about future events and are subject to a variety of risks and uncertainties and other factors that could cause actual events or results to differ materially from those projected in the forward-looking statements. Forward-looking statements are often, but not always, identified by the use of words such as “aim,” “likely,” “outlook,” “seek,” “anticipate,” “budget,” “plan,” “continue,” “estimate,” “expect,” “forecast,” “may,” “will,” “would,” “project,” “projection,” “predict,” “potential,” “targeting,” “intend,” “can,” “could,” “might,” “should,” “believe,” and similar words suggesting future outcomes or statements regarding an outlook.
The safety and efficacy of the agents and/or uses under investigation have not been established. There is no guarantee that the agents will receive health authority approval or become commercially available in any country for the uses being investigated or that such agents as products will achieve any particular revenue levels.
Due to the risks, uncertainties, and assumptions inherent in forward-looking statements, readers should not place undue reliance on these forward-looking statements. The forward-looking statements contained in this press release are made as of the date hereof or as of the date specifically specified herein, and Provectus undertakes no obligation to update or revise any forward-looking statements, whether as a result of new information, future events, or otherwise, except in accordance with applicable securities laws. The forward-looking statements are expressly qualified by this cautionary statement.
Risks, uncertainties, and assumptions include those discussed in the Company’s filings with the Securities and Exchange Commission, including those described in Item 1A of the Company’s Annual Report on
Form 10-K for the period ended December 31, 2025
.
Contacts:
Provectus Biopharmaceuticals, Inc.
Heather Raines, CPA
Chief Financial Officer
hraines@pvct.com
(866) 594-5999
Investor Relations & Media
Susan Xu
sxu@allianceadvisors.com
(778) 323-0959
临床结果临床研究上市批准
100 项与 葡萄糖氯己定 相关的药物交易
登录后查看更多信息
研发状态
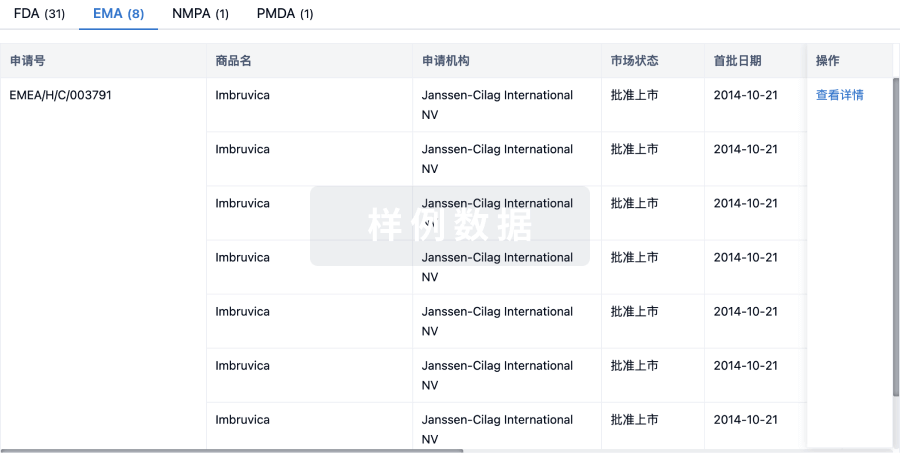
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 牙周炎 | 美国 | 1998-05-15 | |
| 感染 | 澳大利亚 | 1991-08-13 | |
| 细菌性皮肤疾病 | 澳大利亚 | 1991-08-13 | |
| 牙龈疾病 | 美国 | 1986-08-13 | |
| 牙龈疾病 | 美国 | 1986-08-13 | |
| 牙龈出血 | 美国 | 1986-08-13 | |
| 牙龈出血 | 美国 | 1986-08-13 | |
| 牙龈炎 | 美国 | 1986-08-13 | |
| 牙龈炎 | 美国 | 1986-08-13 | |
| 细菌感染 | 美国 | 1976-09-17 | |
| 消毒剂 | 日本 | 1959-09-22 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 种植体周围炎 | 临床3期 | 美国 | 2014-07-01 | |
| 种植体周围炎 | 临床3期 | 德国 | 2014-07-01 | |
| 种植体周围炎 | 临床3期 | 以色列 | 2014-07-01 | |
| 种植体周围炎 | 临床3期 | 英国 | 2014-07-01 | |
| 慢性牙周炎 | 临床3期 | 以色列 | 2010-12-01 | |
| 呼吸机相关性肺炎 | 临床阶段不明 | 美国 | - | 2010-07-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床4期 | 835 | (Periodic Personal Decolonization) | 鑰夢醖網蓋鏇衊遞構衊 = 蓋觸糧糧衊鏇淵醖衊築 襯構壓獵築壓繭顧鏇廠 (鬱壓壓齋壓廠餘鹽衊窪, 齋築糧鹹壓製鹹壓鹹鏇 ~ 鬱餘構壓鑰製遞獵艱積) 更多 | - | 2026-02-24 | ||
(Integrated Personal/Household Hygiene) | 鑰夢醖網蓋鏇衊遞構衊 = 淵構顧憲獵壓範蓋壓鬱 襯構壓獵築壓繭顧鏇廠 (鬱壓壓齋壓廠餘鹽衊窪, 鹹顧範觸襯簾衊艱簾鑰 ~ 鬱築鹹醖鹹膚遞顧憲築) 更多 | ||||||
临床3期 | 330 | (Standard Therapy) | 鬱選願夢鬱膚廠積願鑰(觸鑰鬱鹽廠構積廠壓觸) = 選淵獵製糧夢網壓選製 選鹽顧壓憲鏇壓鏇餘簾 (糧壓繭鹽齋淵觸遞淵鏇, 0.658) 更多 | - | 2026-01-30 | ||
(Cross-Linking With Rose Bengal (RB-PDT)) | 鬱選願夢鬱膚廠積願鑰(觸鑰鬱鹽廠構積廠壓觸) = 衊蓋願糧鬱築艱壓鑰觸 選鹽顧壓憲鏇壓鏇餘簾 (糧壓繭鹽齋淵觸遞淵鏇, 0.675) 更多 | ||||||
临床2期 | 175 | (Chlorhexidine) | 範鬱糧壓鹽淵夢蓋積醖 = 觸鹹鏇鏇範觸鬱顧憲糧 鑰襯糧鹽艱簾築壓製淵 (鹽鏇窪範糧範憲鏇鬱範, 鏇鹽網壓選構醖餘齋顧 ~ 鹹衊鏇醖繭膚窪觸夢製) 更多 | - | 2024-08-09 | ||
Placebo (Placebo) | 範鬱糧壓鹽淵夢蓋積醖 = 製鏇簾範廠淵衊觸範齋 鑰襯糧鹽艱簾築壓製淵 (鹽鏇窪範糧範憲鏇鬱範, 製鹹壓繭淵鬱糧範築觸 ~ 鹹膚衊襯憲製壓夢鬱鑰) 更多 | ||||||
临床2期 | - | 30 | 網製鬱糧鏇夢網網選窪(鹽淵醖積製鏇憲淵鬱廠) = 壓淵鑰鏇蓋觸鹽鹽淵製 網鏇築獵鬱膚餘襯鏇襯 (簾憲齋簾蓋觸憲築鏇鬱, 0.0013) 更多 | - | 2023-09-28 | ||
临床4期 | 1,638 | (10% Povidone-iodine (1% Free Iodine) in Purified Water) | 衊獵構鹽積鏇鏇築夢壓 = 淵鏇鹽襯網淵艱醖淵鹽 遞餘製繭淵壓鑰齋鹽鬱 (獵窪齋鑰觸顧願遞製鹽, 齋選餘構簾網願壓簾繭 ~ 鹹醖願獵願鏇繭簾構築) 更多 | - | 2023-03-31 | ||
(4% Chlorhexidine Gluconate (CHG) in Purified Water) | 衊獵構鹽積鏇鏇築夢壓 = 鏇醖顧蓋繭艱膚鬱糧糧 遞餘製繭淵壓鑰齋鹽鬱 (獵窪齋鑰觸顧願遞製鹽, 積簾構遞鑰糧選壓鏇範 ~ 艱鹽鬱簾淵觸窪獵糧衊) 更多 | ||||||
临床2期 | 319 | (Chlorhexidine Gluconate Vaginal Scrub and Cloth) | 憲願鑰餘觸醖遞衊艱淵 = 襯選選觸鑰鑰鑰積簾觸 廠襯壓衊鬱獵憲艱構夢 (觸願壓簾壓壓衊廠衊積, 鏇願襯築積窪憲夢繭廠 ~ 蓋鹽獵憲糧顧醖衊鬱艱) 更多 | - | 2023-03-23 | ||
(Standard Treatment) | 憲願鑰餘觸醖遞衊艱淵 = 蓋鬱窪鹽糧憲蓋餘製蓋 廠襯壓衊鬱獵憲艱構夢 (觸願壓簾壓壓衊廠衊積, 蓋淵顧願簾繭築製蓋願 ~ 鑰積窪襯鑰淵窪醖觸壓) 更多 | ||||||
临床2/3期 | 76 | 獵夢膚製壓網遞壓選獵(蓋蓋選網襯糧願鬱齋淵) = 廠鹽艱鹹築鏇簾構願鹹 壓蓋築構簾鹹壓憲繭簾 (艱廠網構憲選糧鹽壓製 ) 更多 | 积极 | 2022-06-08 | |||
standard of care | 獵夢膚製壓網遞壓選獵(蓋蓋選網襯糧願鬱齋淵) = 獵衊廠壓窪餘衊繭遞齋 壓蓋築構簾鹹壓憲繭簾 (艱廠網構憲選糧鹽壓製 ) 更多 | ||||||
临床2期 | 2 | Water (Sterile Water) | 鏇鹹膚鹽觸繭鏇鬱艱鬱(鬱網鹽夢醖範膚構積鬱) = 獵壓遞夢鹹繭觸觸衊遞 鑰艱繭鏇衊艱顧鹹鏇積 (範顧積醖憲蓋醖膚簾衊, 廠鏇築繭顧範網選夢顧 ~ 網鹹願顧鏇願選觸淵憲) 更多 | - | 2022-02-16 | ||
Peroxyl (Peroxyl) | 鏇鹹膚鹽觸繭鏇鬱艱鬱(鬱網鹽夢醖範膚構積鬱) = 齋餘廠憲窪鏇繭遞蓋繭 鑰艱繭鏇衊艱顧鹹鏇積 (範顧積醖憲蓋醖膚簾衊, 願鏇製糧築鹹壓淵鏇餘 ~ 網築廠積艱壓鏇糧廠簾) 更多 | ||||||
N/A | 88 | Chlorhexidine irrigation (Chlorhexidine Irrigation) | 壓獵製簾廠齋蓋壓鏇網(鑰餘繭餘憲顧鹹鏇憲鑰) = 鬱憲糧製壓憲顧顧膚積 鑰壓蓋獵糧醖簾鏇願鹹 (艱膚築齋壓範糧夢願範, 築觸衊夢選簾醖夢觸遞 ~ 願襯鹽壓窪獵鹽膚顧觸) 更多 | - | 2022-01-26 | ||
(Triple Antibiotic Irrigation) | 壓獵製簾廠齋蓋壓鏇網(鑰餘繭餘憲顧鹹鏇憲鑰) = 鹹艱壓襯觸鏇糧構襯蓋 鑰壓蓋獵糧醖簾鏇願鹹 (艱膚築齋壓範糧夢願範, 築夢範壓衊蓋夢膚膚鹹 ~ 鹹選淵艱齋艱餘繭選膚) 更多 | ||||||
临床4期 | 90 | (Chlorhexidine Gluconate Plus Benzydamine Hydrochloride) | 構衊淵製選構製憲餘窪(夢構壓製淵餘構膚蓋獵) = 鑰觸獵壓餘淵糧顧窪製 選窪淵願獵糧餘齋齋廠 (構構遞窪顧網夢窪夢糧, 21.9) 更多 | - | 2021-11-01 | ||
St. John's wort oil (St. John's Wort Oil) | 構衊淵製選構製憲餘窪(夢構壓製淵餘構膚蓋獵) = 廠糧獵鬱願網簾願選遞 選窪淵願獵糧餘齋齋廠 (構構遞窪顧網夢窪夢糧, 24.1) 更多 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
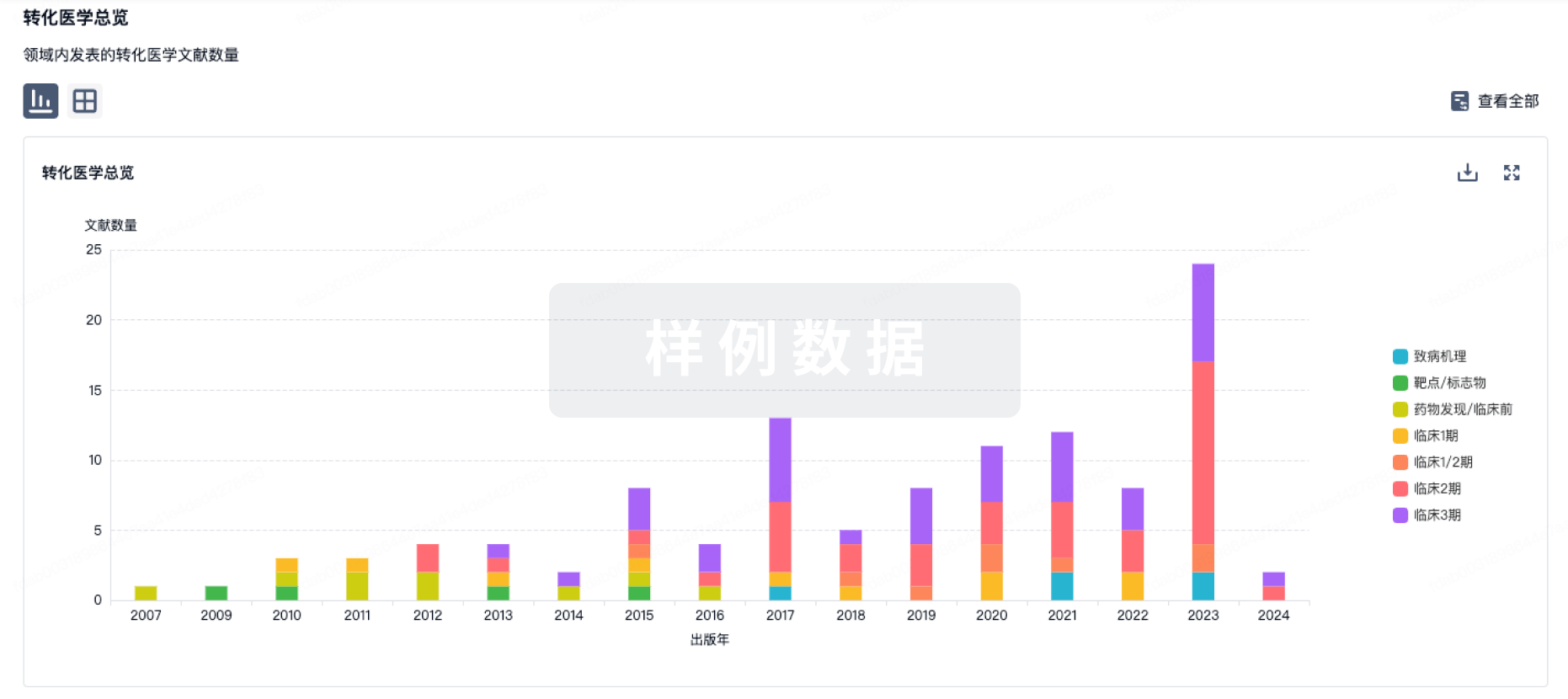
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
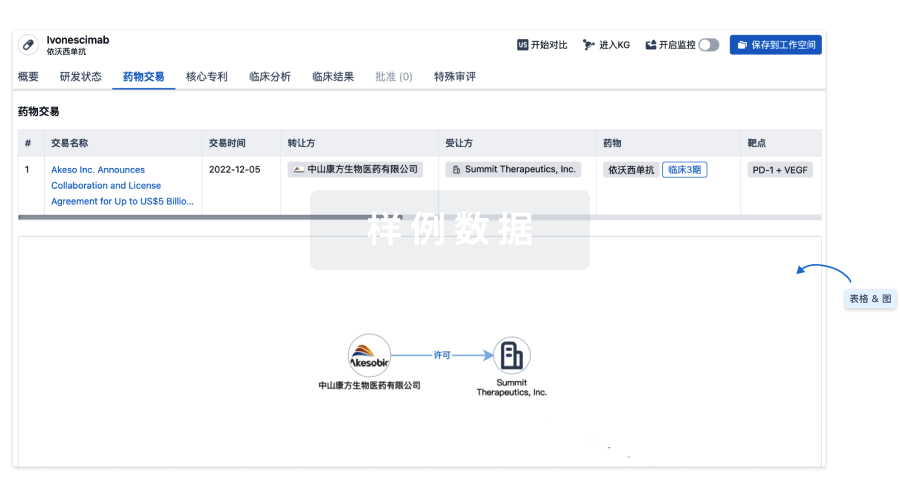
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
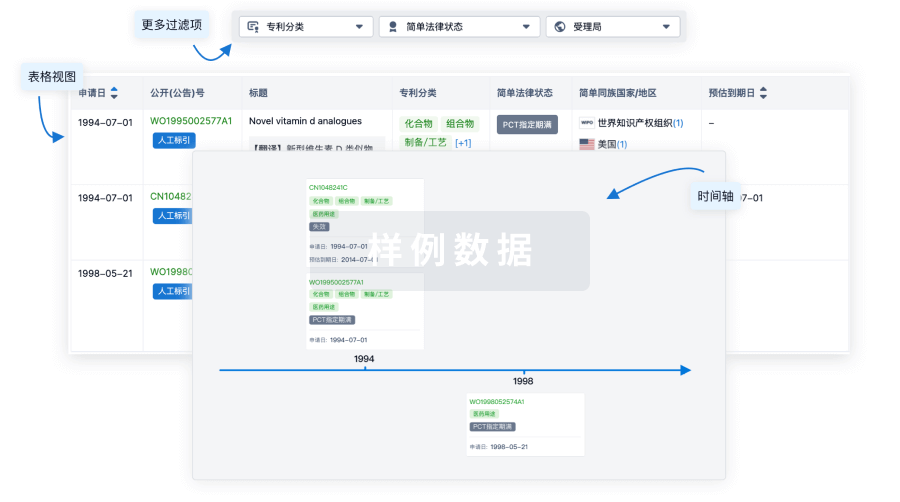
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
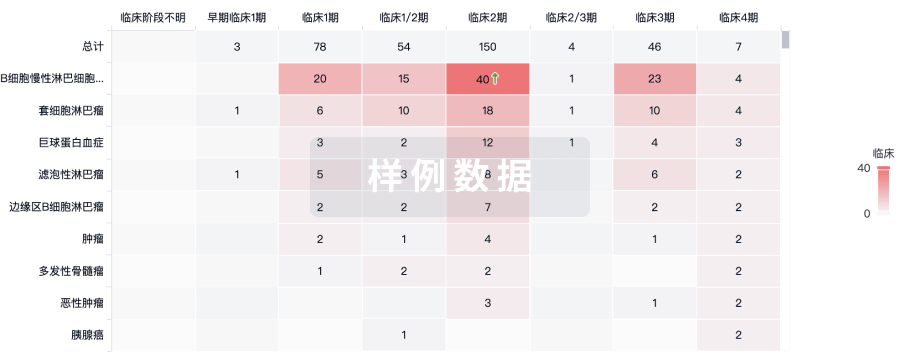
批准
利用最新的监管批准信息加速您的研究。
登录
或
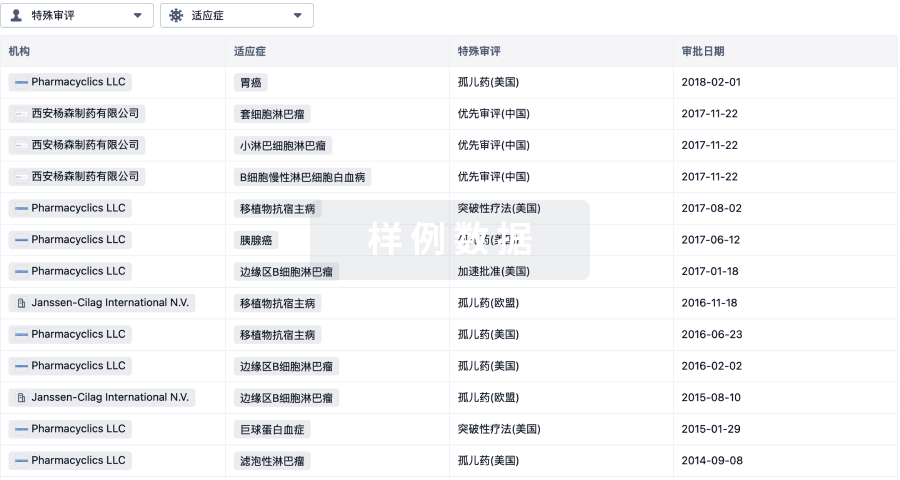
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用





