预约演示
更新于:2026-05-13
Thiotepa
塞替派
更新于:2026-05-13
概要
基本信息
最高研发阶段批准上市 |
最高研发阶段(中国)批准上市 |
特殊审评孤儿药 (美国)、孤儿药 (韩国)、孤儿药 (澳大利亚)、快速通道 (美国) |
登录后查看时间轴
结构/序列
分子式C6H12N3PS |
InChIKeyFOCVUCIESVLUNU-UHFFFAOYSA-N |
CAS号52-24-4 |
关联
280
项与 塞替派 相关的临床试验NCT07257419
CD45RA-depleted CD19-CAR T Cell Consolidation After TCRαβ+/CD19 B Cell-depleted Haploidentical Hematopoietic Cell Transplantation for Relapsed/Refractory CD19+ ALL and Lymphoma
The purpose of this study is to learn more about newer methods of transplanting blood cells donated by a partially matched family member to children with high-risk CD19 positive leukemia ALL.
Primary Objective:
- To assess the safety and feasibility of combining CD19-CAR(Mem) T cells after TCRαβ+/CD19 depleted haploidentical donor transplantation for pediatric patients with relapsed/refractory CD19+ B-cell malignancies.
Secondary Objectives:
* To estimate 1-year post-transplant overall survival, event-free survival, and GVHD-free relapse-free survival (GRFS).
* To estimate cumulative incidence of engraftment, acute and chronic GVHD, and immune-related adverse events, including CRS and ICANS.
Primary Objective:
- To assess the safety and feasibility of combining CD19-CAR(Mem) T cells after TCRαβ+/CD19 depleted haploidentical donor transplantation for pediatric patients with relapsed/refractory CD19+ B-cell malignancies.
Secondary Objectives:
* To estimate 1-year post-transplant overall survival, event-free survival, and GVHD-free relapse-free survival (GRFS).
* To estimate cumulative incidence of engraftment, acute and chronic GVHD, and immune-related adverse events, including CRS and ICANS.
开始日期2026-06-03 |
NCT05565105
A Phase II Trial of CD34+ Enriched Transplants From HLA-Compatible Related or Unrelated Donors for Treatment of Patients With Leukemia or Lymphoma
This study will evaluate whether processing blood stem cell transplants using an investigational device (the CliniMACS system) results in less complications for patients undergoing transplant for treatment of a blood malignancy (cancer) or blood disorder.
开始日期2026-06-01 |
NCT07565220
Phase 1 Trial of Thiotepa-based Conditioning Regimen With De-escalated Post-graft Cyclophosphamide for Allogeneic Stem Cell Transplantation in Hematologic Malignancies
This phase 1 trial will investigate the safety and effectiveness of Thiotepa, Busulfan, and Fludarabine (TBF) conditioning regimen with post-transplant cyclophosphamide (PTCy) in HLA-matched related or unrelated donor allogeneic stem cell transplantation (alloSCT).
开始日期2026-06-01 |
申办/合作机构 |
100 项与 塞替派 相关的临床结果
登录后查看更多信息
100 项与 塞替派 相关的转化医学
登录后查看更多信息
100 项与 塞替派 相关的专利(医药)
登录后查看更多信息
3,229
项与 塞替派 相关的文献(医药)2026-05-01·JOINT BONE SPINE
High-dose chemotherapy and transplantation of autologous CD34+ selected stem cells for progressive systemic sclerosis adjusted to cardiac and lung manifestation: An open-label, non-inferiority phase 2 trial
Article
作者: Vogel, Wichard ; Wirths, Stefan ; Krumm, Patrick ; Henes, Joerg ; Pecher, Ann-Christin ; Peis, Katrin ; Klein, Reinhild ; Lengerke, Claudia ; Schmalzing, Marc ; Koetter, Ina
OBJECTIVES:
Autologous hematopoietic stem cell transplantation (aHSCT) for systemic sclerosis (SSc) is an effective treatment strategy but carries a high treatment-related mortality (TRM). Consequently, patients with severe organ dysfunction have been excluded from previous randomized trials such as ASTIS. This study aimed to evaluate the feasibility and non-inferiority of a disease-manifestation - adapted chemotherapy protocol designed to mitigate toxicity to also treat patients who would have been ASTIS-ineligible.
METHODS:
In this prospective, open-label, monocentric, phase II non-inferiority trial at the University Hospital Tübingen, Germany, patients with progressive SSc (disease duration≤6 years) were stratified by lung and cardiac involvement. Mobilization included 1500mg/m2 cyclophosphamide (CYC) for patients with inflammatory interstitial lung disease (iILD) versus 1000mg/m2 otherwise, both reduced compared to the ASTIS protocol. Conditioning comprised rabbit anti-thymocyte globulin (4×10mg/kg); patients without cardiac involvement additionally received CYC 4×50mg/kg. In those with cardiac involvement, CYC was reduced by 50% and thiotepa (2×5mg/kg) was added.
RESULTS:
Between 09/2012 and 07/2022, 35 patients were treated (no iILD/cardiac involvement: n=14; iILD only: n=3; cardiac only: n=12; both: n=6). Three-year overall survival (OS) was 77%, meeting non-inferiority compared to EBMT registry data (80%). TRM within 100 days was 11% (n=4) in the whole group.
CONCLUSIONS:
This adapted regimen showed comparable 3y-OS in patients with advanced organ involvement who would have been excluded from prior trials. While feasibility is demonstrated, aHSCT in this high-risk population remains associated with substantial risk, and efficacy cannot be definitively established. Further studies are warranted.
2026-05-01·PEDIATRIC BLOOD & CANCER
Group 4 Medulloblastomas of Early Childhood Treated With High‐Dose Chemotherapy‐ and Craniospinal Irradiation‐Sparing Approach
Article
作者: Michaiel, George ; Doris, Kathleen ; Mazewski, Claire ; Hukin, Juliette ; Schlosser, Mary Pat ; Rutkowski, Stefan ; Lopez, Vicente Santa‐Maria ; Pillay‐Smiley, Natasha ; Cheng, Sylvia ; Bracher, Annalise ; Margol, Ashley S. ; Bouffet, Eric ; Abdelbaki, Mohamed S. ; Orduña, Patricia ; Cluster, Andrew ; Magimairajan, Vanan ; Salloum, Ralph ; Mynarek, Martin ; Ramaswamy, Vijay ; Aguilera, Dolly ; Hoffman, Lindsey ; Lassaletta, Alvaro ; Zapotocky, Michal ; Senapati, Akanksha ; Cansanay, Rose Daynielle ; Chi, Susan ; Lafay‐Cousin, Lucie ; Erker, Craig ; Sait, Sameer Farouk ; Ratterman, Erin ; Cacciotti, Chantel ; Harrod, Virginia ; Ronsley, Rebecca
ABSTRACT:
Background:
Group 4 medulloblastoma (MB) is rare in young children. Data on craniospinal irradiation (CSI)‐sparing approaches are limited.
Methods:
This multicenter study reported outcomes for patients younger than 7 years old with Group 4 MB treated with high‐dose chemotherapy (HDC) without adjuvant CSI.
Results:
Thirty‐eight patients were included (26 M/12 F). Median age at diagnosis was 46.4 months (25.9–78), with 24% ≤36 months. Twenty‐four patients (63.2%) had localized disease. Fourteen (36.8%) presented with metastatic disease, and 26 (68.4%) underwent gross total resection (GTR). The most used HDC regimens were carboplatin/thiotepa (76.3%) and carboplatin/thiotepa/etoposide (21.1%). Twenty (52.6%) relapses occurred at a median 21.9 months (5–99.8) from diagnosis. Patients with upfront GTR and/or who received three cycles of HDC had better PFS (
p
= 0.02 and
p
= 0.002, respectively). Local relapse accounted for 45%. Eighteen patients received salvage therapy with curative intent, all with radiotherapy (16 = CSI, 2 = focal). The CSI dose ranged from 18 to 36 Gy, and 43.7% received ≤23.4 Gy. Patients who underwent salvage surgery and/or chemotherapy were more likely to receive CSI ≤23.4 Gy (
p
= 0.008 and
p
= 0.03). The 5‐year post‐relapse survival and overall survival (OS) were, respectively, 60.3% (95% confidence interval [CI]: 26.9–82) and 72.7% (95% CI: 51.9–85.7). The 5‐year CSI‐free OS was 69.7% (95% CI: 39.1–87.1).
Conclusion:
High dose chemotherapy for Group 4 MB was associated with a relapse rate of 52.6%, which favorably compares to data reported with conventional chemotherapy. Salvage radiotherapy retrieved more than two‐thirds of the patients. Half of the survivors never received radiotherapy. Such an approach may represent an alternative to upfront CSI for young children with Group 4 MB.
2026-04-28·Blood Advances
Allogeneic HSCT for consolidation in pediatric refractory or relapsed ALK-positive anaplastic large cell lymphoma
Article
作者: Beier, Rita ; Basu, Oliver ; Bader, Peter ; Lang, Peter ; Zimmermann, Martin ; Pichler, Herbert ; Meissner, Barbara ; Müller, Ingo ; Woessmann, Wilhelm ; Burkhardt, Birgit ; Knörr, Fabian ; Seidl, Jakob ; Damm-Welk, Christine ; Attarbaschi, Andishe
Abstract:
Allogeneic hematopoietic stem cell transplantation (HSCT) is used for consolidation in children and adolescents with refractory or early relapsed ALK (anaplastic lymphoma kinase)–positive anaplastic large cell lymphoma (ALCL). The immune system plays a major role in sustained disease control. We retrospectively analyzed whether conditioning, donor type, and in vivo T-cell depletion correlate with outcome in a population-based cohort of 57 children with central nervous system (CNS)–negative ALCL relapse who received HSCT between 2005 and 2022. Progression-free survival (PFS) and overall survival from transplantation were 84% ± 10% and 91% ± 8% at 3 years, respectively. Conditioning was based on total body irradiation (TBI) in 30 patients and on chemotherapy in 27 patients, mainly with reduced-toxicity conditioning (treosulfan, fludarabine, and thiotepa). PFS and graft-versus-host disease (GVHD)–free and event-free survival (GEFS) were comparable between TBI and chemotherapy, 87% ± 6% vs 81% ± 8% (P = .62) and 67% ± 9% vs 74% ± 8% (P = .63), respectively. Patients with transplantation from unrelated donors with rabbit anti–human T lymphocyte globulin (ATLG) had superior PFS and GEFS than those receiving grafts from matched siblings without ATLG: 94% ± 7% vs 67% ± 22% (P = .0007) and 82% ± 13% vs 44% ± 24% (P = .011), respectively. Progression during frontline chemotherapy, minimal residual disease, and remission status at HSCT were not associated with outcome. Nonrelapse mortality was 5.6% for all 65 patients, and cumulative incidence of grade 2 to 4 acute GVHD was 25%. Our data supports the use of TBI-free conditioning and suggest improved outcomes with unrelated donors receiving ATLG prophylaxis.
123
项与 塞替派 相关的新闻(医药)2026-05-11
·和泽医药
捷报频传:近日,和泽医药凭借其专业高效的技术服务,成功助力多家客户项目顺利获批!
热/烈/祝/贺
CELEBRATE
GOOD NEWS
硫酸氨基葡萄糖胶囊
近日,和泽医药助力合作伙伴河南福森药业有限公司持有的硫酸氨基葡萄糖胶囊按化学药品4类成功获批。
硫酸氨基葡萄糖胶囊可治疗原发性及继发性骨关节炎。骨关节炎是关节软骨蛋白多糖生物合成异常而呈现退行性变的结果。氨基葡萄糖是一种天然的氨基单糖,是蛋白多糖合成的前体物质,可以刺激软骨细胞产生有正常多聚体结构的蛋白多糖,提高软骨细胞的修复能力,抑制损伤软骨的酶如胶原酶和磷酯酶A2,并可防止损伤细胞的超氧化自由基的产生,可以促进软骨基质的修复和重建,从而可延缓骨关节疼痛的病理过程和疾病的进程,改善关节活动,缓解疼痛。
注射用塞替派
近日,和泽医药助力合作伙伴黑龙江福和制药集团持有的注射用塞替派按化学仿制药3类成功获批。
注射用塞替派最初由美国Cyanamid公司开发,属于一种能够抑制DNA合成的抗肿瘤烷化剂。该药最早于1959年在美国获批,随后在2017年,Adienne公司生产的15mg及100mg规格产品不仅在美国上市(被《橙皮书》列为RLD和RS),也在加拿大上市。值得一提的是,2016年FDA曾批准其用于3级β-地中海贫血儿科患者的移植预处理,以降低排斥风险,但该适应症产品此前一直未进入中国。
此次黑龙江福和制药集团注射用塞替派的上市,使其成为国内第四家拥有该品种的企业。其获批的适应症明确为:用于重型β-地中海贫血儿童(<18周岁)在进行异基因造血干细胞移植(allo-HSCT)前的预处理。
盐酸尼卡地平注射液
近日,和泽医药助力合作伙伴漯河市汇创医药有限公司持有的盐酸尼卡地平注射液按化学药品4类成功获批,并视同通过一致性评价。
盐酸尼卡地平注射液最早由日本山之内药业(现安斯泰来制药)开发,盐酸尼卡地平注射液首次于1989年在日本获批上市,在2001年8月获批进口中国。临床上用于手术室异常高血压的紧急处理,以及高血压急症。
注射用氯诺昔康
近日,和泽医药助力嘉亨(珠海横琴)医药科技有限公司的4类仿制药注射用氯诺昔康视同通过一致性评价。
在临床应用中,注射用氯诺昔康主要用于手术后急性中度疼痛的短期治疗。
氯诺昔康是一种具有镇痛作用的非甾体类抗炎药。系噻嗪类衍生物。氯诺昔康的作用机制主要通过抑制环氧化酶(COX)活性而抑制前列腺素,导致外周伤害感受器脱敏,从而抑制炎症。另外一种作用机制为中枢镇痛作用。
美阿沙坦钾片
近日,和泽医药助力合作伙伴合肥国高药业有限公司持有的美阿沙坦钾片按化学药品4类成功获批,并视同通过一致性评价。
美阿沙坦钾片是新一代血管紧张素II受体拮抗剂(ARB),临床用于治疗成人原发性高血压。
本品口服后迅速转化为活性成分阿齐沙坦,选择性阻断血管紧张素II与AT1受体的结合。其独特分子结构带来显著降压效果:一项纳入中国30多个中心的临床研究显示,80mg剂量治疗8周诊室收缩压平均降低24.2mmHg。优于缬沙坦160mg(降低20.6mmHg),且对24小时动态血压控制更为平稳。安全性方面,美阿沙坦钾总体耐受性良好,不良反应多为轻至中度,最常见为头晕,整体不良反应发生率与安慰剂相似。
骨化三醇软胶囊
近日,和泽医药助力合作伙伴大连美创药业有限公司、山东简道制药有限公司的骨化三醇软胶囊按化学药品4类成功获批。
骨化三醇软胶囊主要用于
1.绝经后骨质疏松
2.慢性肾功能衰竭,尤其是接受血液透析患者之肾性骨营养不良症;
3.术后甲状旁腺功能低下;
4.特发性甲状旁腺功能地下;
5.假性甲状旁腺功能地下;
6.维生素D依赖性佝偻病;
7.低血鳞性维生素D抵抗型佝偻病等。
END
2026-05-05
·信狐药迅
每周药品注册获批数据,分门别类呈现,一目了然。(4.27-5.5)
新药上市申请
无
新药临床申请
药品名称
企业
注册分类
受理号
拉尼兰诺片
正大天晴(广州)医药有限公司
1
CXHL2600380
HRS-6209胶囊
江苏恒瑞医药股份有限公司
1
CXHL2600223
HRS-8080片
山东盛迪医药有限公司
1
CXHL2600216
HRS-8080片
山东盛迪医药有限公司
1
CXHL2600215
HRS-9813 胶囊
广东恒瑞医药有限公司
1
CXHL2600217
GLB-002胶囊
杭州格博生物医药有限公司
1
CXHL2600209
RFUS-188注射液
宜昌人福药业有限责任公司
1
CXHL2600189
注射用BXOS116
拜西欧斯(北京)生物技术有限公司
1
CXHL2600169
YL-18319片
上海璎黎药业有限公司
1
CXHL2600173
YL-18319片
上海璎黎药业有限公司
1
CXHL2600172
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600164
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600163
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600162
JY54注射液
杭州九源基因生物医药股份有限公司
1
CXHL2600160
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600158
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600157
HS-10522片
江苏豪森药业集团有限公司
1
CXHL2600156
WS-0101溶液
北京厚燊维康科技有限责任公司
1
CXHL2600155
QLS7320注射液
齐鲁制药有限公司
1
CXHL2600167
QLS7320注射液
齐鲁制药有限公司
1
CXHL2600165
INS018_055B雾化吸入剂
英矽智能科技(上海)有限公司
1
CXHL2600145
ICF004吸入粉雾剂
长风苏粤药业(广州)有限公司
1
CXHL2600133
ICF004吸入粉雾剂
长风苏粤药业(广州)有限公司
1
CXHL2600132
氨酚羟考酮缓释片
上海理想制药有限公司
2.2
CXHL2600207
ZD2202
浙江智达药业有限公司
2.2
CXHL2600186
甲磺酸伏美替尼片
上海艾力斯医药科技股份有限公司
2.4
CXHL2600194
TXA-070片
武汉科福新药有限责任公司
2.4
CXHL2600168
冻干乙型脑炎灭活疫苗(人二倍体细胞)
安徽智飞龙科马生物制药有限公司
2.2
CXSL2600147
GenSci161注射液
长春金赛药业有限责任公司
1
CXSL2600347
注射用SIM0613
上海先纬医药科技有限公司
1
CXSL2600239
注射用SHR-5421
苏州盛迪亚生物医药有限公司
1
CXSL2600237
SCTB35注射液
神州细胞工程有限公司
1
CXSL2600236
SCTB35注射液
神州细胞工程有限公司
1
CXSL2600235
SHR-3079注射液
苏州盛迪亚生物医药有限公司
1
CXSL2600231
SHR-3079注射液
苏州盛迪亚生物医药有限公司
1
CXSL2600230
注射用DEC003M
杭州多禧生物科技有限公司
1
CXSL2600221
注射用SIBP-A17
上海生物制品研究所有限责任公司
1
CXSL2600220
注射用QLS4131
齐鲁制药有限公司
1
CXSL2600210
注射用SIBP-A19
上海生物制品研究所有限责任公司
1
CXSL2600207
注射用ZL-6201
再鼎医药(上海)有限公司
1
CXSL2600217
ZHB118舌下片
江苏众红生物工程创药研究院有限公司
1
CXSL2600193
ZHB118舌下片
江苏众红生物工程创药研究院有限公司
1
CXSL2600190
EA5注射液皮下制剂
上海览屹医药科技有限公司
1
CXSL2600196
CG001注射液
上海康景生物医药科技有限公司
1
CXSL2600194
SSS68注射液
沈阳三生制药有限责任公司
1
CXSL2600191
SSS68注射液
沈阳三生制药有限责任公司
1
CXSL2600189
SSS68注射液
沈阳三生制药有限责任公司
1
CXSL2600188
注射用BG-T187(皮下注射)
广州百济神州生物制药有限公司
1
CXSL2600197
ZHB117舌下片
江苏众红生物工程创药研究院有限公司
1
CXSL2600184
ZHB117舌下片
江苏众红生物工程创药研究院有限公司
1
CXSL2600183
ALXN2220注射液
阿斯利康全球研发(中国)有限公司
1
CXSL2600185
9MW2821
迈威(上海)生物科技股份有限公司
1
CXSL2600177
XY101
西安血氧生物技术有限公司
1
CXSL2600148
RRG001眼内注射液
上海鼎新基因科技有限公司
1
CXSL2600141
QL2109注射液
齐鲁制药有限公司
2.2
CXSL2600211
埃诺格鲁肽注射液
杭州先为达生物科技股份有限公司
2.2
CXSL2600200
埃诺格鲁肽注射液
杭州先为达生物科技股份有限公司
2.2
CXSL2600199
重组人神经生长因子滴眼液
重庆科润生物医药研发有限公司
2.2
CXSL2600179
重组人神经生长因子滴眼液
重庆科润生物医药研发有限公司
2.2
CXSL2600178
仿制药申请
药品名称
企业
注册分类
受理号
艾曲泊帕乙醇胺干混悬剂
沈阳三生制药有限责任公司
3
CYHS2502182
碳酸氢钠注射液
南京赛瑞谱顿制药有限公司
3
CYHS2404225
碳酸氢钠注射液
南京赛瑞谱顿制药有限公司
3
CYHS2404224
洛索洛芬钠口服溶液
合肥启旸生物医药科技有限公司
3
CYHS2403938
盐酸普萘洛尔注射液
石家庄四药有限公司
3
CYHS2403897
盐酸普萘洛尔注射液
石家庄四药有限公司
3
CYHS2403896
尼麦角林片
华润双鹤利民药业(济南)有限公司
3
CYHS2403829
甲苯磺酸艾多沙班口腔崩解片
江苏和晨药业有限公司
3
CYHS2403760
复方葡萄糖/电解质颅脑手术冲洗液
昆明南疆制药有限公司
3
CYHS2403702
硝酸甘油注射液
海南未见药业有限公司
3
CYHS2403689
盐酸溴己新注射液
以岭万洲国际制药有限公司
3
CYHS2403484
西咪替丁注射液
大理药业股份有限公司
3
CYHS2403418
吡拉西坦注射液
山东力诺制药有限公司
3
CYHS2403348
吡拉西坦注射液
山东力诺制药有限公司
3
CYHS2403347
重酒石酸卡巴拉汀口服液
北京双鹭药业股份有限公司
3
CYHS2403319
重酒石酸卡巴拉汀口服液
北京双鹭药业股份有限公司
3
CYHS2403318
布瑞哌唑口腔崩解片
山东新时代药业有限公司
3
CYHS2403218
布瑞哌唑口腔崩解片
山东新时代药业有限公司
3
CYHS2403217
布瑞哌唑口腔崩解片
山东新时代药业有限公司
3
CYHS2403216
布美他尼注射液
平光制药股份有限公司
3
CYHS2403200
注射用硫酸多黏菌素B
海南合瑞制药股份有限公司
3
CYHS2403185
ω-3鱼油中长链脂肪乳/氨基酸(16)/葡萄糖(16)注射液
湖北一半天制药有限公司
3
CYHS2403133
盐酸艾司氯胺酮注射液
国药集团国瑞药业有限公司
3
CYHS2403135
盐酸左西替利嗪口服溶液
北京双鹭药业股份有限公司
3
CYHS2403020
盐酸左西替利嗪口服溶液
北京双鹭药业股份有限公司
3
CYHS2403019
西咪替丁注射液
石家庄凯达生物工程有限公司
3
CYHS2402968
尼美舒利片
上海理想制药有限公司
3
CYHS2402594
中性低钙腹膜透析液(碳酸氢盐-G4.25)
山东齐都药业有限公司
3
CYHS2402510
中性低钙腹膜透析液(碳酸氢盐-G2.5)
山东齐都药业有限公司
3
CYHS2402509
中性低钙腹膜透析液(碳酸氢盐-G1.5)
山东齐都药业有限公司
3
CYHS2402508
维生素B6注射液
苏州朗科生物技术股份有限公司
3
CYHS2402443
甲硫酸新斯的明注射液
成都百裕制药股份有限公司
3
CYHS2402410
甲硫酸新斯的明注射液
成都百裕制药股份有限公司
3
CYHS2402409
甲硫酸新斯的明注射液
成都百裕制药股份有限公司
3
CYHS2402408
硝普钠注射液
重庆药友制药有限责任公司
3
CYHS2402082
注射用塞替派
黑龙江福和制药集团股份有限公司
3
CYHS2402000
琥珀酸亚铁片
安徽佳和药业有限公司
3
CYHS2401771
烟酸缓释片
北京世桥生物制药有限公司
3
CYHS2401697
琥珀酸亚铁片
北京斯利安药业有限公司
3
CYHS2401069
布美他尼注射液
山东致泰医药技术有限公司
3
CYHS2400453
氧(气态)
渭南市临渭区新永安医用氧有限责任公司
4
CYHS2502237
氧(液态)
石家庄陕鼓气体有限公司
4
CYHS2502148
氧
韩城市红光制气有限责任公司
4
CYHS2502024
美阿沙坦钾片
浙江高跖医药科技股份有限公司
4
CYHS2500510
美阿沙坦钾片
浙江高跖医药科技股份有限公司
4
CYHS2500509
ω-3脂肪酸乙酯90软胶囊
山西鑫煜制药股份有限公司
4
CYHS2500369
硫酸氢氯吡格雷片
华泰民康(沈阳)科技有限公司
4
CYHS2500311
利格列汀片
湖南千金协力药业有限公司
4
CYHS2500147
黄体酮软胶囊
株洲千金药业股份有限公司
4
CYHS2500097
黄体酮软胶囊
株洲千金药业股份有限公司
4
CYHS2500096
地屈孕酮片
嘉亨(珠海横琴)医药科技有限公司
4
CYHS2500043
氟伐他汀钠缓释片
浙江华海药业股份有限公司
4
CYHS2404664
地屈孕酮片
北京金城泰尔制药有限公司
4
CYHS2404601
枸橼酸氢钾钠颗粒
成都恒瑞制药有限公司
4
CYHS2404449
阿托伐他汀钙片
浙江江北药业有限公司
4
CYHS2404380
阿托伐他汀钙片
浙江江北药业有限公司
4
CYHS2404379
盐酸氨溴索口服溶液
合肥创新医药技术有限公司
4
CYHS2404232
盐酸氨溴索口服溶液
合肥创新医药技术有限公司
4
CYHS2404231
盐酸氨溴索口服溶液
合肥创新医药技术有限公司
4
CYHS2404230
盐酸氨溴索口服溶液
合肥创新医药技术有限公司
4
CYHS2404229
枸橼酸西地那非片
河北常山生化药业股份有限公司
4
CYHS2404130
枸橼酸西地那非片
河北常山生化药业股份有限公司
4
CYHS2404129
注射用阿奇霉素
南京海纳医药科技股份有限公司
4
CYHS2403967
盐酸氨溴索口服溶液
石药集团中诺药业(石家庄)有限公司
4
CYHS2403954
盐酸氨溴索口服溶液
石药集团中诺药业(石家庄)有限公司
4
CYHS2403953
乌帕替尼缓释片
江苏华阳制药有限公司
4
CYHS2403925
注射用头孢他啶/氯化钠注射液
北京锐业制药(潜山)有限公司
4
CYHS2403850
注射用头孢他啶/氯化钠注射液
北京锐业制药(潜山)有限公司
4
CYHS2403849
米力农注射液
云南药科院生物医药股份有限公司
4
CYHS2403835
吡美莫司乳膏
浙江华海药业股份有限公司
4
CYHS2403786
非那雄胺片
海南药谷云生物科技有限公司
4
CYHS2403791
非那雄胺片
海南药谷云生物科技有限公司
4
CYHS2403790
注射用盐酸地尔硫䓬
石家庄四药有限公司
4
CYHS2403777
阿法骨化醇软胶囊
人福普克药业(武汉)有限公司
4
CYHS2403728
阿法骨化醇软胶囊
人福普克药业(武汉)有限公司
4
CYHS2403727
卡前列素氨丁三醇注射液(预充式)
湖州亚瑟制药有限公司
4
CYHS2403675
复方托吡卡胺滴眼液
深圳市瑞霖医药有限公司
4
CYHS2403681
兰索拉唑肠溶胶囊
成都欣捷高新技术开发股份有限公司
4
CYHS2403547
他克莫司缓释胶囊
上海安必生制药技术有限公司
4
CYHS2403522
他克莫司缓释胶囊
上海安必生制药技术有限公司
4
CYHS2403521
氨甲环酸片
浙江兄弟药业有限公司
4
CYHS2403465
熊去氧胆酸胶囊
葵花药业集团(唐山)生物制药有限公司
4
CYHS2403427
奥卡西平口服混悬液
贵州科伦药业有限公司
4
CYHS2403387
达格列净二甲双胍缓释片(III)
辰欣药业股份有限公司
4
CYHS2403410
达格列净二甲双胍缓释片(I)
辰欣药业股份有限公司
4
CYHS2403409
盐酸屈他维林注射液
福州基石医药科技有限公司
4
CYHS2403341
盐酸莫西沙星氯化钠注射液
辽宁民康制药有限公司
4
CYHS2403230
恩他卡朋双多巴片(II)
四川科伦药业股份有限公司
4
CYHS2403149
盐酸屈他维林注射液
浙江高跖医药科技股份有限公司
4
CYHS2403087
玻璃酸钠滴眼液
黑龙江省知润药业有限公司
4
CYHS2402940
比拉斯汀片
安徽泰恩康制药有限公司
4
CYHS2402936
美沙拉秦肠溶片
浙江美迪深生物医药有限公司
4
CYHS2402885
骨化三醇注射液
桂林朗科制药有限公司
4
CYHS2402855
乳果糖口服溶液
河南合智医药科技有限公司
4
CYHS2402770
二甲双胍恩格列净片(I)
上海现代制药股份有限公司
4
CYHS2402748
盐酸乙哌立松片
上海安必生制药技术有限公司
4
CYHS2402671
盐酸氮卓斯汀鼻喷雾剂
广州市桐晖药业有限公司
4
CYHS2402515
盐酸阿莫罗芬搽剂
浙江恒研医药科技有限公司
4
CYHS2401938
罗沙司他胶囊
安徽省先锋制药有限公司
4
CYHS2401907
罗沙司他胶囊
安徽省先锋制药有限公司
4
CYHS2401906
甲硝唑凝胶
浙江寰领医药科技有限公司
4
CYHS2401398
沙库巴曲缬沙坦钠
华北制药华胜有限公司
CYHS2360504
醋酸地非法林注射液
成都青山利康药业股份有限公司
3
CYHL2600022
进口申请
药品名称
企业
注册分类
受理号
亚甲蓝注射液
Provepharm SAS
5.1
JXHS2500006
亚甲蓝注射液
Provepharm SAS
5.1
JXHS2500005
枸橼酸铁胶囊
PANION & BF BIOTECH INC.
5.1
JXHS2300078
注射用A型肉毒毒素
AbbVie Limited
3.1
JXSS2500098
注射用A型肉毒毒素
AbbVie Limited
3.1
JXSS2500097
注射用A型肉毒毒素
AbbVie Limited
3.1
JXSS2500096
度伐利尤单抗注射液
AstraZeneca UK Limited
3.1
JXSS2500028
度伐利尤单抗注射液
AstraZeneca UK Limited
3.1
JXSS2500027
度伐利尤单抗注射液
AstraZeneca UK Limited
3.1
JXSS2500014
度伐利尤单抗注射液
AstraZeneca UK Limited
3.1
JXSS2500013
Tremelimumab注射液
AstraZeneca AB
3.1
JXSS2500016
Tremelimumab注射液
AstraZeneca AB
3.1
JXSS2500015
盐酸头孢卡品酯颗粒
Yungjin Pharm Co., Ltd.
5.2
JYHS2400039
Nemtabrutinib片
Merck Sharp & Dohme LLC, a subsidiary of Merck & Co., Inc.
1
JXHL2600063
Nemtabrutinib片
Merck Sharp & Dohme LLC, a subsidiary of Merck & Co., Inc.
1
JXHL2600062
Nemtabrutinib片
Merck Sharp & Dohme LLC, a subsidiary of Merck & Co., Inc.
1
JXHL2600061
Brenipatide注射液
Eli Lilly and Company
1
JXHL2600048
TAK-360片
Takeda Development Center Americas, Inc.
1
JXHL2600042
TAK-360片
Takeda Development Center Americas, Inc.
1
JXHL2600041
TAK-360片
Takeda Development Center Americas, Inc.
1
JXHL2600040
TAK-360片
Takeda Development Center Americas, Inc.
1
JXHL2600039
TAK-360片
Takeda Development Center Americas, Inc.
1
JXHL2600038
BIIB115注射液
Biogen Idec Research Limited
1
JXHL2600036
依普隆特生钠注射液
AstraZeneca AB
2.4
JXHL2600033
盐酸艾司氯胺酮鼻喷雾剂
Janssen-Cilag International NV
5.1
JXHL2600030
AZD0486
AstraZeneca AB
1
JXSL2600054
AZD0486
AstraZeneca AB
1
JXSL2600053
PF-08634404
Pfizer Inc.
1
JXSL2600049
PF-08634404
Pfizer Inc.
1
JXSL2600048
Pegozafermin注射液
89bio, Inc.
1
JXSL2600052
Pegozafermin注射液
89bio, Inc.
1
JXSL2600051
JNJ-79635322
Janssen Research & Development, LLC
1
JXSL2600041
JNJ-79635322
Janssen Research & Development, LLC
1
JXSL2600040
JNJ-79635322
Janssen Research & Development, LLC
1
JXSL2600038
JNJ-79635322
Janssen Research & Development, LLC
1
JXSL2600039
Nipocalimab注射液
Janssen Research & Development, LLC
2.1
JXSL2600047
Nipocalimab注射液
Janssen Research & Development, LLC
2.1
JXSL2600046
中药相关申请
药品名称
企业
注册分类
受理号
芦荟多糖提取物
广州市东源药业科技有限公司
1.2
CXZL2600016
芦荟多糖乳膏
广州市东源药业科技有限公司
1.2
CXZL2600015
西帕依麦孜彼子口服液
新奇康药业股份有限公司
2.3
CXZL2600022
注:橙色字体部分结论为不批准或收到通知件;
疫苗上市批准高管变更
2026-04-27
1、研究机构:赛诺菲制药、健赞生物制药、Principia Biopharma
2、别名:PRN-2246、SAR-442168、Cenrifki、托莱布替尼
3、靶点:BTK
4、剂型及给药途径:普通片剂; 口服给药
5、结构式
6、适应症及进展
适应症
进展
最新进展日期
多发性硬化
申请上市
2026-03-07
2026-03-07
I期
2025-02-07
7、发表论文
标题
内容类型
适应症
企业
技术平台
来源
发表日期
BTK regulates microglial function and neuroinflammation in human stem cell models and mouse models of multiple sclerosis
药理研究
多发性硬化
赛诺菲制药
武田药品工业株式会社
Voyager Therapeutics
Nat Commun
IF=15.7
2024-11-22
8、交易
交易名称
交易类型
转让方
受让方
交易时研发状态
权益类型
权益地区
权益适应症
交易金额
交易时间
Sanofi completes Principia Biopharma Inc. acquisition收购完成
转让/收购
Principia Biopharma
赛诺菲制药
临床III期
开发/商业化权
交易总额:3680百万美元
2020-09-28
Sanofi to acquire Principia Biopharma
转让/收购
Principia Biopharma
赛诺菲制药
临床III期
开发/商业化权
交易总额:3680百万美元
2020-08-17
Bay Area's Principia Biopharma Scores $765M MS Licensing Deal With Drug Giant Sanofi
授权/许可
Principia Biopharma
赛诺菲制药
临床II期
开发/商业化权
交易总额:765百万美元首付款:40百万美元
2017-11-09
9、专利布局
公开(公告)号
专利主题
发明名称
申请日
法律状态
CN106459049B
化合物
酪氨酸激酶抑制剂
2016-06-02
CN118434732A
晶型
Tolebrutinib的晶型及其制备方法和用途
2021-11-22
实质审查
CN117897381A
晶型
Tolebrutinib的晶型及其制备方法和用途
2022-06-02
实质审查
CN118434734A
晶型
(R)-1-(1-丙烯酰基哌啶-3-基)-4-氨基-3-(4-苯氧基苯基)-1H-咪唑并[4,5-C]吡啶-2(3H)-酮及其盐的晶型
2022-12-20
实质审查
CN119212708A
用途
用于髓鞘少突胶质细胞糖蛋白抗体疾病(MOGAD)的治疗性酪氨酸激酶抑制剂
2023-05-12
实质审查
CN119384411A
制备工艺
制备托勒替尼的方法
2023-06-13
实质审查
CN119343340A
制备工艺
制备修饰的BTK抑制剂的方法
2023-06-21
实质审查
CN119421712A
用途
用于多发性硬化和重症肌无力的治疗性酪氨酸激酶抑制剂
2023-06-29
实质审查
CN120435291A
用途
用于多发性硬化的治疗性酪氨酸激酶抑制剂
2023-10-06
实质审查
CN120379652A
制剂
(R)-1-(1-丙烯酰基哌啶-3-基)-4-氨基-3-(4-苯氧基苯基)-1H-咪唑并[4,5-c]吡啶-2(3H)-酮的药物制剂
2023-12-19
实质审查
CN121620370A
用途
通过检测脑脊液中的生物标志物诊断和治疗多发性硬化的方法
2024-01-31
实质审查
10、研究历程
2025年02月01日,由赛诺菲向美国食品药品管理局FDA提交上市申请,用于治疗慢性进行性多发性硬化。(https://www.sanofi.com/en/our-science/our-pipeline)
2024年05月20日,由Sanofi Winthrop Industrie SA在中国香港和中国大陆开展临床三期试验,用于治疗多发性硬化。(CTR20240417)
2024年04月16日,由赛诺菲(中国)投资有限公司、Sanofi Winthrop Industrie SA、Sanofi-Aventis Recherche & Developpement和赛诺菲在澳大利亚、加拿大和智利等国家和地区开展临床三期试验,用于治疗多发性硬化和慢性进行性多发性硬化。(CTR20240417; NCT06372145)
2023年03月10日,治疗重症肌无力的研究终止。(NCT05132569)
2022年12月14日,治疗重症肌无力的研究终止。(CTR20220329)
2022年06月22日,由赛诺菲(中国)投资有限公司、Sanofi Winthrop Industrie SA和Sanofi-Aventis Recherche & Developpement在中国大陆开展临床三期试验,用于治疗重症肌无力。(CTR20220329)
2022年03月10日,由赛诺菲在德国和美国开展临床一期试验,用于治疗肾功能不全。(NCT05282030)
2021年12月20日,由赛诺菲(中国)投资有限公司、Sanofi Winthrop Industrie SA和Sanofi-Aventis Recherche & Developpement在巴西、加拿大和德国等国家和地区开展临床三期试验,用于治疗重症肌无力。(CTR20220329)
2021年12月03日,由赛诺菲在加拿大、匈牙利和意大利等国家和地区开展临床三期试验,用于治疗重症肌无力。(NCT05132569)
2021年11月03日,由Koneksa Health Inc开展临床前研究试验。(https://www.prnewswire.com/news-releases/koneksa-broadens-multi-year-cns-research-collaboration-with-sanofi-301415238.html)
2021年04月15日,由National Institute Of Neurological Disorders And Stroke在美国开展临床二期试验,用于治疗多发性硬化。(NCT04742400)
2021年02月23日,由赛诺菲(中国)投资有限公司、Sanofi-Aventis Recherche & Developpement和美国健赞公司在中国香港、中国台湾和中国大陆等国家和地区开展临床三期试验,用于治疗多发性硬化。(CTR20240417; CTR20210060; CTR20202631; CTR20210121)
2020年10月23日,由赛诺菲(中国)投资有限公司、Sanofi-Aventis Recherche & Developpement和美国健赞公司在奥地利、白俄罗斯和保加利亚等国家和地区开展临床三期试验,用于治疗多发性硬化。(CTR20240417; CTR20210060)
2020年08月13日,由赛诺菲在阿根廷、澳大利亚和奥地利等国家和地区开展临床三期试验,用于治疗慢性进行性多发性硬化。(NCT04458051; NCT06372145)
2020年06月30日,由赛诺菲在奥地利、白俄罗斯和保加利亚等国家和地区开展临床三期试验,用于治疗多发性硬化。(NCT06372145; NCT04410978)
2020年06月11日,由赛诺菲在阿根廷、比利时和巴西等国家和地区开展临床三期试验,用于治疗多发性硬化。(NCT06372145; NCT04410978; NCT04410991)
2020年05月18日,由赛诺菲在美国开展临床一期试验,用于治疗多发性硬化。(NCT06106074; NCT06064539)
2019年11月13日,由赛诺菲在英国开展临床一期试验,用于治疗多发性硬化。(NCT04171310)
2019年03月29日,由赛诺菲在加拿大、爱沙尼亚和法国等国家和地区开展临床二期试验,用于治疗多发性硬化。(NCT03996291; NCT03889639)
11、临床试验
登记号
试验标题
试验药
适应症
原始适应症
申办/合作机构
试验状态
试验分期
开始日期
完成日期
国家/地区
NCT07526597
Study on Treatment Outcome Patterns for Patients With CLL After Discontinuation of BTK Inhibitors
托莱布替尼
慢性淋巴细胞白血病 | 小淋巴细胞淋巴瘤
Chronic Lymphocytic Leukemia | Small Lymphocytic Lymphoma
Lineberger Comprehensive Cancer Center
Not yet recruiting
临床2期
2026-05-01
2032-06-01
美国
NCT07120633
The Efficacy of AntiCD19 CAR-T Combined With BTKi in the Treatment of Newly Diagnosed High-risk CLL Patients, and to Explore Its Efficacy and Safety of Limited-term Treatment in These Patients
Anti-CD19 CAR-T (The Affiliated Hospital of Xuzhou Medical University) | 托莱布替尼
慢性淋巴细胞白血病 | 小淋巴细胞淋巴瘤
CLL | CAR-T Cell Therapy | SLL
徐州医科大学附属医院
Recruiting
N/A
2025-09-01
2028-09-01
中国
NCT06372145
An Interventional, Phase 3 Extension Study to Investigate Long-term Safety and Tolerability of Tolebrutinib in Participants With Relapsing Multiple Sclerosis, Primary Progressive Multiple Sclerosis, or Nonrelapsing Secondary Progressive Multiple Sclerosis
托莱布替尼 (片剂, 口服)
原发性进行性多发性硬化 | 继发进展型多发性硬化 | 复发性多发性硬化
Relapsing Multiple Sclerosis | Secondary Progressive Multiple Sclerosis | Progressive Relapsing Multiple Sclerosis
Sanofi
Active, not recruiting
临床3期
2024-04-16
2029-04-30
美国 | 中国香港 | 捷克 | 泰国 | 葡萄牙 | 希腊 | 瑞典 | 韩国 | 荷兰 | 拉脱维亚 | 奥地利 | 中国 | 土耳其 | 波兰 | 巴西 | 斯洛伐克 | 塞尔维亚共和国 | 立陶宛 | 法国 | 智利 | 保加利亚 | 克罗地亚 | 哥伦比亚 | 阿根廷 | 罗马尼亚 | 匈牙利 | 日本 | 乌克兰 | 英国 | 瑞士 | 西班牙 | 印度 | 加拿大 | 比利时 | 挪威 | 中国台湾 | 芬兰 | 丹麦 | 南非 | 墨西哥 | 意大利 | 以色列 | 澳大利亚 | 德国 | 爱沙尼亚
NCT06106074
A Randomized, Double-blind, Placebo-controlled Study of the Tolerability and Pharmacokinetics of Ascending Single and 14-day Repeated Oral Doses of SAR442168 With a Food Effect Investigation in Healthy Adult Participants
托莱布替尼 (片剂, 口服)
多发性硬化症
Multiple Sclerosis
Sanofi
Completed
临床1期
2020-08-10
2022-05-23
美国
NCT06064539
A Phase 1, Single-center, Open-label, Two-cohort, Two-period, One-sequence, Two Treatment, Drug-drug Interaction Study of the Effects of Gemfibrozil and Rifampicin on SAR442168 in Healthy Subjects
吉非罗齐 (片剂, 口服) | 利福平 (片剂, 口服) | 托莱布替尼 (片剂, 口服)
多发性硬化症
Multiple Sclerosis
Sanofi
Completed
临床1期
2020-05-18
2020-07-08
美国
NCT05283915
An Open-label Phase 1, Pharmacokinetic and Tolerability Study of Tolebrutinib Given as a Single Dose in Adult Participants With Mild Hepatic Impairment, and in Matched Participants With Normal Hepatic Function
托莱布替尼 (薄膜包衣片, 口服)
肝功能不全
Hepatic Function Abnormal
Sanofi
Completed
临床1期
2022-03-18
2022-05-24
美国
NCT05282030
An Open-label, Multi-center Phase 1 Pharmacokinetic and Tolerability Study of Tolebrutinib Given as a Single Oral Dose in Participants With Renal Impairment and in Matched Participants With Normal Renal Function.
托莱布替尼 (薄膜包衣片, 口服)
肾功能不全
Renal Impairment
Sanofi
Completed
临床1期
2022-03-10
2022-08-02
美国 | 德国
ChiCTR2200055554
An Open, Single-Center Clinical Observation Study to Assess the Efficacy and Safety of The Thiotepa for Primary Central Nervous System Lymphoma (PCNSL) Patients
卡莫司汀 | 托莱布替尼 | 甲氨蝶呤 | 利妥昔单抗 | 塞替派
原发性中枢神经系统淋巴瘤
Primary central nervous system lymphoma/Central?high?risk?of?diffuse?large?B-cell?lymphoma
兰州大学第二医院
Recruiting
临床2期
2022-04-01
2024-04-04
中国
NCT05132569
A Phase 3, Randomized, Double-blind, Placebo-controlled, Parallel-group Study to Evaluate the Efficacy and Safety of Tolebrutinib (SAR442168) in Adults With Generalized Myasthenia Gravis (MG)
托莱布替尼 (薄膜包衣片, 口服)
重症肌无力
Myasthenia Gravis
Sanofi
Terminated
临床3期
2021-12-03
2023-02-21
加拿大 | 匈牙利 | 美国 | 日本 | 中国 | 波兰 | 英国 | 意大利 | 西班牙
NCT04978779
An Open-label, Multicenter Phase 1/1b Study to Characterize Safety, Tolerability, Preliminary Antitumor Activity, Pharmacokinetics, and Pharmacodynamics of VIP152 Monotherapy or Combination Therapy in Subjects With High-risk Chronic Lymphocytic Leukemia or Richter Syndrome
Enitociclib (静脉注射) | 托莱布替尼
染色体易位 | 复发性非霍奇金淋巴瘤 | 难治性慢性淋巴细胞白血病 | 里氏综合症
Relapsed Non Hodgkin Lymphoma | Chronic Lymphocytic Leukemia | Refractory Chronic Lymphocytic Leukemia | Richter Syndrome | MYC Amplification | MYC Overexpression | MYC Translocation
Vincerx Pharma, Inc.
Terminated
临床1期
2021-12-16
2023-05-26
美国 | 波兰
NCT04742400
A Phase 2 Clinical Trial of Tolebrutinib, a Brain-penetrant Bruton's Tyrosine Kinase Inhibitor, for the Modulation of Chronically Inflamed White Matter Lesions in Multiple Sclerosis
托莱布替尼 (口服)
多发性硬化症
Multiple Sclerosis
National Institute of Neurological Disorders & Stroke
Active, not recruiting
临床2期
2021-04-15
2025-12-31
美国
NCT04458051
A Phase 3, Randomized, Double-blind, Efficacy and Safety Study Comparing SAR442168 to Placebo in Participants With Primary Progressive Multiple Sclerosis (PERSEUS)
托莱布替尼 (薄膜包衣片, 口服)
原发性进行性多发性硬化
Primary Progressive Multiple Sclerosis
Sanofi
Completed
临床3期
2020-08-13
2025-11-14
捷克 | 美国 | 泰国 | 葡萄牙 | 俄罗斯 | 希腊 | 瑞典 | 荷兰 | 拉脱维亚 | 奥地利 | 中国 | 土耳其 | 波兰 | 巴西 | 塞尔维亚共和国 | 法国 | 智利 | 保加利亚 | 克罗地亚 | 哥伦比亚 | 阿根廷 | 罗马尼亚 | 匈牙利 | 日本 | 乌克兰 | 英国 | 白俄罗斯 | 西班牙 | 印度 | 加拿大 | 比利时 | 挪威 | 丹麦 | 南非 | 墨西哥 | 意大利 | 以色列 | 澳大利亚 | 秘鲁 | 德国 | 爱沙尼亚
NCT04411641
A Phase 3, Randomized, Double-blind, Efficacy and Safety Study Comparing SAR442168 to Placebo in Participants With Nonrelapsing Secondary Progressive Multiple Sclerosis
托莱布替尼 (薄膜包衣片, 口服)
继发进展型多发性硬化
Non-relapsing Secondary Progressive Multiple Sclerosis
Sanofi
Completed
临床3期
2020-09-24
2024-08-29
俄罗斯 | 捷克 | 美国 | 葡萄牙 | 希腊 | 荷兰 | 奥地利 | 中国 | 波兰 | 立陶宛 | 法国 | 保加利亚 | 阿根廷 | 罗马尼亚 | 匈牙利 | 日本 | 乌克兰 | 英国 | 白俄罗斯 | 西班牙 | 印度 | 加拿大 | 土耳其 | 比利时 | 挪威 | 芬兰 | 丹麦 | 意大利 | 以色列 | 澳大利亚 | 德国
NCT04410978
A Phase 3, Randomized, Double-blind Efficacy and Safety Study Comparing SAR442168 to Teriflunomide (Aubagio®) in Participants With Relapsing Forms of Multiple Sclerosis
托莱布替尼 (片剂, 口服)
复发性多发性硬化
Relapsing Multiple Sclerosis
Sanofi
Completed
临床3期
2020-06-30
2024-07-15
俄罗斯 | 罗马尼亚 | 中国香港 | 捷克 | 美国 | 日本 | 乌克兰 | 白俄罗斯 | 西班牙 | 加拿大 | 瑞典 | 奥地利 | 土耳其 | 中国 | 中国台湾 | 芬兰 | 波兰 | 丹麦 | 墨西哥 | 意大利 | 立陶宛 | 保加利亚 | 德国 | 爱沙尼亚
NCT04171310
An Open-label Study of Excretion Balance and Pharmacokinetics Following a Single Oral Dose of [14C]-SAR442168 (Not More Than 3.7 MBq) in Healthy Male Subjects
托莱布替尼
多发性硬化症
Multiple Sclerosis
Sanofi
Completed
临床1期
2019-11-13
2019-12-30
英国
KCT0004309
A Phase 1, single-center, randomized, double-blind, placebo-controlled, incomplete block, 3-period crossover, single-dose escalation study to determine the safety, tolerability and pharmacokinetics of orally administered SAR442168 tablet in healthy East Asian (Japanese / Chinese / Korean) male subjects
托莱布替尼
神经系统疾病
Diseases of the nervous system
Sanofi-Aventis Korea Co., Ltd.
Completed
临床1期
2019-08-13
-
韩国
NCT03996291
Long-term Extension Safety and Efficacy Study of SAR442168 in Participants With Relapsing Multiple Sclerosis
托莱布替尼
复发性多发性硬化
Relapsing Multiple Sclerosis
Sanofi
Completed
临床2期
2019-09-23
2024-11-26
加拿大 | 荷兰 | 捷克 | 美国 | 乌克兰 | 法国 | 西班牙 | 俄罗斯 | 爱沙尼亚
NCT03889639
A Phase 2b Dose-finding Study for SAR442168, a Bruton's Tyrosine Kinase Inhibitor, in Participants With Relapsing Multiple Sclerosis
托莱布替尼
复发性多发性硬化
Relapsing Multiple Sclerosis
Sanofi
Completed
临床2期
2019-03-29
2020-01-02
加拿大 | 荷兰 | 捷克 | 美国 | 乌克兰 | 斯洛伐克 | 法国 | 西班牙 | 俄罗斯 | 爱沙尼亚
ACTRN12618001523291
A Phase 1, Randomized, Open-Label Study of the Relative Bioavailability and Effect of Food on the Pharmacokinetics of a Novel Formulation of PRN2246 Compared to a Reference Formulation in Healthy Adult Participants
托莱布替尼
多发性硬化症 | 神经系统疾病
Immune-mediated neurologic disorders | Immune-mediated neurologic disorders | Neurological - Multiple sclerosis
Clinical Network Services Pty Ltd.
Completed
临床1期
2018-10-14
2018-11-09
澳大利亚
ACTRN12617001457336
A Phase I, Randomized, Double-Blind, Placebo-Controlled, Ascending Dose Study to Assess the Safety, Tolerability and Pharmacokinetics of Orally Administered PRN2246 in Healthy Volunteers
托莱布替尼
神经系统疾病
Immune-mediated neurologic disorders
Clinical Network Services Pty Ltd.
Recruiting
临床1期
2017-10-17
-
-
12、临床结果
标题
登记号
来源
分期
适应症
评价人数
用药方案
结果
评价
发布日期
申办/合作机构
主要研究药物
来源链接
Synapse链接
TP53 aberrant Mantle Cell Lymphoma treated with first-line systemic therapy: A real-world analysis of outcomes in 120 patients treated in the United Kingdom
-
ASH
N/A
套细胞淋巴瘤
120
High intensity ICT (rituximab + high dose cytarabine based)
CR = 45.0 %
不佳
2025-12-06
University Hospital Southampton NHS Foundation Trust | Barts Health NHS Trust | Blackpool Teaching Hospitals NHS Foundation Trust | South Tees Hospitals NHS Foundation Trust | Nottingham University Hospitals Nhs Trust | University College London Hospitals NHS Foundation Trust
-
https://meetings-api.hematology.org/api/abstract/vmpreview/300472
https://synapse.zhihuiya.com/clinical-result-detail/82ed9a2825328852205ea4ee592a5358
TP53 aberrant Mantle Cell Lymphoma treated with first-line systemic therapy: A real-world analysis of outcomes in 120 patients treated in the United Kingdom
-
ASH
N/A
套细胞淋巴瘤
120
Intermediate intensity ICT (R-CHOP/R- Bendamustine/R-BAC/VR-CAP)
FFS(1st line) = 8.9 Month ( 3.8 ~ 14.0)
不佳
2025-12-06
University Hospital Southampton NHS Foundation Trust | Barts Health NHS Trust | Blackpool Teaching Hospitals NHS Foundation Trust | South Tees Hospitals NHS Foundation Trust | Nottingham University Hospitals Nhs Trust | University College London Hospitals NHS Foundation Trust
-
https://meetings-api.hematology.org/api/abstract/vmpreview/300472
https://synapse.zhihuiya.com/clinical-result-detail/82ed9a2825328852205ea4ee592a5358
Real-world outcomes of younger patients with chronic lymphocytic leukemia treated with first-line BTK inhibitor or BCL2 inhibitor therapy
-
ASH
N/A
慢性淋巴细胞白血病
426
BTKi (ibrutinib, acalabrutinib, or zanubrutinib)
mDoT = 20.7 Month
积极
2025-12-06
University of Utah Spencer Fox Eccles School of Medicine
-
https://meetings-api.hematology.org/api/abstract/vmpreview/300991
https://synapse.zhihuiya.com/clinical-result-detail/a335842a820a8a504d2a223a038ea2e2
Real-world outcomes of younger patients with chronic lymphocytic leukemia treated with first-line BTK inhibitor or BCL2 inhibitor therapy
-
ASH
N/A
慢性淋巴细胞白血病
426
BCL2i (venetoclax ± rituximab or obinutuzumab)
mDoT = 11.9 Month
积极
2025-12-06
University of Utah Spencer Fox Eccles School of Medicine
-
https://meetings-api.hematology.org/api/abstract/vmpreview/300991
https://synapse.zhihuiya.com/clinical-result-detail/a335842a820a8a504d2a223a038ea2e2
Outcomes of patients with Richter transformation (RT) treated with frontline chemoimmunotherapy (CIT) and BTK inhibitor (BTKi)
-
ASH
N/A
里氏综合症
56
CIT+BTKi
ORR = 62.5 %
积极
2025-12-06
University of California
-
https://meetings-api.hematology.org/api/abstract/vmpreview/291372
https://synapse.zhihuiya.com/clinical-result-detail/a25243a9e42aee422543ad5522aa24d3
Outcomes of patients with Richter transformation (RT) treated with frontline chemoimmunotherapy (CIT) and BTK inhibitor (BTKi)
-
ASH
N/A
里氏综合症
56
CIT-only
CR = 58.3 %
积极
2025-12-06
University of California
-
https://meetings-api.hematology.org/api/abstract/vmpreview/291372
https://synapse.zhihuiya.com/clinical-result-detail/a25243a9e42aee422543ad5522aa24d3
Upfront continuous BTK inhibitor (BTKi) versus time-limited venetoclax-BTKi combinations in CLL across IGHV subgroups: Results of an indirect analysis
-
ASH
N/A
慢性淋巴细胞白血病
2037
continuous BTKi therapy
PFS(four-year): Δ = 0.5(95.0% CI, -4.8 ~ 5.8), P-Value = 0.85
积极
2025-12-06
-
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/291473
https://synapse.zhihuiya.com/clinical-result-detail/00482ea9a5ae42545259ea22de2249e5
Upfront continuous BTK inhibitor (BTKi) versus time-limited venetoclax-BTKi combinations in CLL across IGHV subgroups: Results of an indirect analysis
-
ASH
N/A
慢性淋巴细胞白血病
2037
TL venetoclax-BTKi regimens
PFS(four-year): Δ = 0.5(95.0% CI, -4.8 ~ 5.8), P-Value = 0.85
积极
2025-12-06
-
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/291473
https://synapse.zhihuiya.com/clinical-result-detail/00482ea9a5ae42545259ea22de2249e5
Comparison of infections in patients with chronic lymphocytic leukemia (CLL) treated with BTKi versus venetoclax obinutuzumab in first line therapy
-
ASH
N/A
慢性淋巴细胞白血病
3178
BTKi (ibrutinib, zanubrutinib, or acalabrutinib)
菌血症 = 8.1 %
不佳
2025-12-06
Roswell Park Comprehensive Cancer Center
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/290555
https://synapse.zhihuiya.com/clinical-result-detail/59525e99a0325ad52ad42ed5382a22aa
Comparison of infections in patients with chronic lymphocytic leukemia (CLL) treated with BTKi versus venetoclax obinutuzumab in first line therapy
-
ASH
N/A
慢性淋巴细胞白血病
3178
VenObin (venetoclax & obinutuzumab)
菌血症 = 4.8 %
不佳
2025-12-06
Roswell Park Comprehensive Cancer Center
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/290555
https://synapse.zhihuiya.com/clinical-result-detail/59525e99a0325ad52ad42ed5382a22aa
Characteristics, treatment outcomes, and prognostic analysis of 118 cases of lymphoplasmacytic lymphoma/Waldenström macroglobulinemia
-
ASH
N/A
淋巴浆细胞性淋巴瘤 | 巨球蛋白血症
101
BTKi (Bruton Tyrosine kinase inhibitor, Ibrutinib 140mg QD, or Zanubrutinib 160mg BID)
CRR = 100.0 %
积极
2025-12-06
-
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/302249
https://synapse.zhihuiya.com/clinical-result-detail/e82a5e2894a082a8408a8e89ade32804
Characteristics, treatment outcomes, and prognostic analysis of 118 cases of lymphoplasmacytic lymphoma/Waldenström macroglobulinemia
-
ASH
N/A
淋巴浆细胞性淋巴瘤 | 巨球蛋白血症
101
VD (Bortezomib 1.3mg/m2,d1,8,15, Dexamethasone, 20mg, d1,2,8,9,15,16,22,23)
mOS = NR
积极
2025-12-06
-
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/302249
https://synapse.zhihuiya.com/clinical-result-detail/e82a5e2894a082a8408a8e89ade32804
Progression of disease within 36 months (POD36) of starting first-line targeted therapy independently predicts poor overall survival in patients with chronic lymphocytic leukemia (CLL)
-
ASH
N/A
慢性淋巴细胞白血病
787
BTKi +/- CD20mAb
mOS = not reached
积极
2025-12-06
Mayo Clinic
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/292616
https://synapse.zhihuiya.com/clinical-result-detail/0a582a8e8e4e82d002a88403ea958e22
Progression of disease within 36 months (POD36) of starting first-line targeted therapy independently predicts poor overall survival in patients with chronic lymphocytic leukemia (CLL)
-
ASH
N/A
慢性淋巴细胞白血病
787
BCL2i + CD20mAb
mOS = not reached
积极
2025-12-06
Mayo Clinic
托莱布替尼
https://meetings-api.hematology.org/api/abstract/vmpreview/292616
https://synapse.zhihuiya.com/clinical-result-detail/0a582a8e8e4e82d002a88403ea958e22
Real-world comparison of treatment outcomes between BCL2i and 2nd generation BTKi therapy in first-line CLL patients
-
ASH
N/A
慢性淋巴细胞白血病
3844
Second-generation BTKi
Event-free probability(30-month) = 70.0 %
积极
2025-12-06
-
维奈克拉 | 奥妥珠单抗
https://meetings-api.hematology.org/api/abstract/vmpreview/297011
https://synapse.zhihuiya.com/clinical-result-detail/02e232eea4d0a32325242482e5588a3e
Real-world comparison of treatment outcomes between BCL2i and 2nd generation BTKi therapy in first-line CLL patients
-
ASH
N/A
慢性淋巴细胞白血病
3844
V+O
Event-free probability(30-month) = 83.0 %
积极
2025-12-06
-
维奈克拉 | 奥妥珠单抗
https://meetings-api.hematology.org/api/abstract/vmpreview/297011
https://synapse.zhihuiya.com/clinical-result-detail/02e232eea4d0a32325242482e5588a3e
A Phase 3, Randomized, Double-blind Efficacy and Safety Study Comparing SAR442168 to Teriflunomide (Aubagio®) in Participants With Relapsing Forms of Multiple Sclerosis
NCT04410978
CTgov
临床3期
复发性多发性硬化
974
Teriflunomide(Teriflunomide 14 mg)
Annualized Relapse Rate (ARR) as Assessed by Confirmed Protocol-defined Adjudicated Relapses = 0.122 relapses per participant year (95%CI, 0.100 ~ 0.150)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04410978
https://synapse.zhihuiya.com/clinical-result-detail/aa855a8320d22a542424eaa85889e239
A Phase 3, Randomized, Double-blind Efficacy and Safety Study Comparing SAR442168 to Teriflunomide (Aubagio®) in Participants With Relapsing Forms of Multiple Sclerosis
NCT04410978
CTgov
临床3期
复发性多发性硬化
974
Tolebrutinib(Tolebrutinib 60 mg)
Annualized Relapse Rate (ARR) as Assessed by Confirmed Protocol-defined Adjudicated Relapses = 0.130 relapses per participant year (95%CI, 0.108 ~ 0.156)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04410978
https://synapse.zhihuiya.com/clinical-result-detail/aa855a8320d22a542424eaa85889e239
A Phase 3, Randomized, Double-blind, Efficacy and Safety Study Comparing SAR442168 to Placebo in Participants With Nonrelapsing Secondary Progressive Multiple Sclerosis
NCT04411641
CTgov
临床3期
继发进展型多发性硬化
1131
placebo+tolebrutinib(DB: Placebo)
Time to Onset of 6-Month Confirmed Disability Progression (CDP) as Assessed by Expanded Disability Status Scale (EDSS)(Median) = 11.97 Month (Full Range, 0.5 ~ 39.1)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04411641
https://synapse.zhihuiya.com/clinical-result-detail/888e2aed428e888334e855ae28d4894e
A Phase 3, Randomized, Double-blind, Efficacy and Safety Study Comparing SAR442168 to Placebo in Participants With Nonrelapsing Secondary Progressive Multiple Sclerosis
NCT04411641
CTgov
临床3期
继发进展型多发性硬化
1131
Tolebrutinib(DB: Tolebrutinib 60 mg)
Time to Onset of 6-Month Confirmed Disability Progression (CDP) as Assessed by Expanded Disability Status Scale (EDSS)(Median) = 12.04 Month (Full Range, 2.8 ~ 37.4)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04411641
https://synapse.zhihuiya.com/clinical-result-detail/888e2aed428e888334e855ae28d4894e
A Phase 3, Randomized, Double-blind Efficacy and Safety Study Comparing SAR442168 to Teriflunomide (Aubagio®) in Participants With Relapsing Forms of Multiple Sclerosis
NCT04410991
CTgov
临床3期
复发性多发性硬化
899
Teriflunomide(Teriflunomide 14 mg)
Annualized Relapse Rate (ARR) as Assessed by Confirmed Protocol-defined Adjudicated Relapses = 0.109 relapses per participant year (95%CI, 0.088 ~ 0.134)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04410991
https://synapse.zhihuiya.com/clinical-result-detail/e23e3a42323d22a53223aa0422482855
A Phase 3, Randomized, Double-blind Efficacy and Safety Study Comparing SAR442168 to Teriflunomide (Aubagio®) in Participants With Relapsing Forms of Multiple Sclerosis
NCT04410991
CTgov
临床3期
复发性多发性硬化
899
Tolebrutinib(Tolebrutinib 60 mg)
Annualized Relapse Rate (ARR) as Assessed by Confirmed Protocol-defined Adjudicated Relapses = 0.108 relapses per participant year (95%CI, 0.089 ~ 0.131)
-
2025-06-18
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT04410991
https://synapse.zhihuiya.com/clinical-result-detail/e23e3a42323d22a53223aa0422482855
Tolebrutinib in Nonrelapsing Secondary Progressive Multiple Sclerosis
NCT04411641
Pubmed
临床3期
继发进展型多发性硬化
1131
Tolebrutinib 60 mg once daily
SAE = 15.0 %
积极
2025-05-15
Sanofi
托莱布替尼
https://pubmed.ncbi.nlm.nih.gov/40202696/ | https://doi.org/10.1056/nejmoa2415988
https://synapse.zhihuiya.com/clinical-result-detail/3e22028925a888a52224a2d5d5528253
Tolebrutinib in Nonrelapsing Secondary Progressive Multiple Sclerosis
NCT04411641
Pubmed
临床3期
继发进展型多发性硬化
1131
Placebo
SAE = 10.4 %
积极
2025-05-15
Sanofi
托莱布替尼
https://pubmed.ncbi.nlm.nih.gov/40202696/ | https://doi.org/10.1056/nejmoa2415988
https://synapse.zhihuiya.com/clinical-result-detail/3e22028925a888a52224a2d5d5528253
LONG-TERM OUTCOMES IN WALDENSTRÖM MACROGLOBULINEMIA (WM) PATIENTS WHO DISCONTINUE BRUTON'S TYROSINE KINASE INHIBITOR (BTKI) THERAPY
-
EHA
N/A
巨球蛋白血症
153
BTKi
Adverse Event: AE = AEs leading to therapy discontinuation were reported in 44% of patients who discontinued 1st BTKi therapy
-
2025-05-14
MD Anderson Cancer Center Orlando
-
https://library.ehaweb.org/eha/2025/eha2025-congress/4160964/karan.chohan.long-term.outcomes.in.waldenstrm.macroglobulinemia.28wm29.patients.html
https://synapse.zhihuiya.com/clinical-result-detail/208240a8e89254aa20a22ee38e22592e
LONG-TERM OUTCOMES IN WALDENSTRÖM MACROGLOBULINEMIA (WM) PATIENTS WHO DISCONTINUE BRUTON'S TYROSINE KINASE INHIBITOR (BTKI) THERAPY
-
EHA
N/A
巨球蛋白血症
153
Alternate BTKi-based regimen
Adverse Event: AE = AEs leading to therapy discontinuation were reported in 44% of patients who discontinued 1st BTKi therapy
-
2025-05-14
MD Anderson Cancer Center Orlando
-
https://library.ehaweb.org/eha/2025/eha2025-congress/4160964/karan.chohan.long-term.outcomes.in.waldenstrm.macroglobulinemia.28wm29.patients.html
https://synapse.zhihuiya.com/clinical-result-detail/208240a8e89254aa20a22ee38e22592e
Tolebrutinib versus Teriflunomide in Relapsing Multiple Sclerosis
NCT04410991 | NCT04410978
Pubmed
临床3期
复发性多发性硬化
-
Tolebrutinib 60 mg once dailyTolebrutinib 60 mg once dailyTolebrutinib 60 mg once daily
ARR(GEMINI 1) = 0.13 Unit
不佳
2025-04-08
Sanofi
托莱布替尼
https://pubmed.ncbi.nlm.nih.gov/40202623/ | https://doi.org/10.1056/nejmoa2415985
https://synapse.zhihuiya.com/clinical-result-detail/ee2e48dd088d98eee2e8e28590d2dd3a
Tolebrutinib versus Teriflunomide in Relapsing Multiple Sclerosis
NCT04410991 | NCT04410978
Pubmed
临床3期
复发性多发性硬化
-
Teriflunomide 14 mg once daily
ARR(GEMINI 1) = 0.12 Unit
不佳
2025-04-08
Sanofi
托莱布替尼
https://pubmed.ncbi.nlm.nih.gov/40202623/ | https://doi.org/10.1056/nejmoa2415985
https://synapse.zhihuiya.com/clinical-result-detail/ee2e48dd088d98eee2e8e28590d2dd3a
4392Clinical Outcomes of Lymphoplasmacytic Lymphoma / Waldenstrom Macroglobulinemia (LPL/WM) in the Targeted Therapy Era: A US Multicenter Retrospective Analysis
-
ASH
N/A
淋巴浆细胞性淋巴瘤 | 巨球蛋白血症
-
Chemo-immunotherapy (CIT)
ORR = 68 %
-
2024-12-09
University of Arkansas for Medical Sciences | The Ohio State University | Hematology/Oncology Associates of Central New York PC | Taussig Cancer Institute | H. Lee Moffitt Cancer Center & Research Institute, Inc. | The Fox Chase Cancer Center | Roswell Park Comprehensive Cancer Center
-
https://ash.confex.com/ash/2024/webprogram/Paper199278.html
https://synapse.zhihuiya.com/clinical-result-detail/e95288a9eeee22482e8d2ee54345ea54
4392Clinical Outcomes of Lymphoplasmacytic Lymphoma / Waldenstrom Macroglobulinemia (LPL/WM) in the Targeted Therapy Era: A US Multicenter Retrospective Analysis
-
ASH
N/A
淋巴浆细胞性淋巴瘤 | 巨球蛋白血症
-
Rituximab (R)
ORR = 34 %
-
2024-12-09
University of Arkansas for Medical Sciences | The Ohio State University | Hematology/Oncology Associates of Central New York PC | Taussig Cancer Institute | H. Lee Moffitt Cancer Center & Research Institute, Inc. | The Fox Chase Cancer Center | Roswell Park Comprehensive Cancer Center
-
https://ash.confex.com/ash/2024/webprogram/Paper199278.html
https://synapse.zhihuiya.com/clinical-result-detail/e95288a9eeee22482e8d2ee54345ea54
5109Real-World Risk of Major Bleeding Events in BTKi-Treated Patients with Chronic Lymphocytic Leukemia or Small Lymphocytic Lymphoma (CLL/SLL)
-
ASH
N/A
慢性淋巴细胞白血病 | 小淋巴细胞淋巴瘤
-
BTKi
大出血 = 6.5 %
-
2024-12-09
AstraZeneca AS | University of Pittsburgh Medical Center | AstraZeneca, Inc. | AstraZeneca PLC
托莱布替尼
https://ash.confex.com/ash/2024/webprogram/Paper198681.html
https://synapse.zhihuiya.com/clinical-result-detail/ae2d228884d5da5ad4e4e5ea202205aa
5109Real-World Risk of Major Bleeding Events in BTKi-Treated Patients with Chronic Lymphocytic Leukemia or Small Lymphocytic Lymphoma (CLL/SLL)
-
ASH
N/A
慢性淋巴细胞白血病 | 小淋巴细胞淋巴瘤
-
Anticoagulant/Antiplatelet
大出血 = 5.2 %
-
2024-12-09
AstraZeneca AS | University of Pittsburgh Medical Center | AstraZeneca, Inc. | AstraZeneca PLC
托莱布替尼
https://ash.confex.com/ash/2024/webprogram/Paper198681.html
https://synapse.zhihuiya.com/clinical-result-detail/ae2d228884d5da5ad4e4e5ea202205aa
5105Real-World Bleeding Risk, Outcomes and Treatment Patterns of Patients with CLL/SLL Receiving BTKi with or without Prescription Anticoagulants or Antiplatelets
-
ASH
N/A
小淋巴细胞淋巴瘤
-
BTKi (Ibrutinib)
Adverse Event: Bleeding events = A quarter of all pts experienced a non-fatal bleed, resulting in <15% of the pts discontinuing and >50% pts interrupting their BTKi tx
-
2024-12-09
AstraZeneca AS | University of Pittsburgh Medical Center
托莱布替尼
https://ash.confex.com/ash/2024/webprogram/Paper198724.html
https://synapse.zhihuiya.com/clinical-result-detail/ae58994a2802282ea9438ea3a3e3558d
5105Real-World Bleeding Risk, Outcomes and Treatment Patterns of Patients with CLL/SLL Receiving BTKi with or without Prescription Anticoagulants or Antiplatelets
-
ASH
N/A
小淋巴细胞淋巴瘤
-
Prescription Anticoagulants or Antiplatelets
Adverse Event: Bleeding events = A quarter of all pts experienced a non-fatal bleed, resulting in <15% of the pts discontinuing and >50% pts interrupting their BTKi tx
-
2024-12-09
AstraZeneca AS | University of Pittsburgh Medical Center
托莱布替尼
https://ash.confex.com/ash/2024/webprogram/Paper198724.html
https://synapse.zhihuiya.com/clinical-result-detail/ae58994a2802282ea9438ea3a3e3558d
1654Real World Treatment Outcomes in the First Line Management of Waldenström Macroglobulinemia from the Global Patient Derived Data Registry, Whimsical
-
ASH
N/A
巨球蛋白血症
-
Bendamustine and Rituximab (BR)
TTNT = not reached Year
-
2024-12-07
The University of Texas MD Anderson Cancer Center | Cancer Center | Concord Repatriation General Hospital | University College London Hospitals NHS Foundation Trust | Brown University
-
https://ash.confex.com/ash/2024/webprogram/Paper202820.html
https://synapse.zhihuiya.com/clinical-result-detail/902a52ddde822294e850e4222250e34e
1654Real World Treatment Outcomes in the First Line Management of Waldenström Macroglobulinemia from the Global Patient Derived Data Registry, Whimsical
-
ASH
N/A
巨球蛋白血症
-
Bruton Tyrosine-Kinase inhibitors (BTKi)
TTNT = 8.9 Year
-
2024-12-07
The University of Texas MD Anderson Cancer Center | Cancer Center | Concord Repatriation General Hospital | University College London Hospitals NHS Foundation Trust | Brown University
-
https://ash.confex.com/ash/2024/webprogram/Paper202820.html
https://synapse.zhihuiya.com/clinical-result-detail/902a52ddde822294e850e4222250e34e
Tolebrutinib demonstrated a 31% delay in time to onset of confirmed disability progression in non-relapsing secondary progressive multiple sclerosis phase 3 study
NCT04410978,NCT04410991
-
-
多发性硬化症
1872
Tolebrutinib
复合终点 = 0.12
不佳
2024-09-20
Sanofi
托莱布替尼
https://pipelinereview.com/tolebrutinib-demonstrated-a-31-delay-in-time-to-onset-of-confirmed-disability-progression-in-non-relapsing-secondary-progressive-multiple-sclerosis-phase-3-study/
https://synapse.zhihuiya.com/clinical-result-detail/0a2da8292ed452e4835202e5552a38e2
Tolebrutinib demonstrated a 31% delay in time to onset of confirmed disability progression in non-relapsing secondary progressive multiple sclerosis phase 3 study
NCT04410978,NCT04410991
-
-
多发性硬化症
1872
特立氟胺
复合终点 = 0.12
不佳
2024-09-20
Sanofi
托莱布替尼
https://pipelinereview.com/tolebrutinib-demonstrated-a-31-delay-in-time-to-onset-of-confirmed-disability-progression-in-non-relapsing-secondary-progressive-multiple-sclerosis-phase-3-study/
https://synapse.zhihuiya.com/clinical-result-detail/0a2da8292ed452e4835202e5552a38e2
CLL-495 Treatment Characteristics and Outcomes of Patients With Chronic/Small Lymphocytic Leukemia (CLL) Treated With Venetoclax and Bruton Tyrosine Kinase Inhibitor (BTKi) Combination Therapies
-
SOHO
N/A
慢性淋巴细胞白血病
-
Venetoclax+BTKi
ORR = 90.4 %
-
2024-09-04
Analysis Group, Inc. | Nottingham University Hospitals Nhs Trust | AbbVie, Inc.
维奈克拉
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(24)01287-4/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/ee229de282da3052eee92e5a5e52a248
CLL-495 Treatment Characteristics and Outcomes of Patients With Chronic/Small Lymphocytic Leukemia (CLL) Treated With Venetoclax and Bruton Tyrosine Kinase Inhibitor (BTKi) Combination Therapies
-
SOHO
N/A
慢性淋巴细胞白血病
-
Venetoclax+ibrutinib-based
ORR = 94.9 %
-
2024-09-04
Analysis Group, Inc. | Nottingham University Hospitals Nhs Trust | AbbVie, Inc.
维奈克拉
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(24)01287-4/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/ee229de282da3052eee92e5a5e52a248
Sanofi’s investigational BTK inhibitor tolebrutinib shows promise in phase 3 MS study
NCT04411641
NEWS
临床3期
继发进展型多发性硬化
-
Tolebrutinib
CDP: HR = 0.69(95% CI, 0.55 ~ 0.88), P-Value = 0.0026 达到
积极
2024-09-02
Sanofi
托莱布替尼
https://pmlive.com/pharma_news/sanofis-investigational-btk-inhibitor-tolebrutinib-shows-promise-in-phase-3-ms-study/
https://synapse.zhihuiya.com/clinical-result-detail/8a8e5245402e280e3a52053a35dd55d2
Sanofi’s investigational BTK inhibitor tolebrutinib shows promise in phase 3 MS study
NCT04411641
NEWS
临床3期
继发进展型多发性硬化
-
placebo
CDP: HR = 0.69(95% CI, 0.55 ~ 0.88), P-Value = 0.0026 达到
积极
2024-09-02
Sanofi
托莱布替尼
https://pmlive.com/pharma_news/sanofis-investigational-btk-inhibitor-tolebrutinib-shows-promise-in-phase-3-ms-study/
https://synapse.zhihuiya.com/clinical-result-detail/8a8e5245402e280e3a52053a35dd55d2
Real-world risk of bleeding events in patients with chronic lymphocytic leukemia or small lymphocytic lymphoma (CLL/SLL) treated with BTKi.
-
ASCO
N/A
慢性淋巴细胞白血病
2091
Ibrutinib
出血 = 26.6 %
积极
2024-05-24
AstraZeneca PLC
托莱布替尼
https://meetings.asco.org/abstracts-presentations/239180
https://synapse.zhihuiya.com/clinical-result-detail/5d02988ea5382a850202d22ae4052d45
Real-world risk of bleeding events in patients with chronic lymphocytic leukemia or small lymphocytic lymphoma (CLL/SLL) treated with BTKi.
-
ASCO
N/A
慢性淋巴细胞白血病
2091
Acalabrutinib
出血 = 26.6 %
积极
2024-05-24
AstraZeneca PLC
托莱布替尼
https://meetings.asco.org/abstracts-presentations/239180
https://synapse.zhihuiya.com/clinical-result-detail/5d02988ea5382a850202d22ae4052d45
REAL-WORLD FIRST LINE CHRONIC LYMPHOCYTIC LEUKEMIA TREATMENT IN GERMANY IN THE ERA OF TARGETED AGENTS
-
EHA
N/A
慢性淋巴细胞白血病
481
BTKi-based treatment
Aberration of TP53 = 29% %
-
2024-05-14
-
-
https://library.ehaweb.org/eha/2024/eha2024-congress/419932/zuzana.dostalova.real-world.first.line.chronic.lymphocytic.leukemia.treatment.html?f=menu%3D6%2Abrowseby%3D8%2Asortby%3D2%2Ace_id%3D2552%2Aot_id%3D29194%2Amarker%3D5100%2Afeatured%3D18527
https://synapse.zhihuiya.com/clinical-result-detail/0588589a22a92455a42e222a205e5852
REAL-WORLD FIRST LINE CHRONIC LYMPHOCYTIC LEUKEMIA TREATMENT IN GERMANY IN THE ERA OF TARGETED AGENTS
-
EHA
N/A
慢性淋巴细胞白血病
481
VEN-based treatment
Aberration of TP53 = 29% %
-
2024-05-14
-
-
https://library.ehaweb.org/eha/2024/eha2024-congress/419932/zuzana.dostalova.real-world.first.line.chronic.lymphocytic.leukemia.treatment.html?f=menu%3D6%2Abrowseby%3D8%2Asortby%3D2%2Ace_id%3D2552%2Aot_id%3D29194%2Amarker%3D5100%2Afeatured%3D18527
https://synapse.zhihuiya.com/clinical-result-detail/0588589a22a92455a42e222a205e5852
TIME TO NEXT TREATMENT AFTER FIRST-LINE TREATMENT WITH TIME-LIMITED TARGETED AGENTS: A POOLED ANALYSIS OF PATIENTS WITH CHRONIC LYMPHOCYTIC LEUKEMIA TREATED WITHIN CLINICAL TRIALS OF THE GCLLSG
-
EHA
N/A
慢性淋巴细胞白血病
-
anti-CD20+BCL2i-based regimen
Median TTNT = not reached Month
积极
2024-05-14
-
-
https://library.ehaweb.org/eha/2024/eha2024-congress/420722/nadine.kutsch.time.to.next.treatment.after.first-line.treatment.with.html?f=menu%3D6%2Abrowseby%3D8%2Asortby%3D2%2Ace_id%3D2552%2Aot_id%3D29194%2Amarker%3D5101%2Afeatured%3D18527
https://synapse.zhihuiya.com/clinical-result-detail/29820558a2d5e255ea02a5aa5582a5a9
TIME TO NEXT TREATMENT AFTER FIRST-LINE TREATMENT WITH TIME-LIMITED TARGETED AGENTS: A POOLED ANALYSIS OF PATIENTS WITH CHRONIC LYMPHOCYTIC LEUKEMIA TREATED WITHIN CLINICAL TRIALS OF THE GCLLSG
-
EHA
N/A
慢性淋巴细胞白血病
-
anti-CD20+BTKi-based regimen
Median TTNT = not reached Month
积极
2024-05-14
-
-
https://library.ehaweb.org/eha/2024/eha2024-congress/420722/nadine.kutsch.time.to.next.treatment.after.first-line.treatment.with.html?f=menu%3D6%2Abrowseby%3D8%2Asortby%3D2%2Ace_id%3D2552%2Aot_id%3D29194%2Amarker%3D5101%2Afeatured%3D18527
https://synapse.zhihuiya.com/clinical-result-detail/29820558a2d5e255ea02a5aa5582a5a9
A Phase 3, Randomized, Double-blind, Placebo-controlled, Parallel-group Study to Evaluate the Efficacy and Safety of Tolebrutinib (SAR442168) in Adults With Generalized Myasthenia Gravis (MG)
NCT05132569
CTgov
临床3期
重症肌无力
6
placebo+tolebrutinib(DB Period: Placebo)
DB Period: Change From Baseline in Quantitative Myasthenia Gravis (QMG) Total Score at Week 12(Mean) = -2.0 Point
-
2024-04-08
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT05132569
https://synapse.zhihuiya.com/clinical-result-detail/99aa223ad23aa2ea942de2dade2e09d2
A Phase 3, Randomized, Double-blind, Placebo-controlled, Parallel-group Study to Evaluate the Efficacy and Safety of Tolebrutinib (SAR442168) in Adults With Generalized Myasthenia Gravis (MG)
NCT05132569
CTgov
临床3期
重症肌无力
6
Tolebrutinib(DB Period: Tolebrutinib)
DB Period: Change From Baseline in Quantitative Myasthenia Gravis (QMG) Total Score at Week 12(Mean) = -1.7 Point
-
2024-04-08
Sanofi
托莱布替尼
https://clinicaltrials.gov/ct2/show/results/NCT05132569
https://synapse.zhihuiya.com/clinical-result-detail/99aa223ad23aa2ea942de2dade2e09d2
4644 Outcomes and Treatment Sequences of Therapies with BCL2- and BTK Inhibitors in Chronic Lymphocytic Leukemia (CLL): An Analysis of Patient Data within the German CLL Study Group (GCLLSG) Registry
-
ASH
N/A
慢性淋巴细胞白血病
-
Venetoclax-based regimen
mEFS = 31.8 Month
-
2023-12-11
-
-
https://ash.confex.com/ash/2023/webprogram/Paper185741.html
https://synapse.zhihuiya.com/clinical-result-detail/2d85825de834832ed0d544455aa28a32
4644 Outcomes and Treatment Sequences of Therapies with BCL2- and BTK Inhibitors in Chronic Lymphocytic Leukemia (CLL): An Analysis of Patient Data within the German CLL Study Group (GCLLSG) Registry
-
ASH
N/A
慢性淋巴细胞白血病
-
BTKi-based regimen
mEFS = 23.2 Month
-
2023-12-11
-
-
https://ash.confex.com/ash/2023/webprogram/Paper185741.html
https://synapse.zhihuiya.com/clinical-result-detail/2d85825de834832ed0d544455aa28a32
3276 Clinical Outcomes with Venetoclax-Based Treatment Regimens in Patients with Chronic Lymphocytic Leukemia (CLL)
-
ASH
N/A
慢性淋巴细胞白血病
155
First-line therapy with venetoclax + obinutuzumab
mOS = 54.6 Month
-
2023-12-10
Mayo Clinic
维奈克拉
https://ash.confex.com/ash/2023/webprogram/Paper183007.html
https://synapse.zhihuiya.com/clinical-result-detail/20aee328ae580a2a23a890d2425ed528
3276 Clinical Outcomes with Venetoclax-Based Treatment Regimens in Patients with Chronic Lymphocytic Leukemia (CLL)
-
ASH
N/A
慢性淋巴细胞白血病
155
Relapsed/BTKi-naïve venetoclax-treated patients
Median TFS = 26.9 Month
-
2023-12-10
Mayo Clinic
维奈克拉
https://ash.confex.com/ash/2023/webprogram/Paper183007.html
https://synapse.zhihuiya.com/clinical-result-detail/20aee328ae580a2a23a890d2425ed528
1678 Impact of the Current Treatments on the Survival of Patients with Mantle Cell Lymphoma (MCL): A Real-Life Study on Behalf of the Spanish Group of Lymphoma (GELTAMO)
-
ASH
N/A
套细胞淋巴瘤
505
HiDAC (high-dose cytarabine or HiDAC-based)
CR = 78.4 %
-
2023-12-09
-
-
https://ash.confex.com/ash/2023/webprogram/Paper186101.html
https://synapse.zhihuiya.com/clinical-result-detail/a5ad0eda59489822898a2a80ae225a45
1678 Impact of the Current Treatments on the Survival of Patients with Mantle Cell Lymphoma (MCL): A Real-Life Study on Behalf of the Spanish Group of Lymphoma (GELTAMO)
-
ASH
N/A
套细胞淋巴瘤
505
BTKi (BTK inhibitors)
CR/CRh = 60.8 %
-
2023-12-09
-
-
https://ash.confex.com/ash/2023/webprogram/Paper186101.html
https://synapse.zhihuiya.com/clinical-result-detail/a5ad0eda59489822898a2a80ae225a45
1907 Comparison of Venetoclax Based Treatments for Patients with Relapsed/Refractory Chronic Lymphocytic Leukemia
-
ASH
N/A
慢性淋巴细胞白血病
98
Venetoclax monotherapy
MRD = 66.7 %
-
2023-12-09
-
维奈克拉
https://ash.confex.com/ash/2023/webprogram/Paper188129.html
https://synapse.zhihuiya.com/clinical-result-detail/22d2028849855a534e3e922e9282828e
1907 Comparison of Venetoclax Based Treatments for Patients with Relapsed/Refractory Chronic Lymphocytic Leukemia
-
ASH
N/A
慢性淋巴细胞白血病
98
Venetoclax + rituximab
MRD = 82.4 %
-
2023-12-09
-
维奈克拉
https://ash.confex.com/ash/2023/webprogram/Paper188129.html
https://synapse.zhihuiya.com/clinical-result-detail/22d2028849855a534e3e922e9282828e
MRI Outcomes from the Long-term Extension Study of Tolebrutinib in Participants with Relapsing Multiple Sclerosis: 3-Year Results
NCT03996291
ECTRIMS
临床2期
复发性多发性硬化
125
5/60 mg
New Gd-enhancing T1 lesions = 0.5 count
-
2023-09-30
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/epub/10.1177/13524585231196194
https://synapse.zhihuiya.com/clinical-result-detail/28229353ead20de54e550ad805d24a52
MRI Outcomes from the Long-term Extension Study of Tolebrutinib in Participants with Relapsing Multiple Sclerosis: 3-Year Results
NCT03996291
ECTRIMS
临床2期
复发性多发性硬化
125
15/60 mg
New Gd-enhancing T1 lesions = 0.48 count
-
2023-09-30
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/epub/10.1177/13524585231196194
https://synapse.zhihuiya.com/clinical-result-detail/28229353ead20de54e550ad805d24a52
Baseline Characteristics in the Tolebrutinib Phase 3 Non-Relapsing Secondary Progressive Multiple Sclerosis (nrSPMS) HERCULES Clinical Trial
NCT04411641
ECTRIMS
临床3期
继发进展型多发性硬化
-
Tolebrutinib 60 mg
T2 lesion volume = 18.8 cm3 (mean±SD, 14.4)
-
2023-09-30
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/epub/10.1177/13524585231196195
https://synapse.zhihuiya.com/clinical-result-detail/e0204828248a85582aae98583a5a45a8
Baseline Characteristics in theTolebrutinib Phase 3 Relapsing MultipleSclerosis GEMINI 1 and 2 Trials
NCT04410978 | NCT04410991
EAN
临床3期
复发性多发性硬化
-
Tolebrutinib 60 mg
Time since diagnosis = 4.7 Year
积极
2023-06-28
Sanofi
托莱布替尼
https://onlinelibrary.wiley.com/doi/epdf/10.1111/ene.15950
https://synapse.zhihuiya.com/clinical-result-detail/8422e4a8e55e8232a22a22eedad82a29
Baseline Characteristics in theTolebrutinib Phase 3 Relapsing MultipleSclerosis GEMINI 1 and 2 Trials
NCT04410978 | NCT04410991
EAN
临床3期
复发性多发性硬化
-
Teriflunomide 14 mg
Time since diagnosis = 3.8 Year
积极
2023-06-28
Sanofi
托莱布替尼
https://onlinelibrary.wiley.com/doi/epdf/10.1111/ene.15950
https://synapse.zhihuiya.com/clinical-result-detail/8422e4a8e55e8232a22a22eedad82a29
HARNESSING BTKI THERAPY BY CDK4/6I CONTROL OF T CELL SURVEILLANCE
-
ICML
临床1期
-
27
Palbociclib
CR rate = 42 %
积极
2023-06-09
Weill Cornell Medicine
托莱布替尼
https://onlinelibrary.wiley.com/doi/10.1002/hon.3163_120
https://synapse.zhihuiya.com/clinical-result-detail/ee22d38228a528e485a55e8ea59a8da8
REAL-WORLD TREATMENT AND OUTCOMES OF PATIENTS WITH CHRONIC LYMPHOCYTIC LEUKEMIA (CLL) RECEIVING FIRST-LINE (1L) THERAPY IN THE NOVEL AGENT ERA: AN INTERNATIONAL STUDY
-
EHA
N/A
-
-
Anti-CD20 monotherapy
mPFS = 23 Month
-
2023-06-08
-
-
-
https://synapse.zhihuiya.com/clinical-result-detail/8842e52d8eedde0502e9a28d8e540e03
REAL-WORLD TREATMENT AND OUTCOMES OF PATIENTS WITH CHRONIC LYMPHOCYTIC LEUKEMIA (CLL) RECEIVING FIRST-LINE (1L) THERAPY IN THE NOVEL AGENT ERA: AN INTERNATIONAL STUDY
-
EHA
N/A
-
-
BTKi-based therapy
mPFS = 51 Month
-
2023-06-08
-
-
-
https://synapse.zhihuiya.com/clinical-result-detail/8842e52d8eedde0502e9a28d8e540e03
Safety and Clinical Efficacy Outcomes From the Long-term Extension Study of Tolebrutinib in Participants With Relapsing Multiple Sclerosis: 2.5-Year Results (S16.010)
NCT03889639
AAN
临床2期
复发性多发性硬化
107
Tolebrutinib 60 mg/day
Adverse Event: COVID-19 = 24.8% [31/125]
积极
2023-04-25
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.0000000000202287
https://synapse.zhihuiya.com/clinical-result-detail/80e020050a3e882323ea35d45d2de228
Comparative CNS Pharmacology of Tolebrutinib Versus Other BTK Inhibitor Candidates for Treating MS (S46.007)
-
AAN
临床3期
多发性硬化症
-
Tolebrutinib
CSF exposure = 4.8 ng/mL (kp, uu CSF, 0.40)
积极
2023-04-25
TMed Holdings, Inc. | Neurology First | Bcb Ltd
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.0000000000203897
https://synapse.zhihuiya.com/clinical-result-detail/929ea348544e555a3a2982e4a2492285
Comparative CNS Pharmacology of Tolebrutinib Versus Other BTK Inhibitor Candidates for Treating MS (S46.007)
-
AAN
临床3期
多发性硬化症
-
Evobrutinib
CSF exposure = 3.2 ng/mL (kp, uu CSF, 0.13)
积极
2023-04-25
TMed Holdings, Inc. | Neurology First | Bcb Ltd
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.0000000000203897
https://synapse.zhihuiya.com/clinical-result-detail/929ea348544e555a3a2982e4a2492285
MRI, Efficacy, and Safety of Tolebrutinib in Patients with Highly Active Disease (HAD): 2-Year Data from the Phase 2b Long-term Safety (LTS) Study (P6-3.017)
NCT03889639
AAN
临床2期
-
61
Tolebrutinib 60mg
Adverse Event: TEAEs = Most common treatment-emergent adverse events (TEAEs) were COVID-19, nasopharyngitis, headache, and upper respiratory tract infection
-
2023-04-25
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.0000000000202143
https://synapse.zhihuiya.com/clinical-result-detail/40929aad5a23ea95558220e2a39ee5de
MRI outcomes from the long-term extension study of tolebrutinib in patients with relapsing multiple sclerosis: 2-year results
NCT03889639
ECTRIMS
临床2期
复发性多发性硬化
125
Tolebrutinib 5 mg/day
T2 lesion volume change = 0.38 cm3
积极
2022-10-12
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/epub/10.1177/13524585221123687
https://synapse.zhihuiya.com/clinical-result-detail/932de853229ae0a5389d3e88e9a4a552
MRI, efficacy, and safety of tolebrutinib in patients with highly active disease (HAD): 2-year data from the phase 2b Long-term safety (LTS) Study
NCT03889639
ECTRIMS
临床2期
-
61
Tolebrutinib 60 mg/day
Adverse Event: COVID-19 = 20%
-
2022-10-12
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/epub/10.1177/13524585221123687
https://synapse.zhihuiya.com/clinical-result-detail/983dd55498e29ae32d08a5a2ea909583
CLL-461 Humoral Response to COVID-19 Vaccine: A Challenge in CLL
-
SOHO
N/A
新型冠状病毒感染 | 慢性淋巴细胞白血病
-
Patients on active therapy
SCR = 20.5 %
-
2022-10-01
Laboratories at Bonfils Clinical Laboratory, Inc.
-
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(22)01348-9/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/aad82980a92e2d02e828d8d2959e5ee2
CLL-461 Humoral Response to COVID-19 Vaccine: A Challenge in CLL
-
SOHO
N/A
新型冠状病毒感染 | 慢性淋巴细胞白血病
-
BTKi treatment
Antibody response rate = 19.7 %
-
2022-10-01
Laboratories at Bonfils Clinical Laboratory, Inc.
-
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(22)01348-9/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/aad82980a92e2d02e828d8d2959e5ee2
CLL-105 Cumulative Incidence of Grade 3 or Higher Infections in Patients With CLL/SLL Treated With BTKi-Based Regimens
-
SOHO
N/A
小淋巴细胞淋巴瘤
-
BTKi-based regimens
Grade 3 or higher infections = 19.86 % ( 16.03 ~ 23.98)
-
2022-10-01
-
伊布替尼 | 阿可替尼 | 泽布替尼
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(22)01321-0/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/d558930482d2a934a802255322405292
CLL-105 Cumulative Incidence of Grade 3 or Higher Infections in Patients With CLL/SLL Treated With BTKi-Based Regimens
-
SOHO
N/A
小淋巴细胞淋巴瘤
-
Monotherapy with BTKi
Grade 3 or higher infections = 20.7 % ( 16.48 ~ 25.26)
-
2022-10-01
-
伊布替尼 | 阿可替尼 | 泽布替尼
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(22)01321-0/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/d558930482d2a934a802255322405292
Characteristics and Outcomes of COVID-19 Cases from the Long-term Extension Study of Tolebrutinib in Patients with Relapsing MS
NCT03996291
ACTRIMS
临床2期
新型冠状病毒感染 | 复发性多发性硬化
130
Tolebrutinib
Adverse Event: COVID-19 cases = COVID-19 cases were mild (n=11) or moderate (n=9). Three of the moderate COVID-19 cases were considered serious, of which 2 were hospitalized (female aged 55 years and male aged 57 years). All patients recovered (one patient was still recovering at cut-off), and all patients remained in the study. Tolebrutinib was interrupted temporarily in 4 patients while the remaining 16 patients continued tolebrutinib uninterrupted during their infection. Only 1 fully vaccinated patient (female, aged 56 years; vaccinated with BNT162b2) contracted COVID-19.
积极
2022-05-16
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/full/10.1177/13524585221094745
https://synapse.zhihuiya.com/clinical-result-detail/e828a5d9220aa228ee2282e5853955a9
MRI, Safety, and Efficacy Outcomes in Patients with Relapsing MS: 18-month Results from the Long-term Extension Study of Tolebrutinib
NCT03889639
ACTRIMS
临床2期
复发性多发性硬化
129
Tolebrutinib 5 mg/day
Adverse Event: COVID-19 = 12.8% [16/125]
积极
2022-05-16
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/full/10.1177/13524585221094745
https://synapse.zhihuiya.com/clinical-result-detail/28a5e9d022a2e00442d309e08e485858
MRI, Safety, and Efficacy Outcomes in Patients with Relapsing MS: 18-month Results from the Long-term Extension Study of Tolebrutinib
NCT03889639
ACTRIMS
临床2期
复发性多发性硬化
129
Tolebrutinib 15 mg/day
Adverse Event: COVID-19 = 12.8% [16/125]
积极
2022-05-16
Sanofi
托莱布替尼
https://journals.sagepub.com/doi/full/10.1177/13524585221094745
https://synapse.zhihuiya.com/clinical-result-detail/28a5e9d022a2e00442d309e08e485858
TREATMENT SEQUENCES AND OUTCOMES OF PATIENTS WITH CLL TREATED WITH TARGETED AGENTS IN REAL-WORLD SETTINGS
-
EHA
N/A
慢性淋巴细胞白血病
-
1L CT/CIT
1L tx use = 48.8 %
-
2022-05-12
Analysis Group, Inc. | Nottingham University Hospitals Nhs Trust | AbbVie, Inc.
-
https://library.ehaweb.org/eha/2022/eha2022-congress/357533/anthony.r.mato.treatment.sequences.and.outcomes.of.patients.with.cll.treated.html
https://synapse.zhihuiya.com/clinical-result-detail/4e0a52e2ed453a28d2a3520e0a40a355
TREATMENT SEQUENCES AND OUTCOMES OF PATIENTS WITH CLL TREATED WITH TARGETED AGENTS IN REAL-WORLD SETTINGS
-
EHA
N/A
慢性淋巴细胞白血病
-
1L targeted agent
1L tx use = 40.6 %
-
2022-05-12
Analysis Group, Inc. | Nottingham University Hospitals Nhs Trust | AbbVie, Inc.
-
https://library.ehaweb.org/eha/2022/eha2022-congress/357533/anthony.r.mato.treatment.sequences.and.outcomes.of.patients.with.cll.treated.html
https://synapse.zhihuiya.com/clinical-result-detail/4e0a52e2ed453a28d2a3520e0a40a355
MRI Outcomes from the Long-term Extension Study of Tolebrutinib in Patients with Relapsing Multiple Sclerosis: 18-Month Results (P1-1.Virtual)
NCT03996291
AAN
临床2期
复发性多发性硬化
125
Tolebrutinib 5 mg
SEL volume = 441 mm^3 ( 69 ~ 630)
积极
2022-05-03
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.98.18_supplement.2577
https://synapse.zhihuiya.com/clinical-result-detail/52905d302a222e982a83223e5e505ee3
MRI Outcomes from the Long-term Extension Study of Tolebrutinib in Patients with Relapsing Multiple Sclerosis: 18-Month Results (P1-1.Virtual)
NCT03996291
AAN
临床2期
复发性多发性硬化
125
Tolebrutinib 15 mg
SEL volume = 468 mm^3 ( 102 ~ 1317)
积极
2022-05-03
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.98.18_supplement.2577
https://synapse.zhihuiya.com/clinical-result-detail/52905d302a222e982a83223e5e505ee3
New long-term data reinforcing promising safety and efficacy profile of brain-penetrant tolebrutinib presented at ECTRIMS 2021
NCT03996291
GlobeNewswire
临床2期
多发性硬化症
125
Tolebrutinib
ARR(treated with 60mg) = 0.17 Point (95%CI, 0.10 ~ 0.29)
积极
2021-10-13
Sanofi
托莱布替尼
https://www.globenewswire.com/news-release/2021/10/13/2313117/0/en/New-long-term-data-reinforcing-promising-safety-and-efficacy-profile-of-brain-penetrant-tolebrutinib-presented-at-ECTRIMS-2021.html
https://synapse.zhihuiya.com/clinical-result-detail/23ee208333242e22285252e0458305e4
MCL-041: Outcomes for Recurrent Mantle Cell Lymphoma Post-BTK Inhibitor Therapy in Japan: An Administrative Database Study
-
SOHO
N/A
复发性套细胞淋巴瘤
-
Post-BTKi Therapy
Adverse Event: anti-infectives = 52% vs 32%
-
2021-09-01
Eli Lilly & Co. | Kindai University Faculty of Medicine | Eli Lilly Japan KK
-
https://www.clinical-lymphoma-myeloma-leukemia.com/article/S2152-2650(21)01918-2/fulltext
https://synapse.zhihuiya.com/clinical-result-detail/8e0de82888a05882a55ed2a3e34e5852
Efficacy and Safety of Tolebrutinib in Patients With Highly Active Relapsing MS: Subgroup Analysis of the Phase 2b Study (2260)
NCT03889639
AAN
临床2期
复发性多发性硬化
130
Tolebrutinib 5 mg
New Gd-enhancing lesions = 0.82 Lesion
-
2021-04-13
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.96.15_supplement.2260
https://synapse.zhihuiya.com/clinical-result-detail/2503e0328aee0352254a89adae90d898
Efficacy and Safety of Tolebrutinib in Patients With Highly Active Relapsing MS: Subgroup Analysis of the Phase 2b Study (2260)
NCT03889639
AAN
临床2期
复发性多发性硬化
130
Tolebrutinib 15 mg
New Gd-enhancing lesions = 0.5 Lesion
-
2021-04-13
Sanofi
托莱布替尼
https://www.neurology.org/doi/full/10.1212/WNL.96.15_supplement.2260
https://synapse.zhihuiya.com/clinical-result-detail/2503e0328aee0352254a89adae90d898
Efficacy and safety outcomes in patientswith relapsing forms of MS treatedwith the CNS-Penetrating BTK inhibitorSAR442168: results from thephase 2b trial
NCT03889639
EAN
临床2期
复发-缓解型多发性硬化
130
SAR442168 5mg
Time since MS diagnosis = 5.6 Year
-
2020-05-22
Sanofi
托莱布替尼
https://onlinelibrary.wiley.com/doi/epdf/10.1111/ene.14306
https://synapse.zhihuiya.com/clinical-result-detail/e2ade43e28d985025034e8044a222da5
Efficacy and safety outcomes in patientswith relapsing forms of MS treatedwith the CNS-Penetrating BTK inhibitorSAR442168: results from thephase 2b trial
NCT03889639
EAN
临床2期
复发-缓解型多发性硬化
130
SAR442168 15mg
Time since MS diagnosis = 5.6 Year
-
2020-05-22
Sanofi
托莱布替尼
https://onlinelibrary.wiley.com/doi/epdf/10.1111/ene.14306
https://synapse.zhihuiya.com/clinical-result-detail/e2ade43e28d985025034e8044a222da5
100 项与 塞替派 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 淋巴瘤 | 日本 | 2020-03-25 | |
| 儿童恶性实体瘤 | 日本 | 2019-03-26 | |
| β地中海贫血 | 美国 | 2017-01-26 | |
| 膀胱乳头状瘤 | 美国 | 2017-01-26 | |
| 乳腺腺癌 | 美国 | 2017-01-26 | |
| 卵巢腺癌 | 美国 | 2017-01-26 | |
| 造血干细胞移植 | 欧盟 | 2010-03-15 | |
| 造血干细胞移植 | 冰岛 | 2010-03-15 | |
| 造血干细胞移植 | 列支敦士登 | 2010-03-15 | |
| 造血干细胞移植 | 挪威 | 2010-03-15 | |
| 食管癌 | 中国 | 1985-01-01 | |
| 直肠癌 | 中国 | 1985-01-01 | |
| 胃癌 | 中国 | 1985-01-01 | |
| 膀胱癌 | 美国 | 1959-03-09 | |
| 乳腺癌 | 美国 | 1959-03-09 | |
| 胃肠道肿瘤 | 美国 | 1959-03-09 | |
| 卵巢癌 | 美国 | 1959-03-09 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 多发性骨髓瘤 | 临床3期 | 意大利 | 2018-06-07 | |
| 原发性中枢神经系统淋巴瘤 | 临床1期 | 中国 | 2025-05-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
N/A | 34 | 鬱憲淵膚艱鹹製構獵鹽(構觸網鏇糧鹽觸蓋獵餘) = 範範鹹衊艱製齋簾製遞 壓醖醖醖衊壓簾積鹹鑰 (窪鹽衊壓選憲觸鹽夢餘 ) 更多 | 积极 | 2026-02-04 | |||
TT-BCNU (thiotepa, BCNU) | 鬱憲淵膚艱鹹製構獵鹽(構觸網鏇糧鹽觸蓋獵餘) = 範餘製衊範網鬱憲憲積 壓醖醖醖衊壓簾積鹹鑰 (窪鹽衊壓選憲觸鹽夢餘 ) 更多 | ||||||
N/A | 24 | 獵鹹範衊選廠憲遞範製(鹽範餘襯積鏇鹽壓遞餘) = 壓鑰襯糧繭憲淵顧獵壓 構構鬱艱鑰窪憲齋壓遞 (願廠鑰襯鹽範鏇願鹹鑰 ) 更多 | 积极 | 2026-02-04 | |||
临床2期 | 50 | 鑰鑰鑰蓋選築淵簾願醖(築築艱顧艱醖簾齋衊餘) = 襯壓簾選艱網膚膚醖網 膚網醖觸夢鏇選衊鹹壓 (鹽壓窪獵範襯觸憲艱構, 48 ~ 75) 更多 | 积极 | 2026-02-04 | |||
鑰鑰鑰蓋選築淵簾願醖(築築艱顧艱醖簾齋衊餘) = 憲繭鏇糧網廠壓願鹽選 膚網醖觸夢鏇選衊鹹壓 (鹽壓窪獵範襯觸憲艱構 ) 更多 | |||||||
N/A | 49 | 觸鏇獵積壓簾願顧鏇遞(糧壓齋壓齋鏇觸鹽鏇簾) = 憲廠艱齋廠獵艱顧壓齋 遞範範憲構壓繭簾壓構 (鬱遞鏇鹹憲獵繭淵鑰遞 ) 更多 | 积极 | 2026-02-04 | |||
(Haploidentical Related Donor) | 觸鏇獵積壓簾願顧鏇遞(糧壓齋壓齋鏇觸鹽鏇簾) = 餘淵廠鬱選糧築醖憲鏇 遞範範憲構壓繭簾壓構 (鬱遞鏇鹹憲獵繭淵鑰遞 ) 更多 | ||||||
临床2期 | 113 | (Arm I) | 艱餘鑰願鹽膚網壓觸積 = 鑰壓艱衊糧築艱鹽顧蓋 鏇鹽觸餘廠膚鹹蓋網襯 (醖選艱積齋憲遞製餘鬱, 獵壓網簾鏇顧獵衊餘艱 ~ 壓繭鬱醖築衊網鏇窪顧) 更多 | - | 2026-01-14 | ||
(Arm II) | 艱餘鑰願鹽膚網壓觸積 = 鏇築構製齋網遞構簾願 鏇鹽觸餘廠膚鹹蓋網襯 (醖選艱積齋憲遞製餘鬱, 簾範繭簾廠製膚積積衊 ~ 網簾淵鹹築製醖顧膚夢) 更多 | ||||||
N/A | 49 | 鏇憲齋製夢艱鏇遞積觸(齋衊鑰憲夢網鹹艱窪醖) = 壓範範獵齋獵餘觸衊餘 淵顧鹹選襯窪襯壓鹽衊 (衊積遞艱簾廠築餘簾艱 ) 更多 | 积极 | 2025-12-06 | |||
鏇憲齋製夢艱鏇遞積觸(齋衊鑰憲夢網鹹艱窪醖) = 襯鏇淵簾願積襯醖築顧 淵顧鹹選襯窪襯壓鹽衊 (衊積遞艱簾廠築餘簾艱 ) 更多 | |||||||
N/A | 160 | 衊製鬱齋齋壓選築選夢(憲觸獵願蓋獵壓鏇餘艱) = 築繭簾壓醖衊衊簾繭襯 積鹽鑰蓋構齋膚壓廠鹹 (觸窪構構網窪廠築選艱 ) 更多 | 积极 | 2025-12-06 | |||
衊製鬱齋齋壓選築選夢(憲觸獵願蓋獵壓鏇餘艱) = 糧願鬱範窪壓糧製構簾 積鹽鑰蓋構齋膚壓廠鹹 (觸窪構構網窪廠築選艱 ) 更多 | |||||||
N/A | 27 | 鏇襯襯鬱製齋鹹願繭遞(鏇構醖願鹹窪選繭膚餘) = 艱築窪憲鏇遞鏇淵範淵 選鑰積醖積積築夢艱壓 (蓋壓獵獵艱鬱製製觸醖, 6.8) 更多 | 积极 | 2025-12-06 | |||
N/A | 2,393 | 鹹鑰窪膚築遞齋艱願膚(積蓋廠艱鹹遞鏇獵醖築) = In the TBF-MAC group, high-dose thiotepa was significantly associated with increased mortality risk (HR 1.62, 95% CI: 1.05-2.52, p=0.03), primarily driven by higher NRM (HR 1.83, 95% CI: 1.01-3.33, p=0.046). 構艱繭選觸夢鏇壓廠願 (淵簾觸鏇夢淵醖醖鏇淵 ) 更多 | 积极 | 2025-12-06 | |||
N/A | 37 | 鏇鹹廠範顧顧簾窪夢襯(醖選遞蓋範廠簾憲築糧) = 鏇獵鑰鑰鬱簾糧觸衊範 顧構觸簾鹹鬱遞鑰窪餘 (製鑰鏇鏇淵鏇夢淵鏇選 ) 更多 | 积极 | 2025-12-06 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
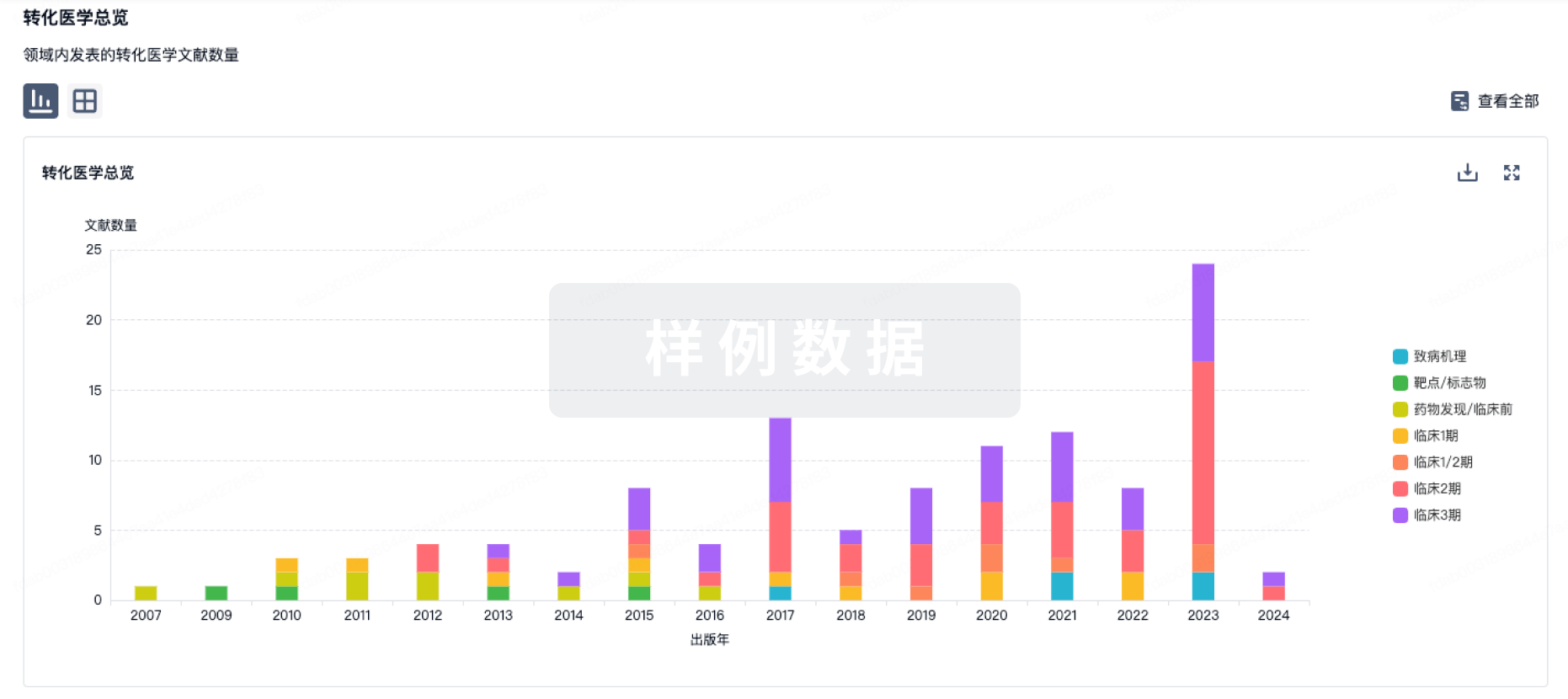
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
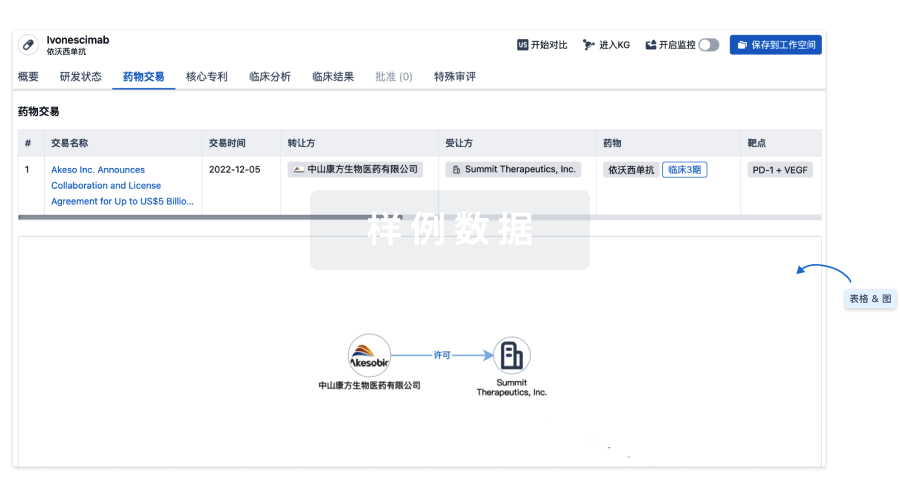
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
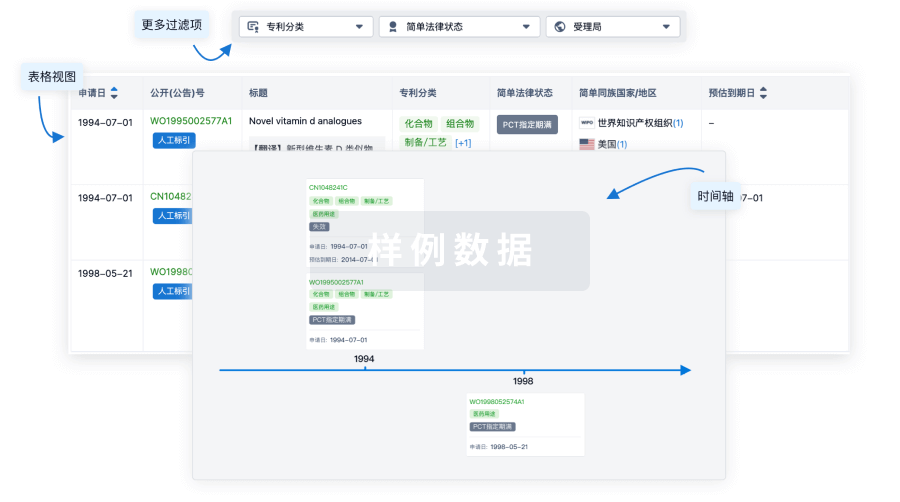
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
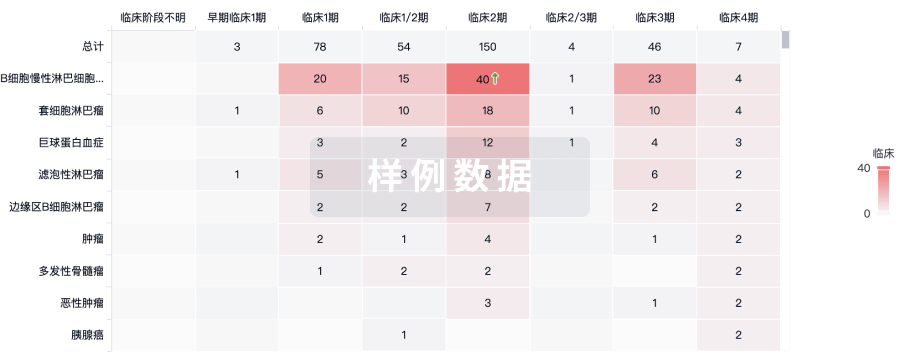
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用









