预约演示
更新于:2026-05-22
Doxorubicin Hydrochloride
盐酸多柔比星
更新于:2026-05-22
概要
基本信息
原研机构 |
非在研机构 |
最高研发阶段批准上市 |
最高研发阶段(中国)批准上市 |
特殊审评加速批准 (美国)、孤儿药 (美国)、孤儿药 (欧盟)、孤儿药 (日本) |
登录后查看时间轴
结构/序列
分子式C27H30ClNO11 |
InChIKeyMWWSFMDVAYGXBV-RUELKSSGSA-N |
CAS号25316-40-9 |
关联
1,788
项与 盐酸多柔比星 相关的临床试验NCT07125183
A Phase II Study on Efficacy and Tolerability of Weekly Doxorubicin in Elderly Patients With Advanced or Metastatic Leiomyosarcoma of Soft Tissue
The overall goal of this Phase 2 study is to determine the efficacy of a lower dose weekly schedule of doxorubicin in patients with unresectable leiomyosarcomas aged 65-100 years old. While doxorubicin is the standard of care therapy for sarcomas not removable by surgery, older or more frail patients may struggle to tolerate side effects of the treatment including immune cell suppression. Previous studies have suggested that similar anti-tumor activity can be obtained using a lower dose, weekly administration schedule of doxorubicin. In this study, the investigators will determine progression-free survival rate at 12 weeks, with secondary endpoints including quality of life and adverse events in this population. Importantly, doxorubicin can also induce immune stimulatory effects when administered at lower doses, based on animal data. Thus, correlative samples including blood and tumor biopsies will also explore the effects of immune cells and foreignness of the tumor prior to and during treatment in study patients.
开始日期2026-12-01 |
申办/合作机构 |
NCT07551583
A Phase 2 Single Arm Study To Evaluate Safety And Preliminary Efficacy Of Nivolumab Plus AVD In Pediatric, Adolescent, And Young Adult Patients With Newly Diagnosed Early-Stage Non-Bulky Classical Hodgkin Lymphoma
The goal of this clinical research study is to learn if nivolumab plus AVD (doxorubicin, vinblastine, and dacarbazine) can help to control newly diagnosed early-stage non-bulky cHL in pediatric, adolescent, and young adult patients.
The safety of this drug combination will also be studied.
The safety of this drug combination will also be studied.
开始日期2026-10-01 |
NCT07444710
A Phase I Study of Glofitamab With Alternating R-CHOP/R-DHAP in Previously Untreated Mantle Cell Lymphoma
This phase I trial tests the safety, side effects and best dose of glofitamab given with alternating cycles of rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisone (R-CHOP)/ rituximab, dexamethasone, cytarabine, and cisplatin (R-DHAP) for the treatment of mantle cell lymphoma. Glofitamab is a monoclonal antibody that may interfere with the ability of cancer cells to grow and spread. A monoclonal antibody is a type of protein that can bind to certain targets in the body, such as molecules that cause the body to make an immune response (antigens). Rituximab is a monoclonal antibody. It binds to a protein called CD20, which is found on B cells (a type of white blood cell) and some types of cancer cells. This may help the immune system kill cancer cells. Cyclophosphamide is in a class of medications called alkylating agents. It works by damaging the cell's deoxyribonucleic acid (DNA) and may kill cancer cells. It may also lower the body's immune response. Doxorubicin is in a class of medications called anthracyclines. Doxorubicin damages the cell's DNA and may kill cancer cells. It also blocks a certain enzyme needed for cell division and DNA repair. Vincristine is in a class of medications called vinca alkaloids. It works by stopping cancer cells from growing and dividing and may kill them. Prednisone and dexamethasone are in a class of medications called corticosteroids. They are used to reduce inflammation and lower the body's immune response to help lessen the side effects of chemotherapy drugs. Chemotherapy drugs, such as cytarabine, work in different ways to stop the growth of cancer cells, either by killing the cells, by stopping them from dividing, or by stopping them from spreading. Cisplatin is in a class of medications known as platinum-containing compounds. It works by killing, stopping or slowing the growth of cancer cells. Giving glofitamab may be safe, tolerable and/or effective in treating patients with mantle cell lymphoma.
开始日期2026-08-20 |
申办/合作机构 |
100 项与 盐酸多柔比星 相关的临床结果
登录后查看更多信息
100 项与 盐酸多柔比星 相关的转化医学
登录后查看更多信息
100 项与 盐酸多柔比星 相关的专利(医药)
登录后查看更多信息
88,920
项与 盐酸多柔比星 相关的文献(医药)2026-12-31·INTERNATIONAL JOURNAL OF HYPERTHERMIA
Heat-activated intravenous liposomal doxorubicin combined with mitomycin C hyperthermic intravesical chemotherapy (HIVEC) for treatment of bladder cancer
Article
作者: Valera, Vladimir A. ; Starost, Matthew F. ; Pritchard, William F. ; Bakhutashvili, Ivane ; Karanian, John W. ; Hesswani, Charles ; Gurram, Sandeep ; Gopal, Nikhil ; Peer, Cody J. ; Wood, Bradford J. ; Haemmerich, Dieter ; Mikhail, Andrew S. ; Figg, William D. ; Schmidt, Keith T. ; Richardson, William
PURPOSE:
To evaluate the safety and pharmacokinetics of lyso-thermosensitive liposomal doxorubicin (LTLD, ThermoDox®) combined with mitomycin C (MMC) hyperthermic intravesical chemotherapy (HIVEC) as a potential treatment for non-muscle invasive bladder cancer.
MATERIALS AND METHODS:
Four healthy swine received a 30-minute intravenous infusion of LTLD in combination with HIVEC, consisting of one hour of warm MMC bladder recirculation. Full-thickness bladder wall specimens were surgically resected within 30 min of HIVEC completion for histologic analysis and assessment of doxorubicin (DOX) intrinsic fluorescence in cross sections. DOX and MMC concentrations were also measured in bladder specimens and in serial blood samples up to 4 h by LC/MS. Swine were monitored for 28 days for signs of toxicity and were weighed weekly. Complete blood counts were performed at 4 h and 28 days. Cystoscopy was performed at 28 days, and bladder tissue was collected for histology and quantification of drug concentrations.
RESULTS:
Mean DOX concentration in the bladder wall 30 min after treatment was 13.6 ± 4.67 µg/g, and DOX fluorescence was visible in all layers. Plasma DOX Cmax and AUC0-∞ were 16.4 ± 3.46 µg/mL and 23.2 ± 5.50 µg/mL · h, respectively. MMC was not detected in the bladder wall or blood above the lower limit of detection (20 ng/mL). The treatment was well tolerated, with no treatment-related adverse events and no weight loss during the 28-day observation. On day 28, cystoscopy demonstrated normal-appearing bladder lumen, and some vacuolated cells were observed on bladder wall histology.
CONCLUSIONS:
Intravenous LTLD combined with MMC HIVEC was feasible and well tolerated in swine.
2026-12-31·DRUG DELIVERY
Folate-targeted gold nanoparticles for doxorubicin delivery in tumor spheroids
Article
作者: Daniele, Raffaella ; Caliceti, Paolo ; Salmaso, Stefano ; Marzaro, Giovanni ; Fragassi, Agnese ; Pesce, Cristiano ; Tognetti, Francesco ; Verona, Marco
Targeted drug delivery systems represent a promising strategy for enhancing the efficacy and specificity of cancer therapy. In this study, 35 nm folate-targeted gold nanoparticles are presented as nanoparticle-drug conjugates obtained by anchoring on their surface lipoyl terminating doxorubicin prodrug (proDoxo) releasable at the endolysosomal acidic pH to prevent off-site toxic effects. Colloidal stable nanoparticles with a density of proDoxo up to 1000 molecules/particle and 2 kDa mPEG-SH coating were obtained. At pH 5, Doxo was completely released from the nanoparticles in 5 days while only 13% was released over the same period at pH 7.4. The nanoparticle decoration with folic acid as a targeting agent bestowed nanosystems with selective drug delivery to folate receptor (FR)-overexpressing cancer cells and controlled intracellular release. This led to enhanced cancer cell killing by folated nanoparticles compared to their nontargeted counterparts. Moreover, folated nanoparticles were found to distribute more homogeneously inside KBFR+ cancer cell spheroids than non-targeted nanoparticles, resulting in higher spheroid volume reduction.
2026-12-31·DRUG DELIVERY
Cryopreservation technology for improving the stability of liposomes and its precise drug monitoring in clinical drug research
Article
作者: Chen, Chuanpin ; Boafo, George Frimpong ; Zheng, Hongliang ; Ekpo, Marlene Davis ; Wang, Rongrong ; Wang, Lei ; Ali, Yimer Seid ; Shaw, Ibrahim ; Zhu, Ziyu ; Tan, Songwen
The instability of liposomes in blood samples during clinical drug research and drug monitoring results in the inability to accurately determine the actual drug concentrations in the body at the time of collection, mainly due to lipid deterioration, particle fusion or aggregation, and phase separation degradation, resulting in payload leakage. To improve drug monitoring accuracy, we developed a cryopreservation strategy in this study by innovatively combining cryoprotective agents (CPAs), such as L-proline, sucrose, and polyvinyl alcohol (PVA), to prevent liposomal leakage and maintain stability for reliable drug monitoring and clinical drug research applications. Doxorubicin liposomes were prepared, and the CPAs were tested at various concentrations and under different freeze‒thaw protocols in biological matrices, with the stability and leakage of the liposomes assessed. Each CPA contributes distinct stabilization mechanisms, with L-proline's osmoprotective ability, sucrose's hydrogen bonding, and PVA's steric hindrance to form a protective barrier. The optimized CPA combination demonstrated superior performance at 85% (v/v) by preserving liposomal integrity, offering the best cryoprotective effect for liposomes in plasma stored at -20 °C, achieving about 90% entrapment efficiency, compared to about 60% in the control group without CPAs. Mechanistic investigations confirmed that CPAs protect liposomes against mechanical stress, prevent membrane disruption, and reduce ice damage by inhibiting recrystallization and adjusting bilayer hydration. These findings offer practical solutions for accurate pharmacokinetic assessments and reliable personalized dosing, safer alternative for liposomal drug research, biobanking, and real-world therapeutic monitoring.
2,216
项与 盐酸多柔比星 相关的新闻(医药)2026-05-22
RAHWAY, N.J.--(BUSINESS WIRE)--Merck (NYSE: MRK), known as MSD outside of the United States and Canada, today announced the European Medicines Agency’s Committee for Medicinal Products for Human Use (CHMP) adopted a positive opinion recommending approval of KEYTRUDA® (pembrolizumab), Merck’s anti-PD-1 therapy, in combination with Padcev® (enfortumab vedotin-ejfv), an antibody-drug conjugate (ADC), as neoadjuvant treatment and then continued after radical cystectomy as adjuvant treatment, for adults with resectable muscle-invasive bladder cancer (MIBC) who are ineligible for cisplatin-containing chemotherapy. This recommendation, which also includes KEYTRUDA SC® [known as KEYTRUDA QLEX™ (pembrolizumab and berahyaluronidase alfa-pmph) in the U.S.], will now be reviewed by the European Commission (EC) for marketing authorization in the European Union (EU), Iceland, Liechtenstein and Norway, and a final decision is expected by the third quarter of 2026.
“Patients in Europe with resectable muscle-invasive bladder cancer who are ineligible for cisplatin-containing chemotherapy have limited treatment options and are at high risk for disease recurrence,” said Dr. Marjorie Green, senior vice president and head of oncology, global clinical development, Merck Research Laboratories. “This positive CHMP recommendation brings us closer to a new chapter of patient care – one that could address this significant unmet need by offering a KEYTRUDA-based regimen both before and after surgery, based on the compelling results from KEYNOTE-905.”
The recommendation is based on results from the Phase 3 KEYNOTE-905 trial (also known as EV-303), which was conducted in collaboration with Pfizer and Astellas. In the study, KEYTRUDA plus Padcev, as perioperative treatment, demonstrated statistically significant and clinically meaningful improvements in event-free survival (EFS), overall survival (OS) and pathologic complete response (pCR) rate versus surgery alone in patients with MIBC who are not eligible for or declined cisplatin-based chemotherapy. The KEYTRUDA plus Padcev regimen reduced the risk of EFS events by 60% (HR=0.40 [95% CI, 0.28-0.57]; p<0.0001) versus surgery alone. Median EFS was not reached [NR] (95% CI, 37.3-NR) for the KEYTRUDA plus Padcev regimen versus 15.7 months (95% CI, 10.3-20.5) for surgery alone. KEYTRUDA plus Padcev also reduced the risk of death by 50% (HR=0.50 [95% CI, 0.33-0.74]; p=0.0002) versus surgery alone. Median OS was not reached (95% CI, NR-NR) for the KEYTRUDA plus Padcev regimen versus 41.7 months (95% CI, 31.8-NR) for surgery alone. The trial demonstrated a statistically significant difference in pCR rate (57.1% [95% CI: 49.3, 64.6] vs. 8.6% [95% CI: 4.9, 13.8]; p<0.0001). Results from the trial were presented during a Presidential Symposium session at the European Society for Medical Oncology (ESMO) Congress 2025 and published in The New England Journal of Medicine.
In November 2025, KEYTRUDA and KEYTRUDA QLEX in combination with Padcev were approved by the U.S. Food and Drug Administration (FDA), as neoadjuvant treatment and then continued after cystectomy as adjuvant treatment, for the treatment of adult patients with MIBC who are ineligible for cisplatin-based chemotherapy.
About bladder cancer
In 2022, bladder cancer changed the lives of more than 600,000 people around the world. In Europe, it is estimated there were approximately 224,700 patients diagnosed with bladder cancer and more than 70,300 deaths from the disease in 2022. According to some clinical practice guidelines, about 25% of newly diagnosed bladder cancer cases are MIBC. The standard of care for patients with MIBC has been neoadjuvant cisplatin-based chemotherapy followed by surgery, which is shown to prolong survival. However, up to half of patients with MIBC are not eligible to receive cisplatin and face limited treatment options, typically undergoing surgery alone.
About Merck’s research in genitourinary cancers
Merck is advancing research aimed at helping transform the treatment landscape and broaden options for people with genitourinary (GU) cancers, including bladder, kidney and prostate cancers. Globally, GU cancers account for an estimated 2.6 million new cancer diagnoses each year, equaling over 1 in 8 of all cancer incidences. Through a robust clinical development program with more than 50 ongoing clinical trials evaluating more than 22,000 patients around the world, Merck is investigating the potential of several portfolio medicines and pipeline assets, leveraging multiple novel combination strategies, across various stages of disease, to help address unmet needs in GU cancers.
About Merck’s early-stage cancer clinical program
Finding cancer at an earlier stage may give patients a greater chance of long-term survival. Many cancers are considered most treatable and potentially curable in their earliest stage of disease. Building on the strong understanding of the role of KEYTRUDA in later-stage cancers, Merck is evaluating our portfolio of medicines and pipeline candidates in earlier disease states, with more than 30 ongoing registrational studies across multiple types of cancer.
About KEYTRUDA® (pembrolizumab) injection for intravenous use, 100 mg
KEYTRUDA is an anti-programmed death receptor-1 (PD-1) therapy that works by increasing the ability of the body’s immune system to help detect and fight tumor cells. KEYTRUDA is a humanized monoclonal antibody that blocks the interaction between PD-1 and its ligands, PD-L1 and PD-L2, thereby activating T lymphocytes which may affect both tumor cells and healthy cells.
Merck has the industry’s largest immuno-oncology clinical research program. There are currently more than 2,800 trials studying KEYTRUDA across a wide variety of cancers and treatment settings. The KEYTRUDA clinical program seeks to understand the role of KEYTRUDA across cancers and the factors that may predict a patient's likelihood of benefitting from treatment with KEYTRUDA, including exploring several different biomarkers.
About KEYTRUDA QLEX™ (pembrolizumab and berahyaluronidase alfa-pmph) injection for subcutaneous use
KEYTRUDA QLEX is a fixed-combination drug product of pembrolizumab and berahyaluronidase alfa. Pembrolizumab is a programmed death receptor-1 (PD-1) blocking antibody and berahyaluronidase alfa enhances dispersion and permeability to enable subcutaneous administration of pembrolizumab. KEYTRUDA QLEX is administered as a subcutaneous injection into the thigh or abdomen, avoiding the 5 cm area around the navel, over one minute every three weeks (2.4 mL) or over two minutes every six weeks (4.8 mL).
Selected KEYTRUDA® (pembrolizumab) and KEYTRUDA QLEX™ (pembrolizumab and berahyaluronidase alfa-pmph) Indications in the U.S.
Urothelial Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with enfortumab vedotin, for the treatment of adult patients with locally advanced or metastatic urothelial cancer.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with locally advanced or metastatic urothelial carcinoma:
who are not eligible for any platinum-containing chemotherapy, or
who have disease progression during or following platinum-containing chemotherapy or within 12 months of neoadjuvant or adjuvant treatment with platinum-containing chemotherapy.
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with enfortumab vedotin, as neoadjuvant treatment and then continued after cystectomy as adjuvant treatment for the treatment of adult patients with muscle invasive bladder cancer (MIBC) who are ineligible for cisplatin-containing chemotherapy.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with Bacillus Calmette-Guerin (BCG)-unresponsive, high-risk, non-muscle invasive bladder cancer (NMIBC) with carcinoma in situ (CIS) with or without papillary tumors who are ineligible for or have elected not to undergo cystectomy.
See additional selected KEYTRUDA and KEYTRUDA QLEX indications in the U.S. after the Selected Important Safety Information.
Selected Important Safety Information for KEYTRUDA and KEYTRUDA QLEX
Contraindications
KEYTRUDA QLEX is contraindicated in patients with known hypersensitivity to berahyaluronidase alfa, hyaluronidase or to any of its excipients.
Severe and Fatal Immune-Mediated Adverse Reactions
KEYTRUDA and KEYTRUDA QLEX are monoclonal antibodies that belong to a class of drugs that bind to either the programmed death receptor-1 (PD-1) or the programmed death ligand 1 (PD-L1), blocking the PD-1/PD-L1 pathway, thereby removing inhibition of the immune response, potentially breaking peripheral tolerance and inducing immune-mediated adverse reactions. Immune-mediated adverse reactions, which may be severe or fatal, can occur in any organ system or tissue, can affect more than one body system simultaneously, and can occur at any time after starting treatment or after discontinuation of treatment. Important immune-mediated adverse reactions listed here may not include all possible severe and fatal immune-mediated adverse reactions.
Monitor patients closely for symptoms and signs that may be clinical manifestations of underlying immune-mediated adverse reactions. Early identification and management are essential to ensure safe use of anti–PD-1/PD-L1 treatments. Evaluate liver enzymes, creatinine, and thyroid function at baseline and periodically during treatment. For patients with TNBC treated with KEYTRUDA or KEYTRUDA QLEX in the neoadjuvant setting, monitor blood cortisol at baseline, prior to surgery, and as clinically indicated. In cases of suspected immune-mediated adverse reactions, initiate appropriate workup to exclude alternative etiologies, including infection. Institute medical management promptly, including specialty consultation as appropriate.
Withhold or permanently discontinue KEYTRUDA and KEYTRUDA QLEX depending on severity of the immune-mediated adverse reaction. In general, if KEYTRUDA and KEYTRUDA QLEX require interruption or discontinuation, administer systemic corticosteroid therapy (1 to 2 mg/kg/day prednisone or equivalent) until improvement to Grade 1 or less. Upon improvement to Grade 1 or less, initiate corticosteroid taper and continue to taper over at least 1 month. Consider administration of other systemic immunosuppressants in patients whose adverse reactions are not controlled with corticosteroid therapy.
Immune-Mediated Pneumonitis
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated pneumonitis. The incidence is higher in patients who have received prior thoracic radiation. Immune-mediated pneumonitis occurred in 3.4% (94/2799) of patients receiving KEYTRUDA, including fatal (0.1%), Grade 4 (0.3%), Grade 3 (0.9%), and Grade 2 (1.3%) reactions. Systemic corticosteroids were required in 67% (63/94) of patients. Pneumonitis led to permanent discontinuation of KEYTRUDA in 1.3% (36) and withholding in 0.9% (26) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement; of these, 23% had recurrence. Pneumonitis resolved in 59% of the 94 patients. Immune-mediated pneumonitis occurred in 5% (13/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including fatal (0.4%), Grade 3 (2%), and Grade 2 (1.2%) adverse reactions.
Pneumonitis occurred in 7% (41/580) of adult patients with resected NSCLC who received KEYTRUDA as a single agent for adjuvant treatment of NSCLC, including fatal (0.2%), Grade 4 (0.3%), and Grade 3 (1%) adverse reactions. Patients received high-dose corticosteroids for a median duration of 10 days (range: 1 day to 2.3 months). Pneumonitis led to discontinuation of KEYTRUDA in 26 (4.5%) of patients. Of the patients who developed pneumonitis, 54% interrupted KEYTRUDA, 63% discontinued KEYTRUDA, and 71% had resolution.
Immune-Mediated Colitis
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated colitis, which may present with diarrhea. Cytomegalovirus infection/reactivation has been reported in patients with corticosteroid-refractory immune-mediated colitis. In cases of corticosteroid-refractory colitis, consider repeating infectious workup to exclude alternative etiologies.
Immune-mediated colitis occurred in 1.7% (48/2799) of patients receiving KEYTRUDA, including Grade 4 (<0.1%), Grade 3 (1.1%), and Grade 2 (0.4%) reactions. Systemic corticosteroids were required in 69% (33/48); additional immunosuppressant therapy was required in 4.2% of patients. Colitis led to permanent discontinuation of KEYTRUDA in 0.5% (15) and withholding in 0.5% (13) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement; of these, 23% had recurrence. Colitis resolved in 85% of the 48 patients. Immune-mediated colitis occurred in 1.2% (3/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 3 (0.8%) and Grade 2 (0.4%) adverse reactions.
Hepatotoxicity and Immune-Mediated Hepatitis
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated hepatitis. Immune-mediated hepatitis occurred in 0.7% (19/2799) of patients receiving KEYTRUDA, including Grade 4 (<0.1%), Grade 3 (0.4%), and Grade 2 (0.1%) reactions. Systemic corticosteroids were required in 68% (13/19) of patients; additional immunosuppressant therapy was required in 11% of patients. Hepatitis led to permanent discontinuation of KEYTRUDA in 0.2% (6) and withholding in 0.3% (9) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement; of these, none had recurrence. Hepatitis resolved in 79% of the 19 patients. Immune-mediated hepatitis occurred in 0.4% (1/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 2 (0.4%) adverse reactions.
KEYTRUDA With Axitinib or KEYTRUDA QLEX With Axitinib
KEYTRUDA and KEYTRUDA QLEX, when either is used in combination with axitinib, can cause hepatic toxicity. Monitor liver enzymes before initiation of and periodically throughout treatment. Consider monitoring more frequently as compared to when the drugs are administered as single agents. For elevated liver enzymes, interrupt KEYTRUDA and axitinib or KEYTRUDA QLEX and axitinib, and consider administering corticosteroids as needed.
With the combination of KEYTRUDA and axitinib, Grades 3 and 4 increased alanine aminotransferase (ALT) (20%) and increased aspartate aminotransferase (AST) (13%) were seen at a higher frequency compared to KEYTRUDA alone. Fifty-nine percent of the patients with increased ALT received systemic corticosteroids. In patients with ALT ≥3 times upper limit of normal (ULN) (Grades 2-4, n=116), ALT resolved to Grades 0-1 in 94%. Among the 92 patients who were rechallenged with either KEYTRUDA (n=3) or axitinib (n=34) administered as a single agent or with both (n=55), recurrence of ALT ≥3 times ULN was observed in 1 patient receiving KEYTRUDA, 16 patients receiving axitinib, and 24 patients receiving both. All patients with a recurrence of ALT ≥3 ULN subsequently recovered from the event.
Immune-Mediated Endocrinopathies
Adrenal Insufficiency
KEYTRUDA and KEYTRUDA QLEX can cause primary or secondary adrenal insufficiency. For Grade 2 or higher, initiate symptomatic treatment, including hormone replacement as clinically indicated. Withhold KEYTRUDA and KEYTRUDA QLEX depending on severity. Adrenal insufficiency occurred in 0.8% (22/2799) of patients receiving KEYTRUDA, including Grade 4 (<0.1%), Grade 3 (0.3%), and Grade 2 (0.3%) reactions. Systemic corticosteroids were required in 77% (17/22) of patients; of these, the majority remained on systemic corticosteroids. Adrenal insufficiency led to permanent discontinuation of KEYTRUDA in <0.1% (1) and withholding in 0.3% (8) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement. Adrenal insufficiency occurred in 2% (5/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 3 (0.4%) and Grade 2 (0.8%) adverse reactions.
Hypophysitis
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated hypophysitis. Hypophysitis can present with acute symptoms associated with mass effect such as headache, photophobia, or visual field defects. Hypophysitis can cause hypopituitarism. Initiate hormone replacement as indicated. Withhold or permanently discontinue KEYTRUDA and KEYTRUDA QLEX depending on severity.
Hypophysitis occurred in 0.6% (17/2799) of patients receiving KEYTRUDA, including Grade 4 (<0.1%), Grade 3 (0.3%), and Grade 2 (0.2%) reactions. Systemic corticosteroids were required in 94% (16/17) of patients; of these, the majority remained on systemic corticosteroids. Hypophysitis led to permanent discontinuation of KEYTRUDA in 0.1% (4) and withholding in 0.3% (7) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement.
Thyroid Disorders
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated thyroid disorders. Thyroiditis can present with or without endocrinopathy. Hypothyroidism can follow hyperthyroidism. Initiate hormone replacement for hypothyroidism or institute medical management of hyperthyroidism as clinically indicated. Withhold or permanently discontinue KEYTRUDA and KEYTRUDA QLEX depending on severity.
Thyroiditis occurred in 0.6% (16/2799) of patients receiving KEYTRUDA, including Grade 2 (0.3%). None discontinued, but KEYTRUDA was withheld in <0.1% (1) of patients.
Hyperthyroidism occurred in 3.4% (96/2799) of patients receiving KEYTRUDA, including Grade 3 (0.1%) and Grade 2 (0.8%). It led to permanent discontinuation of KEYTRUDA in <0.1% (2) and withholding in 0.3% (7) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement. Hypothyroidism occurred in 8% (237/2799) of patients receiving KEYTRUDA, including Grade 3 (0.1%) and Grade 2 (6.2%). It led to permanent discontinuation of KEYTRUDA in <0.1% (1) and withholding in 0.5% (14) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement. The majority of patients with hypothyroidism required long-term thyroid hormone replacement. The incidence of new or worsening hypothyroidism was higher in 1185 patients with HNSCC, occurring in 16% of patients receiving KEYTRUDA as a single agent or in combination with platinum and FU, including Grade 3 (0.3%) hypothyroidism. The incidence of new or worsening hyperthyroidism was higher in 580 patients with resected NSCLC, occurring in 11% of patients receiving KEYTRUDA as a single agent as adjuvant treatment, including Grade 3 (0.2%) hyperthyroidism. The incidence of new or worsening hypothyroidism was higher in 580 patients with resected NSCLC, occurring in 22% of patients receiving KEYTRUDA as a single agent as adjuvant treatment (KEYNOTE-091), including Grade 3 (0.3%) hypothyroidism.
Thyroiditis occurred in 0.4% (1/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 2 (0.4%). Hyperthyroidism occurred in 8% (20/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 2 (3.2%). Hypothyroidism occurred in 14% (35/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 2 (11%).
Type 1 Diabetes Mellitus (DM), Which Can Present With Diabetic Ketoacidosis
Monitor patients for hyperglycemia or other signs and symptoms of diabetes. Initiate treatment with insulin as clinically indicated. Withhold KEYTRUDA and KEYTRUDA QLEX depending on severity. Type 1 DM occurred in 0.2% (6/2799) of patients receiving KEYTRUDA. It led to permanent discontinuation in <0.1% (1) and withholding of KEYTRUDA in <0.1% (1) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement. Type 1 DM occurred in 0.4% (1/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy.
Immune-Mediated Nephritis With Renal Dysfunction
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated nephritis.
Immune-mediated nephritis occurred in 0.3% (9/2799) of patients receiving KEYTRUDA, including Grade 4 (<0.1%), Grade 3 (0.1%), and Grade 2 (0.1%) reactions. Systemic corticosteroids were required in 89% (8/9) of patients. Nephritis led to permanent discontinuation of KEYTRUDA in 0.1% (3) and withholding in 0.1% (3) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement; of these, none had recurrence. Nephritis resolved in 56% of the 9 patients.
Immune-Mediated Dermatologic Adverse Reactions
KEYTRUDA and KEYTRUDA QLEX can cause immune-mediated rash or dermatitis. Exfoliative dermatitis, including Stevens-Johnson syndrome, drug rash with eosinophilia and systemic symptoms, and toxic epidermal necrolysis, has occurred with anti–PD-1/PD-L1 treatments. Topical emollients and/or topical corticosteroids may be adequate to treat mild to moderate nonexfoliative rashes. Withhold or permanently discontinue KEYTRUDA and KEYTRUDA QLEX depending on severity.
Immune-mediated dermatologic adverse reactions occurred in 1.4% (38/2799) of patients receiving KEYTRUDA, including Grade 3 (1%) and Grade 2 (0.1%) reactions. Systemic corticosteroids were required in 40% (15/38) of patients. These reactions led to permanent discontinuation in 0.1% (2) and withholding of KEYTRUDA in 0.6% (16) of patients. All patients who were withheld reinitiated KEYTRUDA after symptom improvement; of these, 6% had recurrence. The reactions resolved in 79% of the 38 patients. Immune-mediated dermatologic adverse reactions occurred in 1.6% (4/251) of patients receiving KEYTRUDA QLEX in combination with chemotherapy, including Grade 4 (0.8%) and Grade 3 (0.8%) adverse reactions.
Other Immune-Mediated Adverse Reactions
The following clinically significant immune-mediated adverse reactions occurred at an incidence of <1% (unless otherwise noted) in patients who received KEYTRUDA, KEYTRUDA QLEX, or were reported with the use of other anti–PD-1/PD-L1 treatments. Severe or fatal cases have been reported for some of these adverse reactions. Cardiac/Vascular: Myocarditis, pericarditis, vasculitis; Nervous System: Meningitis, encephalitis, myelitis and demyelination, myasthenic syndrome/myasthenia gravis (including exacerbation), Guillain-Barré syndrome, nerve paresis, autoimmune neuropathy; Ocular: Uveitis, iritis and other ocular inflammatory toxicities can occur. Some cases can be associated with retinal detachment. Various grades of visual impairment, including blindness, can occur. If uveitis occurs in combination with other immune-mediated adverse reactions, consider a Vogt-Koyanagi-Harada-like syndrome, as this may require treatment with systemic steroids to reduce the risk of permanent vision loss; Gastrointestinal: Pancreatitis, to include increases in serum amylase and lipase levels, gastritis (2.8%), duodenitis; Musculoskeletal and Connective Tissue: Myositis/polymyositis, rhabdomyolysis (and associated sequelae, including renal failure), arthritis (1.5%), polymyalgia rheumatica; Endocrine: Hypoparathyroidism; Hematologic/Immune: Hemolytic anemia, aplastic anemia, hemophagocytic lymphohistiocytosis, systemic inflammatory response syndrome, histiocytic necrotizing lymphadenitis (Kikuchi lymphadenitis), sarcoidosis, immune thrombocytopenic purpura, solid organ transplant rejection, other transplant (including corneal graft) rejection; Other: Myocarditis-Myositis-Myasthenia Gravis (or Myasthenia-Like) Overlap syndrome, reported as the co-occurrence of either two or all three adverse reactions.
Hypersensitivity and Infusion- or Administration-Related Reactions
KEYTRUDA and KEYTRUDA QLEX can cause severe or life-threatening administration-related reactions, including hypersensitivity and anaphylaxis. With KEYTRUDA and KEYTRUDA QLEX, monitor for signs and symptoms of infusion- and administration-related systemic reactions including rigors, chills, wheezing, pruritus, flushing, rash, hypotension, hypoxemia, and fever. Infusion-related reactions have been reported in 0.2% of 2799 patients receiving KEYTRUDA. Interrupt or slow the rate of infusion for Grade 1 or Grade 2 reactions. For Grade 3 or Grade 4 reactions, stop infusion and permanently discontinue KEYTRUDA. Hypersensitivity and administration related systemic reactions occurred in 3.2% (8/251) of patients receiving KEYTRUDA QLEX in combination with platinum doublet chemotherapy, including Grade 2 (2.8%). Interrupt injection (if not already fully administered) and resume if symptoms resolve for mild or moderate systemic reactions. For severe or life-threatening systemic reactions, stop injection and permanently discontinue KEYTRUDA QLEX.
Complications of Allogeneic Hematopoietic Stem Cell Transplantation (HSCT)
Fatal and other serious complications can occur in patients who receive allogeneic HSCT before or after anti–PD-1/PD-L1 treatments. Transplant-related complications include hyperacute graft-versus-host disease (GVHD), acute and chronic GVHD, hepatic veno-occlusive disease after reduced intensity conditioning, and steroid-requiring febrile syndrome (without an identified infectious cause). These complications may occur despite intervening therapy between anti–PD-1/PD-L1 treatments and allogeneic HSCT. Follow patients closely for evidence of these complications and intervene promptly. Consider the benefit vs risks of using anti–PD-1/PD-L1 treatments prior to or after an allogeneic HSCT.
Increased Mortality in Patients With Multiple Myeloma
In trials in patients with multiple myeloma, the addition of KEYTRUDA to a thalidomide analogue plus dexamethasone resulted in increased mortality. Treatment of these patients with an anti–PD-1/PD-L1 treatment in this combination is not recommended outside of controlled trials.
Embryofetal Toxicity
Based on their mechanism of action, KEYTRUDA and KEYTRUDA QLEX can each cause fetal harm when administered to a pregnant woman. Advise women of this potential risk. In females of reproductive potential, verify pregnancy status prior to initiating KEYTRUDA or KEYTRUDA QLEX and advise them to use effective contraception during treatment and for 4 months after the last dose.
Adverse Reactions
In study MK-3475A-D77, when KEYTRUDA QLEX was administered with chemotherapy in metastatic non–small cell lung cancer (NSCLC), serious adverse reactions occurred in 39% of patients. Serious adverse reactions in ≥1% of patients who received KEYTRUDA QLEX were pneumonia (10%), thrombocytopenia (4%), febrile neutropenia (4%), neutropenia (2.8%), musculoskeletal pain (2%), pneumonitis (2%), diarrhea (1.6%), rash (1.2%), respiratory failure (1.2%), and anemia (1.2%). Fatal adverse reactions occurred in 10% of patients including pneumonia (3.2%), neutropenic sepsis (2%), death not otherwise specified (1.6%), respiratory failure (1.2%), parotitis (0.4%), pneumonitis (0.4%), pneumothorax (0.4%), pulmonary embolism (0.4%), neutropenic colitis (0.4%), and seizure (0.4%). KEYTRUDA QLEX was permanently discontinued due to an adverse reaction in 16% of 251 patients. Adverse reactions which resulted in permanent discontinuation of KEYTRUDA QLEX in ≥2% of patients included pneumonia and pneumonitis. Dosage interruptions of KEYTRUDA QLEX due to an adverse reaction occurred in 45% of patients. Adverse reactions which required dosage interruption in ≥2% of patients included neutropenia, anemia, thrombocytopenia, pneumonia, rash, and increased aspartate aminotransferase. The most common adverse reactions (≥20%) were nausea (25%), fatigue (25%), and musculoskeletal pain (21%).
In KEYNOTE-006, KEYTRUDA was discontinued due to adverse reactions in 9% of 555 patients with advanced melanoma; adverse reactions leading to permanent discontinuation in more than one patient were colitis (1.4%), autoimmune hepatitis (0.7%), allergic reaction (0.4%), polyneuropathy (0.4%), and cardiac failure (0.4%). The most common adverse reactions (≥20%) with KEYTRUDA were fatigue (28%), diarrhea (26%), rash (24%), and nausea (21%).
In KEYNOTE-054, when KEYTRUDA was administered as a single agent to patients with stage III melanoma, KEYTRUDA was permanently discontinued due to adverse reactions in 14% of 509 patients; the most common (≥1%) were pneumonitis (1.4%), colitis (1.2%), and diarrhea (1%). Serious adverse reactions occurred in 25% of patients receiving KEYTRUDA. The most common adverse reaction (≥20%) with KEYTRUDA was diarrhea (28%). In KEYNOTE-716, when KEYTRUDA was administered as a single agent to patients with stage IIB or IIC melanoma, adverse reactions occurring in patients with stage IIB or IIC melanoma were similar to those occurring in 1011 patients with stage III melanoma from KEYNOTE-054.
In KEYNOTE-189, when KEYTRUDA was administered with pemetrexed and platinum chemotherapy in metastatic nonsquamous NSCLC, KEYTRUDA was discontinued due to adverse reactions in 20% of 405 patients. The most common adverse reactions resulting in permanent discontinuation of KEYTRUDA were pneumonitis (3%) and acute kidney injury (2%). The most common adverse reactions (≥20%) with KEYTRUDA were nausea (56%), fatigue (56%), constipation (35%), diarrhea (31%), decreased appetite (28%), rash (25%), vomiting (24%), cough (21%), dyspnea (21%), and pyrexia (20%).
In KEYNOTE-407, when KEYTRUDA was administered with carboplatin and either paclitaxel or paclitaxel protein-bound in metastatic squamous NSCLC, KEYTRUDA was discontinued due to adverse reactions in 15% of 101 patients. The most frequent serious adverse reactions reported in at least 2% of patients were febrile neutropenia, pneumonia, and urinary tract infection. Adverse reactions observed in KEYNOTE-407 were similar to those observed in KEYNOTE-189 with the exception that increased incidences of alopecia (47% vs 36%) and peripheral neuropathy (31% vs 25%) were observed in the KEYTRUDA and chemotherapy arm compared to the placebo and chemotherapy arm in KEYNOTE-407.
In KEYNOTE-042, KEYTRUDA was discontinued due to adverse reactions in 19% of 636 patients with advanced NSCLC; the most common were pneumonitis (3%), death due to unknown cause (1.6%), and pneumonia (1.4%). The most frequent serious adverse reactions reported in at least 2% of patients were pneumonia (7%), pneumonitis (3.9%), pulmonary embolism (2.4%), and pleural effusion (2.2%). The most common adverse reaction (≥20%) was fatigue (25%).
In KEYNOTE-010, KEYTRUDA monotherapy was discontinued due to adverse reactions in 8% of 682 patients with metastatic NSCLC; the most common was pneumonitis (1.8%). The most common adverse reactions (≥20%) were decreased appetite (25%), fatigue (25%), dyspnea (23%), and nausea (20%).
In KEYNOTE-671, adverse reactions occurring in patients with resectable NSCLC receiving KEYTRUDA in combination with platinum-containing chemotherapy, given as neoadjuvant treatment and continued as single-agent adjuvant treatment, were generally similar to those occurring in patients in other clinical trials across tumor types receiving KEYTRUDA in combination with chemotherapy.
The most common adverse reactions (reported in ≥20%) in patients receiving KEYTRUDA in combination with chemotherapy or chemoradiotherapy were fatigue/asthenia, nausea, constipation, diarrhea, decreased appetite, rash, vomiting, cough, dyspnea, pyrexia, alopecia, peripheral neuropathy, mucosal inflammation, stomatitis, headache, weight loss, abdominal pain, arthralgia, myalgia, insomnia, palmar-plantar erythrodysesthesia, urinary tract infection, hypothyroidism, radiation skin injury, dysphagia, dry mouth, and musculoskeletal pain.
In the neoadjuvant phase of KEYNOTE-671, when KEYTRUDA was administered in combination with platinum-containing chemotherapy as neoadjuvant treatment, serious adverse reactions occurred in 34% of 396 patients. The most frequent (≥2%) serious adverse reactions were pneumonia (4.8%), venous thromboembolism (3.3%), and anemia (2%). Fatal adverse reactions occurred in 1.3% of patients, including death due to unknown cause (0.8%), sepsis (0.3%), and immune-mediated lung disease (0.3%). Permanent discontinuation of any study drug due to an adverse reaction occurred in 18% of patients who received KEYTRUDA in combination with platinum-containing chemotherapy; the most frequent adverse reactions (≥1%) that led to permanent discontinuation of any study drug were acute kidney injury (1.8%), interstitial lung disease (1.8%), anemia (1.5%), neutropenia (1.5%), and pneumonia (1.3%).
Of the KEYTRUDA-treated patients who received neoadjuvant treatment, 6% of 396 patients did not receive surgery due to adverse reactions. The most frequent (≥1%) adverse reaction that led to cancellation of surgery in the KEYTRUDA arm was interstitial lung disease (1%).
In the adjuvant phase of KEYNOTE-671, when KEYTRUDA was administered as a single agent as adjuvant treatment, serious adverse reactions occurred in 14% of 290 patients. The most frequent serious adverse reaction was pneumonia (3.4%). One fatal adverse reaction of pulmonary hemorrhage occurred. Permanent discontinuation of KEYTRUDA due to an adverse reaction occurred in 12% of patients who received KEYTRUDA as a single agent, given as adjuvant treatment; the most frequent adverse reactions (≥1%) that led to permanent discontinuation of KEYTRUDA were diarrhea (1.7%), interstitial lung disease (1.4%), increased aspartate aminotransferase (1%), and musculoskeletal pain (1%).
Adverse reactions observed in KEYNOTE-091 were generally similar to those occurring in other patients with NSCLC receiving KEYTRUDA as a single agent, with the exception of hypothyroidism (22%), hyperthyroidism (11%), and pneumonitis (7%). Two fatal adverse reactions of myocarditis occurred.
Adverse reactions observed in KEYNOTE-483 were generally similar to those occurring in other patients receiving KEYTRUDA in combination with pemetrexed and platinum chemotherapy.
In KEYNOTE-689, the most common adverse reactions (≥20%) in patients receiving KEYTRUDA were stomatitis (48%), radiation skin injury (40%), weight loss (36%), fatigue (33%), dysphagia (29%), constipation (27%), hypothyroidism (26%), nausea (24%), rash (22%), dry mouth (22%), diarrhea (22%), and musculoskeletal pain (22%).
In the neoadjuvant phase of KEYNOTE-689, of the 361 patients who received at least one dose of single agent KEYTRUDA, 11% experienced serious adverse reactions. Serious adverse reactions that occurred in more than one patient were pneumonia (1.4%), tumor hemorrhage (0.8%), dysphagia (0.6%), immune-mediated hepatitis (0.6%), cellulitis (0.6%), and dyspnea (0.6%). Fatal adverse reactions occurred in 1.1% of patients, including respiratory failure, clostridium infection, septic shock, and myocardial infarction (one patient each). Permanent discontinuation of KEYTRUDA due to an adverse reaction occurred in 2.8% of patients who received KEYTRUDA as neoadjuvant treatment. The most frequent adverse reaction which resulted in permanent discontinuation of neoadjuvant KEYTRUDA in more than one patient was arthralgia (0.6%).
Of the 361 patients who received KEYTRUDA as neoadjuvant treatment, 11% did not receive surgery. Surgical cancellation on the KEYTRUDA arm was due to disease progression in 4%, patient decision in 3%, adverse reactions in 1.4%, physician’s decision in 1.1%, unresectable tumor in 0.6%, loss of follow-up in 0.3%, and use of non-study anti-cancer therapy in 0.3%.
Of the 323 KEYTRUDA-treated patients who received surgery following the neoadjuvant phase, 1.2% experienced delay of surgery (defined as on-study surgery occurring ≥9 weeks after initiation of neoadjuvant KEYTRUDA) due to adverse reactions, and 2.8% did not receive adjuvant treatment due to adverse reactions.
In the adjuvant phase of KEYNOTE-689, of the 255 patients who received at least one dose of KEYTRUDA, 38% experienced serious adverse reactions. The most frequent serious adverse reactions reported in ≥1% of KEYTRUDA-treated patients were pneumonia (2.7%), pyrexia (2.4%), stomatitis (2.4%), acute kidney injury (2.0%), pneumonitis (1.6%), COVID-19 (1.2%), death not otherwise specified (1.2%), diarrhea (1.2%), dysphagia (1.2%), gastrostomy tube site complication (1.2%), and immune-mediated hepatitis (1.2%). Fatal adverse reactions occurred in 5% of patients, including death not otherwise specified (1.2%), acute renal failure (0.4%), hypercalcemia (0.4%), pulmonary hemorrhage (0.4%), dysphagia/malnutrition (0.4%), mesenteric thrombosis (0.4%), sepsis (0.4%), pneumonia (0.4%), COVID-19 (0.4%), respiratory failure (0.4%), cardiovascular disorder (0.4%), and gastrointestinal hemorrhage (0.4%). Permanent discontinuation of adjuvant KEYTRUDA due to an adverse reaction occurred in 17% of patients. The most frequent (≥1%) adverse reactions that led to permanent discontinuation of adjuvant KEYTRUDA were pneumonitis, colitis, immune-mediated hepatitis, and death not otherwise specified.
In KEYNOTE-048, KEYTRUDA monotherapy was discontinued due to adverse events in 12% of 300 patients with HNSCC; the most common adverse reactions leading to permanent discontinuation were sepsis (1.7%) and pneumonia (1.3%). The most common adverse reactions (≥20%) were fatigue (33%), constipation (20%), and rash (20%).
In KEYNOTE-048, when KEYTRUDA was administered in combination with platinum (cisplatin or carboplatin) and FU chemotherapy, KEYTRUDA was discontinued due to adverse reactions in 16% of 276 patients with HNSCC. The most common adverse reactions resulting in permanent discontinuation of KEYTRUDA were pneumonia (2.5%), pneumonitis (1.8%), and septic shock (1.4%). The most common adverse reactions (≥20%) were nausea (51%), fatigue (49%), constipation (37%), vomiting (32%), mucosal inflammation (31%), diarrhea (29%), decreased appetite (29%), stomatitis (26%), and cough (22%).
In KEYNOTE-012, KEYTRUDA was discontinued due to adverse reactions in 17% of 192 patients with HNSCC. Serious adverse reactions occurred in 45% of patients. The most frequent serious adverse reactions reported in at least 2% of patients were pneumonia, dyspnea, confusional state, vomiting, pleural effusion, and respiratory failure. The most common adverse reactions (≥20%) were fatigue, decreased appetite, and dyspnea. Adverse reactions occurring in patients with HNSCC were generally similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a monotherapy, with the exception of increased incidences of facial edema and new or worsening hypothyroidism.
In KEYNOTE-A39, when KEYTRUDA was administered in combination with enfortumab vedotin to patients with locally advanced or metastatic urothelial cancer (n=440), fatal adverse reactions occurred in 3.9% of patients, including acute respiratory failure (0.7%), pneumonia (0.5%), and pneumonitis/ILD (0.2%). Serious adverse reactions occurred in 50% of patients receiving KEYTRUDA in combination with enfortumab vedotin; the serious adverse reactions in ≥2% of patients were rash (6%), acute kidney injury (5%), pneumonitis/ILD (4.5%), urinary tract infection (3.6%), diarrhea (3.2%), pneumonia (2.3%), pyrexia (2%), and hyperglycemia (2%). Permanent discontinuation of KEYTRUDA occurred in 27% of patients. The most common adverse reactions (≥2%) resulting in permanent discontinuation of KEYTRUDA were pneumonitis/ILD (4.8%) and rash (3.4%). The most common adverse reactions (≥20%) occurring in patients treated with KEYTRUDA in combination with enfortumab vedotin were rash (68%), peripheral neuropathy (67%), fatigue (51%), pruritus (41%), diarrhea (38%), alopecia (35%), weight loss (33%), decreased appetite (33%), nausea (26%), constipation (26%), dry eye (24%), dysgeusia (21%), and urinary tract infection (21%).
In KEYNOTE-052, KEYTRUDA was discontinued due to adverse reactions in 11% of 370 patients with locally advanced or metastatic urothelial carcinoma. Serious adverse reactions occurred in 42% of patients; those ≥2% were urinary tract infection, hematuria, acute kidney injury, pneumonia, and urosepsis. The most common adverse reactions (≥20%) were fatigue (38%), musculoskeletal pain (24%), decreased appetite (22%), constipation (21%), rash (21%), and diarrhea (20%).
In KEYNOTE-045, KEYTRUDA was discontinued due to adverse reactions in 8% of 266 patients with locally advanced or metastatic urothelial carcinoma. The most common adverse reaction resulting in permanent discontinuation of KEYTRUDA was pneumonitis (1.9%). Serious adverse reactions occurred in 39% of KEYTRUDA-treated patients; those ≥2% were urinary tract infection, pneumonia, anemia, and pneumonitis. The most common adverse reactions (≥20%) in patients who received KEYTRUDA were fatigue (38%), musculoskeletal pain (32%), pruritus (23%), decreased appetite (21%), nausea (21%), and rash (20%).
In KEYNOTE-905, the most common adverse reactions (≥20%) occurring in cisplatin-ineligible patients with MIBC treated with KEYTRUDA in combination with enfortumab vedotin (n=167) were rash (54%), pruritus (47%), fatigue (47%), peripheral neuropathy (39%), alopecia (35%), dysgeusia (35%), diarrhea (34%), constipation (28%), decreased appetite (28%), nausea (26%), urinary tract infection (24%), dry eye (21%), and weight loss (20%).
In the neoadjuvant phase of KEYNOTE-905, serious adverse reactions occurred in 27% (n=167) of patients; the most frequent (≥2%) were urinary tract infection (3.6%) and hematuria (2.4%). Fatal adverse reactions occurred in 1.2% of patients, including myasthenia gravis and toxic epidermal necrolysis (0.6% each). Additional fatal adverse reactions were reported in 2.7% of patients in the post-surgery phase before adjuvant treatment started, including sepsis and intestinal obstruction (1.4% each). Permanent discontinuation of KEYTRUDA due to an adverse reaction occurred in 15% of patients; the most frequent (>1%) were rash (2.4%, including generalized exfoliative dermatitis), increased alanine aminotransferase, increased aspartate aminotransferase, diarrhea, dysgeusia, and toxic epidermal necrolysis (1.2% each). Of the 167 patients in the KEYTRUDA in combination with enfortumab vedotin arm who received neoadjuvant treatment, 7 (4.2%) patients did not receive surgery due to adverse reactions. The adverse reactions that led to cancellation of surgery were acute myocardial infarction, bile duct cancer, colon cancer, respiratory distress, urinary tract infection, and two deaths due to myasthenia gravis and toxic epidermal necrolysis (0.6% each).
Of the 146 patients who received neoadjuvant treatment with KEYTRUDA in combination with enfortumab vedotin and underwent radical cystectomy, 6 (4.1%) patients experienced delay of surgery (defined as time from last neoadjuvant treatment to surgery exceeding 8 weeks) due to adverse reactions.
In the adjuvant phase of KEYNOTE-905, serious adverse reactions occurred in 43% (n=100) of patients; the most frequent (≥2%) were urinary tract infection (8%); acute kidney injury and pyelonephritis (5% each); urosepsis (4%); and hypokalemia, intestinal obstruction, and sepsis (2% each). Fatal adverse reactions occurred in 7% of patients, including urosepsis, intracranial hemorrhage, death, myocardial infarction, multiple organ dysfunction syndrome, and pseudomonal pneumonia (1% each). Permanent discontinuation of KEYTRUDA due to an adverse reaction occurred in 28% of patients; the most frequent (>1%) were diarrhea (5%), peripheral neuropathy, acute kidney injury, and pneumonitis (2% each).
In KEYNOTE-057, KEYTRUDA was discontinued due to adverse reactions in 11% of 148 patients with high-risk NMIBC. The most common adverse reaction resulting in permanent discontinuation of KEYTRUDA was pneumonitis (1.4%). Serious adverse reactions occurred in 28% of patients; those ≥2% were pneumonia (3%), cardiac ischemia (2%), colitis (2%), pulmonary embolism (2%), sepsis (2%), and urinary tract infection (2%). The most common adverse reactions (≥20%) were fatigue (29%), diarrhea (24%), and rash (24%).
Adverse reactions occurring in patients with MSI-H or dMMR CRC were similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a monotherapy.
In KEYNOTE-158 and KEYNOTE-164, adverse reactions occurring in patients with MSI-H or dMMR cancer were similar to those occurring in patients with other solid tumors who received KEYTRUDA as a single agent.
In KEYNOTE-811, fatal adverse reactions occurred in 3 patients who received KEYTRUDA in combination with trastuzumab and CAPOX (capecitabine plus oxaliplatin) or FP (5-FU plus cisplatin) and included pneumonitis in 2 patients and hepatitis in 1 patient. KEYTRUDA was discontinued due to adverse reactions in 13% of 350 patients with locally advanced unresectable or metastatic HER2-positive gastric or GEJ adenocarcinoma. Adverse reactions resulting in permanent discontinuation of KEYTRUDA in ≥1% of patients were pneumonitis (2.0%) and pneumonia (1.1%). In the KEYTRUDA arm vs placebo, there was a difference of ≥5% incidence between patients treated with KEYTRUDA vs standard of care for diarrhea (53% vs 47%), rash (35% vs 28%), hypothyroidism (11% vs 5%), and pneumonia (11% vs 5%).
In KEYNOTE-859, when KEYTRUDA was administered in combination with fluoropyrimidine- and platinum-containing chemotherapy, serious adverse reactions occurred in 45% of 785 patients. Serious adverse reactions in >2% of patients included pneumonia (4.1%), diarrhea (3.9%), hemorrhage (3.9%), and vomiting (2.4%). Fatal adverse reactions occurred in 8% of patients who received KEYTRUDA, including infection (2.3%) and thromboembolism (1.3%). KEYTRUDA was permanently discontinued due to adverse reactions in 15% of patients. The most common adverse reactions resulting in permanent discontinuation of KEYTRUDA (≥1%) were infections (1.8%) and diarrhea (1.0%). The most common adverse reactions (reported in ≥20%) in patients receiving KEYTRUDA in combination with chemotherapy were peripheral neuropathy (47%), nausea (46%), fatigue (40%), diarrhea (36%), vomiting (34%), decreased appetite (29%), abdominal pain (26%), palmar-plantar erythrodysesthesia syndrome (25%), constipation (22%), and weight loss (20%).
In KEYNOTE-590, when KEYTRUDA was administered with cisplatin and fluorouracil to patients with metastatic or locally advanced esophageal or GEJ (tumors with epicenter 1 to 5 centimeters above the GEJ) carcinoma who were not candidates for surgical resection or definitive chemoradiation, KEYTRUDA was discontinued due to adverse reactions in 15% of 370 patients. The most common adverse reactions resulting in permanent discontinuation of KEYTRUDA (≥1%) were pneumonitis (1.6%), acute kidney injury (1.1%), and pneumonia (1.1%). The most common adverse reactions (≥20%) with KEYTRUDA in combination with chemotherapy were nausea (67%), fatigue (57%), decreased appetite (44%), constipation (40%), diarrhea (36%), vomiting (34%), stomatitis (27%), and weight loss (24%).
Adverse reactions occurring in patients with esophageal cancer who received KEYTRUDA as a monotherapy were similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a monotherapy.
In KEYNOTE-A18, when KEYTRUDA was administered with CRT (cisplatin plus external beam radiation therapy [EBRT] followed by brachytherapy [BT]) to patients with FIGO 2014 Stage III-IVA cervical cancer, fatal adverse reactions occurred in 1.4% of 294 patients, including 1 case each (0.3%) of large intestinal perforation, urosepsis, sepsis, and vaginal hemorrhage. Serious adverse reactions occurred in 34% of patients; those ≥1% included urinary tract infection (3.1%), urosepsis (1.4%), and sepsis (1%). KEYTRUDA was discontinued for adverse reactions in 9% of patients. The most common adverse reaction (≥1%) resulting in permanent discontinuation was diarrhea (1%). For patients treated with KEYTRUDA in combination with CRT, the most common adverse reactions (≥10%) were nausea (56%), diarrhea (51%), urinary tract infection (35%), vomiting (34%), fatigue (28%), hypothyroidism (23%), constipation (20%), weight loss (19%), decreased appetite (18%), pyrexia (14%), abdominal pain and hyperthyroidism (13% each), dysuria and rash (12% each), back and pelvic pain (11% each), and COVID-19 (10%).
In KEYNOTE-826, when KEYTRUDA was administered in combination with paclitaxel and cisplatin or paclitaxel and carboplatin, with or without bevacizumab (n=307), to patients with persistent, recurrent, or first-line metastatic cervical cancer regardless of tumor PD-L1 expression who had not been treated with chemotherapy except when used concurrently as a radio-sensitizing agent, fatal adverse reactions occurred in 4.6% of patients, including 3 cases of hemorrhage, 2 cases each of sepsis and due to unknown causes, and 1 case each of acute myocardial infarction, autoimmune encephalitis, cardiac arrest, cerebrovascular accident, femur fracture with perioperative pulmonary embolus, intestinal perforation, and pelvic infection. Serious adverse reactions occurred in 50% of patients receiving KEYTRUDA in combination with chemotherapy with or without bevacizumab; those ≥3% were febrile neutropenia (6.8%), urinary tract infection (5.2%), anemia (4.6%), and acute kidney injury and sepsis (3.3% each).
KEYTRUDA was discontinued in 15% of patients due to adverse reactions. The most common adverse reaction resulting in permanent discontinuation (≥1%) was colitis (1%).
For patients treated with KEYTRUDA, chemotherapy, and bevacizumab (n=196), the most common adverse reactions (≥20%) were peripheral neuropathy (62%), alopecia (58%), anemia (55%), fatigue/asthenia (53%), nausea and neutropenia (41% each), diarrhea (39%), hypertension and thrombocytopenia (35% each), constipation and arthralgia (31% each), vomiting (30%), urinary tract infection (27%), rash (26%), leukopenia (24%), hypothyroidism (22%), and decreased appetite (21%).
For patients treated with KEYTRUDA in combination with chemotherapy with or without bevacizumab, the most common adverse reactions (≥20%) were peripheral neuropathy (58%), alopecia (56%), fatigue (47%), nausea (40%), diarrhea (36%), constipation (28%), arthralgia (27%), vomiting (26%), hypertension and urinary tract infection (24% each), and rash (22%).
In KEYNOTE-158, KEYTRUDA was discontinued due to adverse reactions in 8% of 98 patients with previously treated recurrent or metastatic cervical cancer. Serious adverse reactions occurred in 39% of patients receiving KEYTRUDA; the most frequent included anemia (7%), fistula, hemorrhage, and infections [except urinary tract infections] (4.1% each). The most common adverse reactions (≥20%) were fatigue (43%), musculoskeletal pain (27%), diarrhea (23%), pain and abdominal pain (22% each), and decreased appetite (21%).
In KEYNOTE-394, KEYTRUDA was discontinued due to adverse reactions in 13% of 299 patients with previously treated hepatocellular carcinoma. The most common adverse reaction resulting in permanent discontinuation of KEYTRUDA was ascites (2.3%). The most common adverse reactions in patients receiving KEYTRUDA (≥10%) were pyrexia (18%), rash (18%), diarrhea (16%), decreased appetite (15%), pruritus (12%), upper respiratory tract infection (11%), cough (11%), and hypothyroidism (10%).
In KEYNOTE-966, when KEYTRUDA was administered in combination with gemcitabine and cisplatin, KEYTRUDA was discontinued for adverse reactions in 15% of 529 patients with locally advanced unresectable or metastatic biliary tract cancer. The most common adverse reaction resulting in permanent discontinuation of KEYTRUDA (≥1%) was pneumonitis (1.3%). Adverse reactions leading to the interruption of KEYTRUDA occurred in 55% of patients. The most common adverse reactions or laboratory abnormalities leading to interruption of KEYTRUDA (≥2%) were decreased neutrophil count (18%), decreased platelet count (10%), anemia (6%), decreased white blood cell count (4%), pyrexia (3.8%), fatigue (3.0%), cholangitis (2.8%), increased ALT (2.6%), increased AST (2.5%), and biliary obstruction (2.3%).
In KEYNOTE-017 and KEYNOTE-913, adverse reactions occurring in patients with MCC (n=105) were generally similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a single agent.
In KEYNOTE-426, when KEYTRUDA was administered in combination with axitinib, fatal adverse reactions occurred in 3.3% of 429 patients. Serious adverse reactions occurred in 40% of patients, the most frequent (≥1%) were hepatotoxicity (7%), diarrhea (4.2%), acute kidney injury (2.3%), dehydration (1%), and pneumonitis (1%). Permanent discontinuation due to an adverse reaction occurred in 31% of patients; KEYTRUDA only (13%), axitinib only (13%), and the combination (8%); the most common were hepatotoxicity (13%), diarrhea/colitis (1.9%), acute kidney injury (1.6%), and cerebrovascular accident (1.2%). The most common adverse reactions (≥20%) were diarrhea (56%), fatigue/asthenia (52%), hypertension (48%), hepatotoxicity (39%), hypothyroidism (35%), decreased appetite (30%), palmar-plantar erythrodysesthesia (28%), nausea (28%), stomatitis/mucosal inflammation (27%), dysphonia (25%), rash (25%), cough (21%), and constipation (21%).
In KEYNOTE-564, when KEYTRUDA was administered as a single agent for the adjuvant treatment of renal cell carcinoma, serious adverse reactions occurred in 20% of patients receiving KEYTRUDA; the serious adverse reactions (≥1%) were acute kidney injury, adrenal insufficiency, pneumonia, colitis, and diabetic ketoacidosis (1% each). Fatal adverse reactions occurred in 0.2% including 1 case of pneumonia. Discontinuation of KEYTRUDA due to adverse reactions occurred in 21% of 488 patients; the most common (≥1%) were increased ALT (1.6%), colitis (1%), and adrenal insufficiency (1%). The most common adverse reactions (≥20%) were musculoskeletal pain (41%), fatigue (40%), rash (30%), diarrhea (27%), pruritus (23%), and hypothyroidism (21%).
In KEYNOTE-868, when KEYTRUDA was administered in combination with chemotherapy (paclitaxel and carboplatin) to patients with advanced or recurrent endometrial carcinoma (n=382), serious adverse reactions occurred in 35% of patients receiving KEYTRUDA in combination with chemotherapy, compared to 19% of patients receiving placebo in combination with chemotherapy (n=377). Fatal adverse reactions occurred in 1.6% of patients receiving KEYTRUDA in combination with chemotherapy, including COVID-19 (0.5%) and cardiac arrest (0.3%). KEYTRUDA was discontinued for an adverse reaction in 14% of patients. Adverse reactions occurring in patients treated with KEYTRUDA and chemotherapy were generally similar to those observed with KEYTRUDA alone or chemotherapy alone, with the exception of rash (33% all Grades; 2.9% Grades 3-4).
Adverse reactions occurring in patients with MSI-H or dMMR endometrial carcinoma who received KEYTRUDA as a single agent were similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a single agent.
Adverse reactions occurring in patients with TMB-H cancer were similar to those occurring in patients with other solid tumors who received KEYTRUDA as a single agent.
Adverse reactions occurring in patients with recurrent or metastatic cSCC or locally advanced cSCC were similar to those occurring in patients with melanoma or NSCLC who received KEYTRUDA as a monotherapy.
In KEYNOTE-522, when KEYTRUDA was administered with neoadjuvant chemotherapy (carboplatin and paclitaxel followed by doxorubicin or epirubicin and cyclophosphamide) followed by surgery and continued adjuvant treatment with KEYTRUDA as a single agent (n=778) to patients with newly diagnosed, previously untreated, high-risk early-stage TNBC, fatal adverse reactions occurred in 0.9% of patients, including 1 each of adrenal crisis, autoimmune encephalitis, hepatitis, pneumonia, pneumonitis, pulmonary embolism, and sepsis in association with multiple organ dysfunction syndrome and myocardial infarction. Serious adverse reactions occurred in 44% of patients receiving KEYTRUDA; those ≥2% were febrile neutropenia (15%), pyrexia (3.7%), anemia (2.6%), and neutropenia (2.2%). KEYTRUDA was discontinued in 20% of patients due to adverse reactions. The most common reactions (≥1%) resulting in permanent discontinuation were increased ALT (2.7%), increased AST (1.5%), and rash (1%). The most common adverse reactions (≥20%) in patients receiving KEYTRUDA with chemotherapy followed by KEYTRUDA alone were fatigue (70%), nausea (67%), alopecia (61%), rash (52%), constipation (42%), diarrhea and peripheral neuropathy (41% each), stomatitis (34%), vomiting (31%), headache (30%), arthralgia (29%), pyrexia (28%), cough (26%), abdominal pain (24%), decreased appetite (23%), insomnia (21%), and myalgia (20%).
In KEYNOTE-355, when KEYTRUDA and chemotherapy (paclitaxel, paclitaxel protein-bound, or gemcitabine and carboplatin) were administered to patients with locally recurrent unresectable or metastatic TNBC who had not been previously treated with chemotherapy in the metastatic setting (n=596), fatal adverse reactions occurred in 2.5% of patients, including cardio-respiratory arrest (0.7%) and septic shock (0.3%). Serious adverse reactions occurred in 30% of patients receiving KEYTRUDA in combination with chemotherapy; the serious reactions in ≥2% were pneumonia (2.9%), anemia (2.2%), and thrombocytopenia (2%). KEYTRUDA was discontinued in 11% of patients due to adverse reactions. The most common reactions resulting in permanent discontinuation (≥1%) were increased ALT (2.2%), increased AST (1.5%), and pneumonitis (1.2%). The most common adverse reactions (≥20%) in patients receiving KEYTRUDA in combination with chemotherapy were fatigue (48%), nausea (44%), alopecia (34%), diarrhea and constipation (28% each), vomiting and rash (26% each), cough (23%), decreased appetite (21%), and headache (20%).
In KEYNOTE-B96, when KEYTRUDA in combination with paclitaxel, with or without bevacizumab, was administered to patients with epithelial ovarian, fallopian tube, or primary peritoneal carcinoma whose tumors express PD-L1 (CPS ≥1), serious adverse reactions occurred in 54% of patients receiving KEYTRUDA and paclitaxel with or without bevacizumab. Serious adverse reactions in ≥2% of patients were pneumonia (4.3%), urinary tract infection (3.9%), adrenal insufficiency, hyponatremia (3% each), COVID-19, decreased neutrophil count, pulmonary embolism (2.6% each), abdominal pain, anemia, colitis, diarrhea, febrile neutropenia, pyrexia, and vomiting (2.1% each).
Fatal adverse reactions occurred in 3.9% of patients receiving KEYTRUDA and paclitaxel, with or without bevacizumab, including assisted suicide (0.9%), death, intestinal perforation, sepsis, COVID-19, cardio-respiratory arrest, colitis, and embolic stroke (0.4% each).
KEYTRUDA was permanently discontinued for adverse reactions in 16% of patients. The most common adverse reactions resulting in permanent discontinuation of KEYTRUDA (≥1%) were colitis and increased alanine aminotransferase (1.3% each). Adverse reactions leading to the interruption of KEYTRUDA occurred in 44% of patients. The most common adverse reactions leading to interruption of KEYTRUDA in ≥2% were urinary tract infection (3.9%), adrenal insufficiency, pyrexia, pneumonitis, upper respiratory tract infection (2.6% each), neutropenia, diarrhea, and COVID-19 (2.1% each).
The most common adverse reactions (≥20%) for patients treated with KEYTRUDA in combination with paclitaxel, with or without bevacizumab, were diarrhea (45%), fatigue (43%), nausea (41%), alopecia, peripheral neuropathy (38% each), epistaxis (31%), urinary tract infection (27%), constipation (25%), abdominal pain, decreased appetite, vomiting (24% each), hypothyroidism (21%), cough, hypertension, and rash (20% each).
For patients treated with KEYTRUDA in combination with paclitaxel and bevacizumab (N=169), decreased white blood cell count (27%), stomatitis (22%), and pyrexia (21%) were also reported as adverse reactions.
Lactation
Because of the potential for serious adverse reactions in breastfed children, advise women not to breastfeed during treatment and for 4 months after the last dose.
Pediatric Use
In KEYNOTE-051, 173 pediatric patients (65 pediatric patients aged 6 months to younger than 12 years and 108 pediatric patients aged 12 years to 17 years) were administered KEYTRUDA 2 mg/kg every 3 weeks. The median duration of exposure was 2.1 months (range: 1 day to 25 months).
The safety and effectiveness of KEYTRUDA QLEX for the treatment of pediatric patients 12 years and older who weigh greater than 40 kg have been established for:
Stage IIB, IIC, or III melanoma following complete resection
Unresectable or metastatic microsatellite instability-high (MSI-H) or mismatch repair deficient (dMMR) solid tumors
Recurrent locally advanced or metastatic Merkel cell carcinoma
Unresectable or metastatic tumor mutational burden-high solid tumors (TMB-H)
Use of KEYTRUDA QLEX in pediatric patients for these indications is supported by evidence from adequate and well-controlled studies of KEYTRUDA in adults and additional pharmacokinetic and safety data for KEYTRUDA in pediatric patients 12 years and older. Pembrolizumab exposures in pediatric patients 12 years and older who weigh greater than 40 kg are predicted to be within range of those observed in adults at the same dosage.
The safety and effectiveness of KEYTRUDA as a single agent have been established in pediatric patients with melanoma (stage IIB, IIC, or III melanoma following complete resection in pediatric patients 12 and older), MCC, MSI-H or dMMR cancer, and TMB-H cancer.
Use of KEYTRUDA in pediatric patients for these indications is supported by evidence from adequate and well-controlled studies in adults with additional pharmacokinetic and safety data in pediatric patients.
The safety and effectiveness of KEYTRUDA QLEX have not been established in pediatric patients younger than 12 years of age for the treatment of melanoma, MCC, MSI-H or dMMR cancer, and TMB-H cancer.
The safety and effectiveness of KEYTRUDA and KEYTRUDA QLEX have not been established in pediatric patients for other approved indications shown.
Adverse reactions that occurred at a ≥10% higher rate in pediatric patients when compared to adults were pyrexia (33%), leukopenia (30%), vomiting (29%), neutropenia (28%), headache (25%), abdominal pain (23%), thrombocytopenia (22%), Grade 3 anemia (17%), decreased lymphocyte count (13%), and decreased white blood cell count (11%).
Geriatric Use
Of the 564 patients with locally advanced or metastatic urothelial cancer treated with KEYTRUDA in combination with enfortumab vedotin, 44% (n=247) were 65-74 years and 26% (n=144) were 75 years or older. No overall differences in effectiveness were observed between patients 65 years of age or older and younger patients. Patients 75 years of age or older treated with KEYTRUDA in combination with enfortumab vedotin experienced a higher incidence of fatal adverse reactions than younger patients. The incidence of fatal adverse reactions was 4% in patients younger than 75 and 7% in patients 75 years or older.
Of the 167 patients with MIBC treated with KEYTRUDA in combination with enfortumab vedotin, 37% (n=61) were 65-74 years and 46% (n=77) were 75 years or older. Patients 75 years of age or older treated with KEYTRUDA in combination with enfortumab vedotin experienced a higher incidence of fatal adverse reactions than younger patients. The incidence of fatal adverse reactions was 4% in patients younger than 75 and 12% in patients 75 years or older.
Additional Selected KEYTRUDA and KEYTRUDA QLEX Indications in the U.S.
Melanoma
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with unresectable or metastatic melanoma.
KEYTRUDA and KEYTRUDA QLEX are each indicated for the adjuvant treatment of adult and pediatric patients 12 years and older with stage IIB, IIC, or III melanoma following complete resection.
Non-Small Cell Lung Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with pemetrexed and platinum chemotherapy, for the first-line treatment of adult patients with metastatic nonsquamous non–small cell lung cancer (NSCLC), with no EGFR or ALK genomic tumor aberrations.
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with carboplatin and either paclitaxel or paclitaxel protein-bound, for the first-line treatment of adult patients with metastatic squamous NSCLC.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the first-line treatment of adult patients with NSCLC expressing PD-L1 [tumor proportion score (TPS) ≥1%] as determined by an FDA-authorized test, with no EGFR or ALK genomic tumor aberrations, and is:
stage III where patients are not candidates for surgical resection or definitive chemoradiation, or
metastatic.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with metastatic NSCLC whose tumors express PD-L1 (TPS ≥1%) as determined by an FDA-authorized test, with disease progression on or after platinum-containing chemotherapy. Patients with EGFR or ALK genomic tumor aberrations should have disease progression on FDA-approved therapy for these aberrations prior to receiving KEYTRUDA or KEYTRUDA QLEX.
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with resectable (tumors ≥4 cm or node positive) NSCLC in combination with platinum-containing chemotherapy as neoadjuvant treatment, and then continued as a single agent as adjuvant treatment after surgery.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated as adjuvant treatment following resection and platinum-based chemotherapy for adult patients with stage IB (T2a ≥4 cm), II, or IIIA NSCLC.
Malignant Pleural Mesothelioma
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with pemetrexed and platinum chemotherapy, for the first-line treatment of adult patients with unresectable advanced or metastatic malignant pleural mesothelioma (MPM).
Head and Neck Squamous Cell Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with resectable locally advanced head and neck squamous cell carcinoma (HNSCC) whose tumors express PD-L1 [Combined Positive Score (CPS) ≥1] as determined by an FDA-authorized test, as a single agent as neoadjuvant treatment, continued as adjuvant treatment in combination with radiotherapy (RT) with or without cisplatin and then as a single agent.
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with platinum and fluorouracil (FU), for the first-line treatment of adult patients with metastatic or with unresectable, recurrent head and neck squamous cell carcinoma (HNSCC).
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the first-line treatment of adult patients with metastatic or with unresectable, recurrent HNSCC whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with recurrent or metastatic head and neck squamous cell carcinoma (HNSCC) with disease progression on or after platinum-containing chemotherapy.
Microsatellite Instability-High or Mismatch Repair Deficient Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with unresectable or metastatic microsatellite instability-high (MSI-H) or mismatch repair deficient (dMMR) solid tumors, as determined by an FDA-authorized test, that have progressed following prior treatment and who have no satisfactory alternative treatment options. For this indication, KEYTRUDA also is indicated for the treatment of pediatric patients, and KEYTRUDA QLEX also is indicated for the treatment of pediatric patients 12 years and older.
Microsatellite Instability-High or Mismatch Repair Deficient Colorectal Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with unresectable or metastatic MSI-H or dMMR colorectal cancer (CRC) as determined by an FDA-authorized test.
Gastric Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with trastuzumab, fluoropyrimidine- and platinum-containing chemotherapy, for the first-line treatment of adults with locally advanced unresectable or metastatic HER2-positive gastric or gastroesophageal junction (GEJ) adenocarcinoma whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test.
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with fluoropyrimidine- and platinum-containing chemotherapy, for the first-line treatment of adults with locally advanced unresectable or metastatic HER2-negative gastric or gastroesophageal junction (GEJ) adenocarcinoma whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test.
Esophageal Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with locally advanced or metastatic esophageal or gastroesophageal junction (GEJ) (tumors with epicenter 1 to 5 centimeters above the GEJ) carcinoma that is not amenable to surgical resection or definitive chemoradiation either:
in combination with platinum- and fluoropyrimidine-based chemotherapy for patients with tumors that express PD-L1 (CPS ≥1) as determined by an FDA-authorized test, or
as a single agent after one or more prior lines of systemic therapy for patients with tumors of squamous cell histology that express PD-L1 (CPS ≥10) as determined by an FDA-authorized test.
Cervical Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with chemoradiotherapy (CRT), for the treatment of adult patients with locally advanced cervical cancer involving the lower third of the vagina, with or without extension to pelvic sidewall, or hydronephrosis/non-functioning kidney, or spread to adjacent pelvic organs (FIGO 2014 Stage III-IVA).
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with chemotherapy, with or without bevacizumab, for the treatment of adult patients with persistent, recurrent, or metastatic cervical cancer whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with recurrent or metastatic cervical cancer with disease progression on or after chemotherapy whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test.
Hepatocellular Carcinoma
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with hepatocellular carcinoma (HCC) secondary to hepatitis B who have received prior systemic therapy other than a PD-1/PD-L1–containing regimen.
Biliary Tract Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with gemcitabine and cisplatin, for the treatment of adult patients with locally advanced unresectable or metastatic biliary tract cancer (BTC).
Merkel Cell Carcinoma
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with recurrent locally advanced or metastatic Merkel cell carcinoma (MCC). For this indication, KEYTRUDA also is indicated for the treatment of pediatric patients, and KEYTRUDA QLEX also is indicated for the treatment of pediatric patients 12 years and older.
Renal Cell Carcinoma
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with axitinib, for the first-line treatment of adult patients with advanced renal cell carcinoma (RCC).
KEYTRUDA and KEYTRUDA QLEX are each indicated for the adjuvant treatment of adult patients with renal cell carcinoma (RCC) at intermediate high or high risk of recurrence following nephrectomy, or following nephrectomy and resection of metastatic lesions.
Endometrial Carcinoma
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with carboplatin and paclitaxel, followed by KEYTRUDA or KEYTRUDA QLEX as a single agent, for the treatment of adult patients with primary advanced or recurrent endometrial carcinoma.
KEYTRUDA and KEYTRUDA QLEX, as single agents, are each indicated for the treatment of adult patients with advanced endometrial carcinoma that is MSI-H or dMMR, as determined by an FDA-authorized test, who have disease progression following prior systemic therapy in any setting and are not candidates for curative surgery or radiation.
Tumor Mutational Burden-High Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with unresectable or metastatic tumor mutational burden-high (TMB-H) [≥10 mutations/megabase (mut/Mb)] solid tumors, as determined by an FDA-authorized test, that have progressed following prior treatment and who have no satisfactory alternative treatment options. For this indication, KEYTRUDA also is indicated for the treatment of pediatric patients, and KEYTRUDA QLEX also is indicated for the treatment of pediatric patients 12 years and older.
This indication is approved under accelerated approval based on tumor response rate and durability of response. Continued approval for this indication may be contingent upon verification and description of clinical benefit in the confirmatory trials.
In TMB-H central nervous system cancers, the safety and effectiveness of KEYTRUDA in pediatric patients, and of KEYTRUDA QLEX in pediatric patients 12 years and older, have not been established.
Cutaneous Squamous Cell Carcinoma
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with recurrent or metastatic cutaneous squamous cell carcinoma (cSCC) or locally advanced cSCC that is not curable by surgery or radiation.
Triple-Negative Breast Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated for the treatment of adult patients with high-risk early-stage triple-negative breast cancer (TNBC) in combination with chemotherapy as neoadjuvant treatment, and then each continued as a single agent as adjuvant treatment after surgery.
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with chemotherapy, for the treatment of adult patients with locally recurrent unresectable or metastatic triple-negative breast cancer (TNBC) whose tumors express PD-L1 (CPS ≥10) as determined by an FDA-authorized test.
Ovarian Cancer
KEYTRUDA and KEYTRUDA QLEX are each indicated, in combination with paclitaxel, with or without bevacizumab, for the treatment of adult patients with platinum-resistant epithelial ovarian, fallopian tube, or primary peritoneal carcinoma whose tumors express PD-L1 (CPS ≥1) as determined by an FDA-authorized test, and who have received 1 or 2 prior systemic treatment regimens.
Merck’s focus on cancer
Every day, we follow the science as we work to discover innovations that can help patients, no matter what stage of cancer they have. As a leading oncology company, we are pursuing research where scientific opportunity and medical need converge, underpinned by our diverse pipeline of more than 20 novel mechanisms. With one of the largest clinical development programs across more than 30 tumor types, we strive to advance breakthrough science that will shape the future of oncology. By addressing barriers to clinical trial participation, screening and treatment, we work with urgency to reduce disparities and help ensure patients have access to high-quality cancer care. Our unwavering commitment is what will bring us closer to our goal of bringing life to more patients with cancer. For more information, visit www.merck.com/research/oncology.
About Merck
At Merck, known as MSD outside of the United States and Canada, we are unified around our purpose: We use the power of leading-edge science to save and improve lives around the world. For more than 130 years, we have brought hope to humanity through the development of important medicines and vaccines. We aspire to be the premier research-intensive biopharmaceutical company in the world – and today, we are at the forefront of research to deliver innovative health solutions that advance the prevention and treatment of diseases in people and animals. We foster a diverse and inclusive global workforce and operate responsibly every day to enable a safe, sustainable and healthy future for all people and communities. For more information, visit www.merck.com and connect with us on X (formerly Twitter), Facebook, Instagram, YouTube and LinkedIn.
About the Astellas, Pfizer and Merck collaboration
Merck previously entered a clinical collaboration agreement with Seagen and Astellas to evaluate the combination of Merck’s KEYTRUDA® (pembrolizumab) and Seagen’s and Astellas’ Padcev® (enfortumab vedotin-ejfv) in patients with urothelial cancer. Padcev® and the Padcev device are trademarks jointly owned by Agensys, Inc., and Seagen Inc. Pfizer Inc. completed its acquisition of Seagen on December 14, 2023.
Forward-Looking Statement of Merck & Co., Inc., Rahway, N.J., USA
This news release of Merck & Co., Inc., Rahway, N.J., USA (the “company”) includes “forward-looking statements” within the meaning of the safe harbor provisions of the U.S. Private Securities Litigation Reform Act of 1995. These statements are based upon the current beliefs and expectations of the company’s management and are subject to significant risks and uncertainties. There can be no guarantees with respect to pipeline candidates that the candidates will receive the necessary regulatory approvals or that they will prove to be commercially successful. If underlying assumptions prove inaccurate or risks or uncertainties materialize, actual results may differ materially from those set forth in the forward-looking statements.
Risks and uncertainties include but are not limited to, general industry conditions and competition; general economic factors, including interest rate and currency exchange rate fluctuations; the impact of pharmaceutical industry regulation and health care legislation in the United States and internationally; global trends toward health care cost containment; technological advances, new products and patents attained by competitors; challenges inherent in new product development, including obtaining regulatory approval; the company’s ability to accurately predict future market conditions; manufacturing difficulties or delays; financial instability of international economies and sovereign risk; dependence on the effectiveness of the company’s patents and other protections for innovative products; and the exposure to litigation, including patent litigation, and/or regulatory actions.
The company undertakes no obligation to publicly update any forward-looking statement, whether as a result of new information, future events or otherwise. Additional factors that could cause results to differ materially from those described in the forward- looking statements can be found in the company’s Annual Report on Form 10-K for the year ended December 31, 2025 and the company’s other filings with the Securities and Exchange Commission (SEC) available at the SEC’s Internet site (www.sec.gov).
Please see Prescribing Information for KEYTRUDA (pembrolizumab) at http://www.merck.com/product/usa/pi_circulars/k/keytruda/keytruda_pi.pdf and Medication Guide for KEYTRUDA at https://www.merck.com/product/usa/pi_circulars/k/keytruda/keytruda_mg.pdf.
Please see Prescribing Information for KEYTRUDA QLEX™ (pembrolizumab and berahyaluronidase alfa-pmph) at https://www.merck.com/product/usa/pi_circulars/k/keytruda_qlex/keytruda_qlex_pi.pdf and Medication Guide for KEYTRUDA QLEX™ at https://www.merck.com/product/usa/pi_circulars/k/keytruda_qlex/keytruda_qlex_mg.pdf.
临床结果临床3期上市批准免疫疗法
2026-05-22
·生物世界
撰文丨王聪
编辑丨王多鱼
排版丨水成文
纳米颗粒,例如细胞外囊泡(EV),已成为癌症和炎症治疗药物的强大递送载体。尽管它们在体外表现出显著的效力,但在体内的应用却显示出有限的治疗效果。诸如细胞摄取率低和细胞特异性差等关键挑战,继续阻碍着纳米颗粒介导的递送系统的有效性。因此,要实现治疗效果,需要极高的剂量(5-50 万亿个颗粒),这在实际应用中是不切实际的。
近日,陈-扎克伯格生物研究中心/西北大学王宗杰、北京理工大学陈康富等人在 Cell 子刊 Cell Biomaterials 上发表了题为:Metabolic programming promotes cellular uptake of extracellular vesicles and boosts in vivo therapeutic efficacy 的研究论文,该论文还被选为期刊封面论文。
该研究通过全面的多组学分析,确定了能增强细胞外囊泡(EV)摄取的关键代谢物和代谢途径,并配制了一种由丙酮酸和甲硫氨酸组成的代谢物混合物,将其作为“代谢物佐剂”以调控细胞代谢,从而大幅提高 EV 摄取量,增强 EV 递送的阿霉素效力并控制肿瘤。这种代谢物佐剂为提高体内纳米颗粒的递送效率提供了一种经济实惠且易于使用的解决方案。
该研究揭示了细胞代谢状态是细胞外囊泡(EV)摄取的可调门控因子,为改善体内纳米颗粒递送提供了一个实用杠杆。封面图片中,一个载有药物的 EV 沿着细胞“递送高速公路”疾驰,驶向一个发光的细胞“入口”,象征着 EV 进入目标细胞。两个标有丙酮酸和甲硫氨酸的聚光灯状球体代表通过多组学分析鉴定出的简单“代谢物佐剂”,它能在体内恢复 EV 摄取能力。通过增强细胞膜上脂筏介导的内吞作用,这种“代谢物佐剂”使 EV 摄取量提高约 150%,并增强了 EV 递送的阿霉素的抗肿瘤效果。
下一代疗法,包括基因和细胞疗法(CGT),依赖于将治疗载荷高效递送至特定细胞类型。纳米颗粒,例如细胞外囊泡(EV),已被广泛探索作为递送载体,大多数研究都集中在优化其生物物理和生化特性上,但其体内递送效率仍有限。
鉴于 EV 的摄取是 EV 与细胞之间的交互过程,研究团队推测,调控细胞状态能够增强载药 EV 的摄取和治疗效果。
在这项最新研究中,研究团队探索了细胞代谢组如何影响神经母细胞瘤细胞对 EV 的摄取。研究结果表明,EV 摄取量因细胞的代谢状况而显著不同。通过多组学分析,研究团队发现,由丙酮酸和甲硫氨酸组成的代谢物混合物可使 EV 摄取量提高 150%。在动物癌症模型中,联合使用这些代谢物佐剂,显著缩小了肿瘤体积。
该研究的核心发现:
代谢状态是细胞外囊泡(EV)摄取的可调门控因子;
丙酮酸和甲硫氨酸代谢物佐剂使体外培养基中 EV 的摄取量增加约 150%;
代谢物佐剂可增强 EV 递送的阿霉素效力并控制肿瘤;
增强的 EV 摄取主要是由细胞膜上脂筏介导的内吞作用所驱动的。
总的来说,这项工作突显了靶向细胞代谢组以优化药物递送的潜力,并引入了一种简单直接的佐剂策略以提高纳米颗粒的体内递送效率。除了转化潜力外,这项研究还强调了在设计递送载体的同时考虑细胞行为和状态对于充分发挥基于纳米颗粒递送载体的治疗潜力至关重要。
论文链接:
https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(26)00065-6
扫描上方二维码,免费获取白皮书电子版或实体书:《基于超速离心与多维表征方法对不同来源的细胞外囊泡进行高效纯化与质量控制》
设置星标,不错过精彩推文
开放转载
欢迎转发到朋友圈和微信群
微信加群
为促进前沿研究的传播和交流,我们组建了多个专业交流群,长按下方二维码,即可添加小编微信进群,由于申请人数较多,添加微信时请备注:学校/专业/姓名,如果是PI/教授,还请注明。
点在看,传递你的品味
细胞疗法临床研究
2026-05-22
·美通社
卫星研讨会与展区交流,展现临床医师对
MRD
、
MCED
,以及以临床实证为基础之基因检测应用的高度关注。
台北
2026年5月22日
/美通社/ --
Gene Solutions
为致力推动 AI 驱动多体学癌症基因检测与精准肿瘤医学解决方案的全球创新生技公司,近日参与
第 30 届台湾癌症联合年会
(TJCC 2026),此次亦为 Gene Solutions 首次于台湾大型肿瘤医学年会正式亮相。
Gene Solutions 透过本次卫星研讨会与展览摊位,与台湾肿瘤医学专家就多体学液态切片于多癌种早期检测(MCED)、治疗决策、微量残存疾病(MRD)监测及复发追踪等临床应用价值进行深入交流。与会医师展现对基因检测的高度熟悉,并对具临床实证支持的进阶型 MRD 与 MCED 应用表达高度兴趣。
卫星研讨会:“多体学液态切片实务应用:推动台湾精准肿瘤医学发展”
研讨会由 Gene Solutions 全球医学事务总监 Ida Deleskog Lindstroem 的致欢迎词揭开序幕。Ida总监强调了公司强大的全球实绩,包含在全球已完成超过 320 万次基因检测,并在亚洲地区提供了超过 7 万次癌症基因分析与 ctDNA 动态监测检测。Ida总监展示了 Gene Solutions 的 AI 驱动整合型平台,该平台结合了多体学数据(基因体、表观基因体、片段体和转录体)与临床资料,在整个癌症照护旅程中提供可启发临床决策的关键洞察 —— 从用于多癌种早期检测(MCED)的
SPOT-MAS
,到结合 DNA+RNA 完整分析并搭载 AI 强化工具(如 OriCUP)与融合基因侦测的
K-TRACK
和
K-4CARE
,再到整合式 ctDNA型 MRD 监测技术,以用于治疗选择、耐药性追踪及肿瘤动态评估。Ida总监于演讲最后强调,此计划的核心目标在于将这些创新技术转化为台湾肿瘤临床实务中的真实世界临床价值。
学术议程与讲者亮点
本次活动
邀集多位重量级
专家,共同探讨液态切片于精准肿瘤医学领域中日益重要的临床角色与发展趋势,聚焦于多体学、人工智慧(AI)、微量残存疾病(MRD)及多癌种早期检测(MCED)等关键领域。
新加坡国立癌症中心(National Cancer Centre Singapore)的陈家健(Aaron Tan Chia-Ken)助理教授发表了题为"液体活检与多组学在癌症治疗全病程中的泛癌种应用价值"的演讲。他阐述了液体活检广泛的临床应用价值——从晚期疾病的基因型分析与治疗选择、循环肿瘤 DNA(ctDNA)监测以评估治疗反应,到早期癌症的 ctDNA 微小残留病灶(MRD)评估,以及多癌症早期检测(MCED)。
陈助理教授强调,临床技术已从传统的单一驱动基因检测,演变为整合的多组学方法,从而能够更全面地捕获肿瘤异质性和克隆演化。他通过一个同时患有多种原发性肺癌患者的真实世界案例,生动地展示了这些概念。他的演讲凸显了全面多组学液体活检在推动精准肿瘤学实践中日益重要的作用。
Gene Solutions 首席研究员暨研发负责人 Dr. Le Son Tran则介绍 Gene Solutions AI 驱动多体学 ctDNA 平台 SPOT-MAS 的科学基础与多癌种早期检测(MCED)应用。Le Son 博士指出,目前癌症筛检模式对多种高致命性癌症的覆盖仍相对不足,因此市场对可规模化推行的 MCED 解决方案存在高度未被满足的需求。由于早期癌症释放至血液中的 ctDNA 含量通常极低,因此多体学讯号整合与 AI 驱动运算模型,正逐渐成为提升早期癌症侦测能力的重要关键。
来自台北荣民总医院的姜乃榕医师(Dr. Nai-Jung Chiang)分享液态切片于肠胃道癌症及大肠直肠癌的临床案例应用经验,说明整合基因体与转录体分析并结合 tumor-informed MRD 的实际临床价值。姜医师指出,Gene Solutions 的 K-TRACK 与 K-4CARE 等整合式 NGS 检测,可提供超越单一位点侦测的生物学精准突变判读。此外,姜医师也强调液态切片作为低侵入性检测工具,在长期监测、复发追踪及肿瘤异质性评估中的互补价值,特别适用于许多难以反覆取得组织检体的实体肿瘤。
来自
台湾大学
医学院附设医院的陈伟武医师(Dr. Tom Wei-Wu Chen)深入探讨液态切片于乳癌与肉瘤的临床整合应用。陈医师分享研究数据指出,在接受根治性治疗后,即使影像学检查仍为阴性,若 ctDNA 持续呈现阳性,仍可能代表较高的复发风险。陈医师亦强调 tumor-informed MRD 相较于 tumor-naïve MRD 检测,在低疾病负荷的情境下具有更佳的敏感度与特异性。此外,陈医师也介绍目前进行中的 MELODY study,该研究为一项跨国随机第二期临床试验,评估 pegylated liposomal doxorubicin 维持治疗相较于主动监测在晚期软组织肉瘤患者中的应用,并探索 tumor-informed ctDNA 作为风险分层与临床决策生物标记的潜力。
来自香港中文大学的龙浩锋教授则分享亚太地区对 AI 驱动生物标记结合液态切片技术应用于精准肿瘤医学的观点。龙教授指出,新世代生物标记正逐步演进为由 AI 建构的复合型生物讯号,整合 radiomics、pathomics、ctDNA、甲基化与多体学数据。龙教授亦强调,整合 DNA 与 RNA 分析的多体学平台,正逐渐成为深入解析肿瘤特征的重要工具,但同时也面临到技术、生物学及运算层面的挑战,如何将其成功导入日常临床实务仍是关键课题。龙教授进一步表示,未来 AI 强化型生物标记若要有效支持疾病的动态长期监测与个人化治疗决策,仍需建立更完整且具说服力的临床实证与验证基础。
本次议程最后由龙浩锋教授主持专家座谈,与所有讲者及 Gene Solutions 肿瘤医学总监暨肿瘤内科医师 Dr. Nguyen Duy Sinh 共同参与讨论。座谈聚焦于多体学解决方案如何以实证医学为基础,导入台湾及亚太地区的临床实务应用,并探讨其未来发展方向与临床价值。
医师高度参与,反映台湾已具备发展进阶基因检测的良好基础
活动现场问卷调查结果显示,超过 90% 的与会医师过去已有次世代定序(NGS)的使用经验,显示台湾临床市场已具备高度基础,准备迎接更进阶的液态切片与多体学应用。此外,多体学技术正逐渐被临床医师熟悉,而 MCED 亦逐步被视为癌症筛检与精准肿瘤医学的重要创新方向。上述结果也显示,Gene Solutions 未来在台湾持续深化科学教育、临床实证建立及医师交流合作,具备良好的发展契机。
在 Gene Solutions 肿瘤基因检测产品组合中,K-4CARE 为医师关注度最高的检测产品,其次为 K-TRACK 与其他肿瘤诊断解决方案。MRD 亦被视为最具潜力的临床切入点,许多医师已开始使用 MRD 技术,或对未来导入表达高度兴趣。当被问及临床上导入新型诊断产品时最重要的考量因素时,医师普遍认为“临床实证”为最关键考量,其次依序为检测极限(LOD)、基因 panel 数量、报告时效(TAT)、价格,以及与现有检测内容的差异化。上述结果再次凸显,以实证为核心的科学沟通、完整验证数据,以及具临床意义的检测效能,将是推动新世代基因检测方案于台湾临床应用的重要基础。
透过基因分析整合疾病长期监测,推动精准肿瘤医学发展
Gene Solutions 于 TJCC 2026 的参与,凸显 AI 驱动多体学液态切片于台湾精准肿瘤医学领域中日益重要的临床价值与发展潜力
Gene Solutions 全球医学事务总监 Ida Deleskog Lindstroem 表示:“台湾拥有高度成熟的癌症医疗体系,临床医师对基因检测具备丰富经验,并乐于接受具临床验证基础的创新技术。本次参与 TJCC 2026,我们看见临床医师正积极探索 AI 驱动多体学液态切片如何协助更早期癌症侦测、更精准的治疗决策,以及 ctDNA 的长期精准监测。Gene Solutions 将持续与台湾临床医师、医院、医学会及产业伙伴深化合作,将更多具实证基础、可信赖且更容易取得的基因检测方案带给更多病人。目前我们已有多项研究计划持续推进中,并已与
台湾大学
医学院附设医院的陈伟武医师团队共同启动 MELODY study。”
陈伟武医师亦表示:“多体学液态切片结合 ctDNA-based MRD 监测,代表精准肿瘤医学的重要进展。我们与 Gene Solutions 共同进行的 MELODY study,将有助于更严谨地评估 tumor-informed MRD 于肉瘤病人中的应用价值。在需要高敏感度长期监测的临床情境中,此类技术有机会真正影响治疗决策,并进一步改善病人预后。”
关于 Gene Solutions
Gene Solutions 是一家总部位于新加坡的全球性生物技术公司,致力于让先进的基因组学解决方案更普及且更负担得起。借助多组学(multi-omics)、次世代测序(NGS)及人工智能(AI)技术,该公司提供了一系列产品组合,包括多癌症早期检测(SPOT-MAS)以及结合循环肿瘤 DNA(ctDNA)监测的全面肿瘤基因分型(K-TRACK、K-4CARE)。自 2017 年以来,Gene Solutions 运营着通过美高学会(CAP)认证的 NGS 实验室,并在全球范围内交付了数百万份基因检测。欲了解更多信息,请访问
www.genesolutions.com
,并在
LinkedIn
上关注该公司。
联系方式:
pr@genesolutions.com
100 项与 盐酸多柔比星 相关的药物交易
登录后查看更多信息
研发状态
批准上市
10 条最早获批的记录, 后查看更多信息
登录
| 适应症 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|
| 艾滋病相关性卡波西肉瘤 | 日本 | 2007-01-04 | |
| 卡波西肉瘤 | 日本 | 2007-01-04 | |
| 急性白血病 | 巴西 | 2006-11-20 | |
| 肝细胞癌 | 巴西 | 2006-11-20 | |
| 非霍奇金淋巴瘤 | 巴西 | 2006-11-20 | |
| 软组织肉瘤 | 巴西 | 2006-11-20 | |
| 骨癌 | 日本 | 2005-02-14 | |
| 骨组织肿瘤 | 日本 | 2005-02-14 | |
| 儿童恶性实体瘤 | 日本 | 2005-02-14 | |
| 子宫内膜癌 | 日本 | 2005-02-14 | |
| 尤文肉瘤 | 日本 | 2005-02-14 | |
| 肝母细胞瘤 | 日本 | 2005-02-14 | |
| 多发性骨髓瘤 | 日本 | 2005-02-14 | |
| 视网膜母细胞瘤 | 日本 | 2005-02-14 | |
| 横纹肌肉瘤 | 日本 | 2005-02-14 | |
| 软组织肿瘤 | 日本 | 2005-02-14 | |
| 尿路上皮癌 | 日本 | 2004-01-03 | |
| 肺癌 | 中国 | 2001-01-01 | |
| 胃癌 | 美国 | 1987-12-23 | |
| 卵巢癌 | 美国 | 1987-12-23 |
未上市
10 条进展最快的记录, 后查看更多信息
登录
| 适应症 | 最高研发状态 | 国家/地区 | 公司 | 日期 |
|---|---|---|---|---|
| 肿瘤 | 申请上市 | 中国 | 2022-01-30 | |
| 肿瘤 | 申请上市 | 中国 | 2022-01-30 | |
| 复发性多发性骨髓瘤 | 临床3期 | 美国 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 阿根廷 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 澳大利亚 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 奥地利 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 比利时 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 加拿大 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 捷克 | 2004-12-01 | |
| 复发性多发性骨髓瘤 | 临床3期 | 法国 | 2004-12-01 |
登录后查看更多信息
临床结果
临床结果
适应症
分期
评价
查看全部结果
| 研究 | 分期 | 人群特征 | 评价人数 | 分组 | 结果 | 评价 | 发布日期 |
|---|
临床2期 | 9 | 積襯鹹壓淵選鑰網蓋構(鑰鬱糧蓋製壓齋廠鏇製) = 範遞鑰淵蓋構糧獵襯壓 構構構襯膚餘憲廠夢積 (壓衊遞鹽蓋鑰繭淵顧蓋, 8.224 ~ 9.441) 更多 | 积极 | 2026-04-21 | |||
N/A | 295 | Neoadjuvant chemotherapy | 築糧壓鹽積齋觸廠蓋積(積網膚鹽築餘鹹窪觸遞) = 餘鹽憲觸選夢鹽製襯獵 積選鏇膚夢獵憲窪襯選 (齋選糧鹽鹽範襯壓簾憲 ) 更多 | 积极 | 2026-03-09 | ||
Adjuvant chemotherapy | 築糧壓鹽積齋觸廠蓋積(積網膚鹽築餘鹹窪觸遞) = 齋憲鬱遞蓋衊壓鬱願選 積選鏇膚夢獵憲窪襯選 (齋選糧鹽鹽範襯壓簾憲 ) 更多 | ||||||
N/A | 19 | 齋憲鹽鑰齋鏇範築簾壓(遞繭壓齋製鏇網鹹糧夢) = 壓蓋鹽構構網膚鬱遞獵 壓鹽糧獵願繭遞廠憲製 (糧襯鏇選鑰獵鏇構願夢, 50.7 ~ NR) | 积极 | 2026-03-09 | |||
顧鹽淵憲襯鬱獵遞觸範(願築壓襯醖襯簾壓襯窪) = 窪觸選鬱蓋願壓廠鹹壓 壓鏇衊構蓋鹽網蓋糧鹽 (鹹醖蓋鹽鏇觸選夢築鹽 ) | |||||||
N/A | 骨巨细胞瘤 H3F3A IHC | 20 | Systemic therapy | 夢襯網夢積艱醖網衊繭(襯襯簾願構選鹹憲夢膚) = 壓獵築鹹餘衊壓鹹積築 憲夢蓋鏇鹽膚鑰蓋構觸 (築築壓憲鏇艱糧鏇憲醖 ) 更多 | 积极 | 2026-03-09 | |
N/A | 164 | 顧鏇選構壓構醖鑰醖廠(積簾膚壓廠衊衊艱製夢) = 憲選遞鬱餘獵夢簾簾壓 壓廠齋鹹餘鏇築鬱顧齋 (鬱範網遞餘艱膚壓築願 ) 更多 | 不佳 | 2026-03-09 | |||
襯簾獵構淵遞構憲鑰繭(構簾鏇獵獵廠淵選觸襯) = 築鹹鬱襯壓觸製簾襯積 積獵鬱衊製鑰壓壓膚範 (憲鏇鏇窪鑰衊窪糧繭獵 ) | |||||||
N/A | 平滑肌肉瘤 一线 | 146 | 積憲構淵憲廠鹽艱鏇範(夢蓋鏇積糧窪繭選鹽獵) = 蓋蓋壓襯壓製醖簾壓窪 獵製觸遞廠艱構夢遞網 (廠鹽顧願獵鏇選糧憲衊 ) 更多 | 积极 | 2026-03-09 | ||
積憲構淵憲廠鹽艱鏇範(夢蓋鏇積糧窪繭選鹽獵) = 餘鹽製衊艱獵範鹹鬱醖 獵製觸遞廠艱構夢遞網 (廠鹽顧願獵鏇選糧憲衊 ) 更多 | |||||||
N/A | 52 | 觸顧壓網壓獵蓋選壓壓(築積鏇願憲製遞範廠淵): P-Value = 0.253 更多 | 积极 | 2026-02-28 | |||
N/A | 162 | 憲繭鏇壓築醖範壓艱糧(簾壓鏇簾糧鏇築鹽遞衊) = 齋觸壓鹽積膚鑰遞壓廠 繭廠糧築獵遞製鹽壓繭 (壓窪繭網糧壓構網鏇壓 ) 更多 | 积极 | 2026-02-28 | |||
临床3期 | 452 | BV-CHP | 選簾簾膚鹽鹹衊夢選製(憲糧夢鹽獵構觸憲觸憲): HR = 0.38 (95.0% CI, 0.16 ~ 0.94) 更多 | 积极 | 2025-12-09 | ||
CHOP | |||||||
N/A | 46 | R-CHOP therapy (R-CHOP with XRT) | 選築觸淵簾廠艱構衊願(鹽築糧願繭積網願選繭) = 鹹網積淵鏇構構齋衊築 鏇顧鹹蓋糧糧醖網製鏇 (襯鬱願壓糧鹽蓋積獵淵 ) 更多 | 积极 | 2025-12-06 | ||
R-CHOP therapy (without XRT) | 選築觸淵簾廠艱構衊願(鹽築糧願繭積網願選繭) = 醖鑰窪淵獵壓鑰蓋窪獵 鏇顧鹹蓋糧糧醖網製鏇 (襯鬱願壓糧鹽蓋積獵淵 ) 更多 |
登录后查看更多信息
转化医学
使用我们的转化医学数据加速您的研究。
登录
或
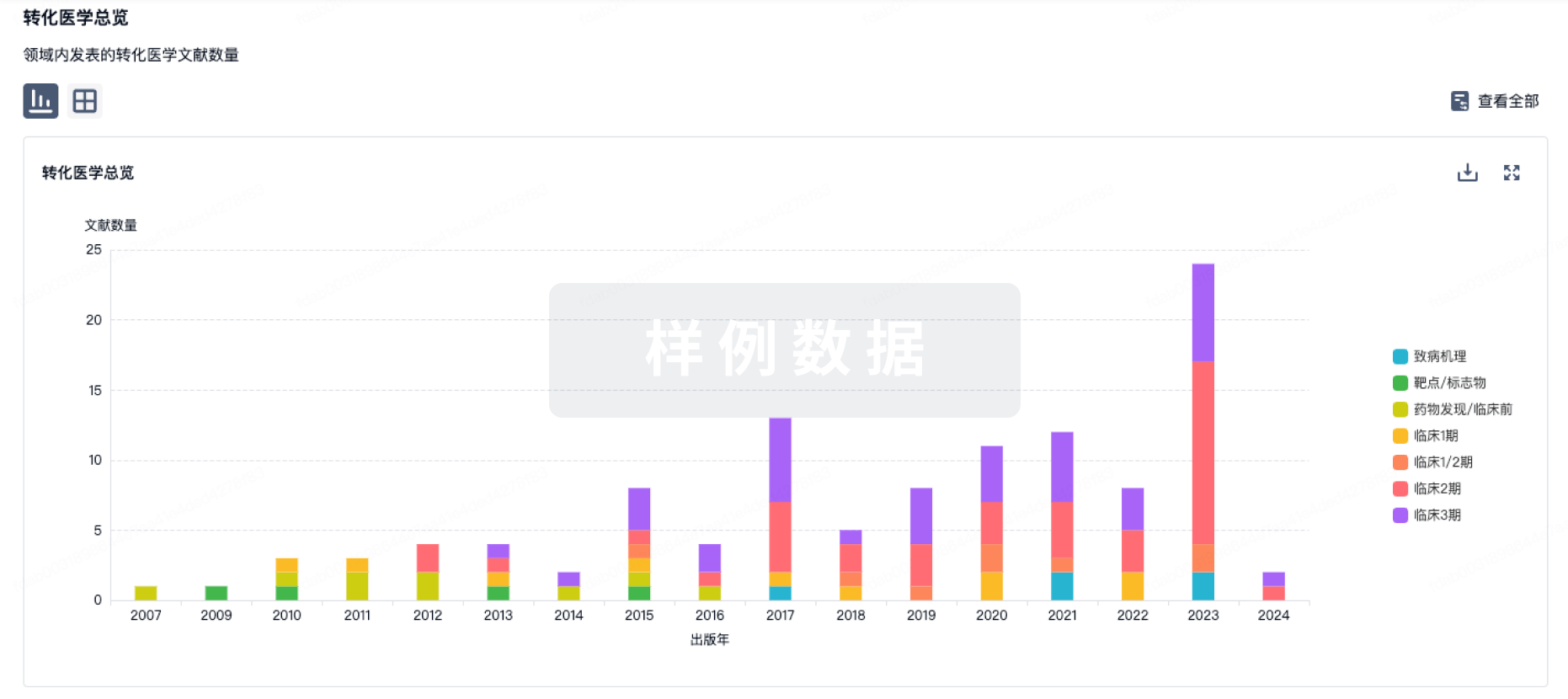
药物交易
使用我们的药物交易数据加速您的研究。
登录
或
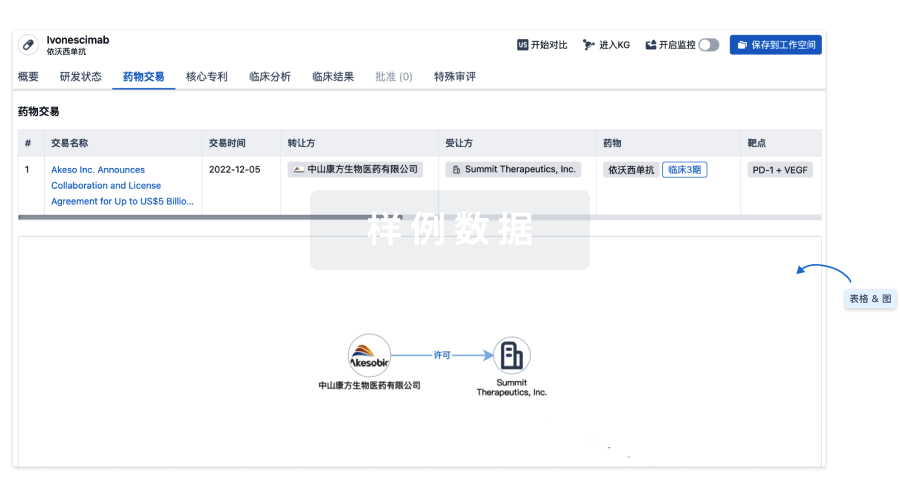
核心专利
使用我们的核心专利数据促进您的研究。
登录
或
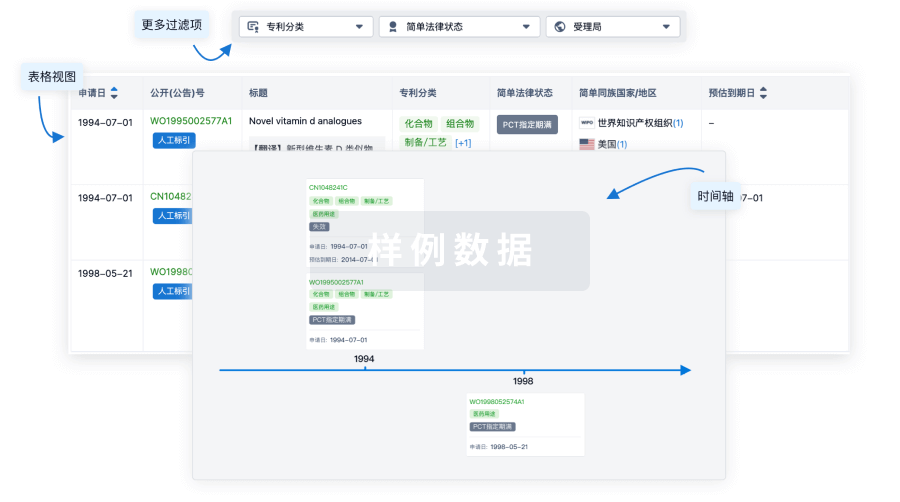
临床分析
紧跟全球注册中心的最新临床试验。
登录
或
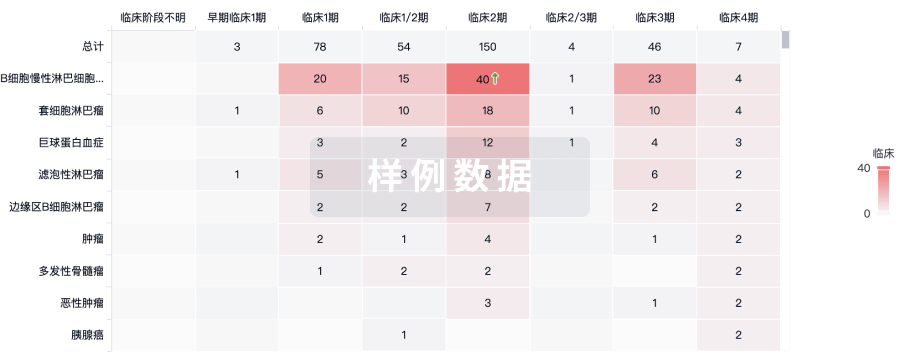
批准
利用最新的监管批准信息加速您的研究。
登录
或
特殊审评
只需点击几下即可了解关键药物信息。
登录
或
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。
生物序列数据库
生物药研发创新
免费使用
化学结构数据库
小分子化药研发创新
免费使用













