预约演示
从CDE承办-知晓药研动向,盘点2020年中国药品审评
2021-01-03
优先审批免疫疗法特殊审批抗体创新药
2020年接近尾声,今年的审评审批申请工作也将告一段落,尽管今年我国深受新冠疫情的影响,但CDE承办的药物审评审批申请(按受理号计,下同)并没有因此而减少。
总体
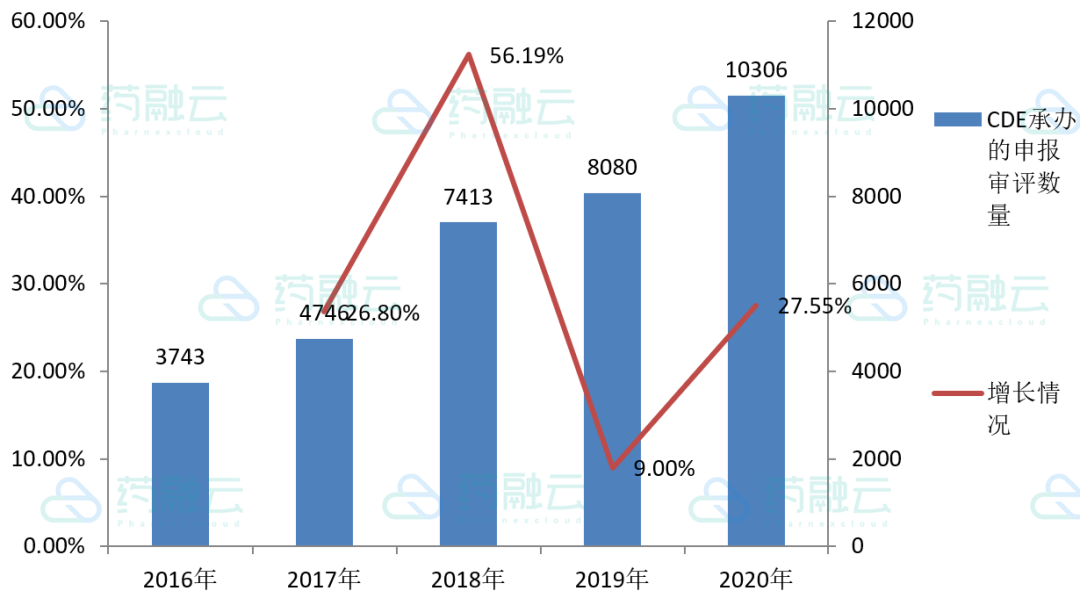
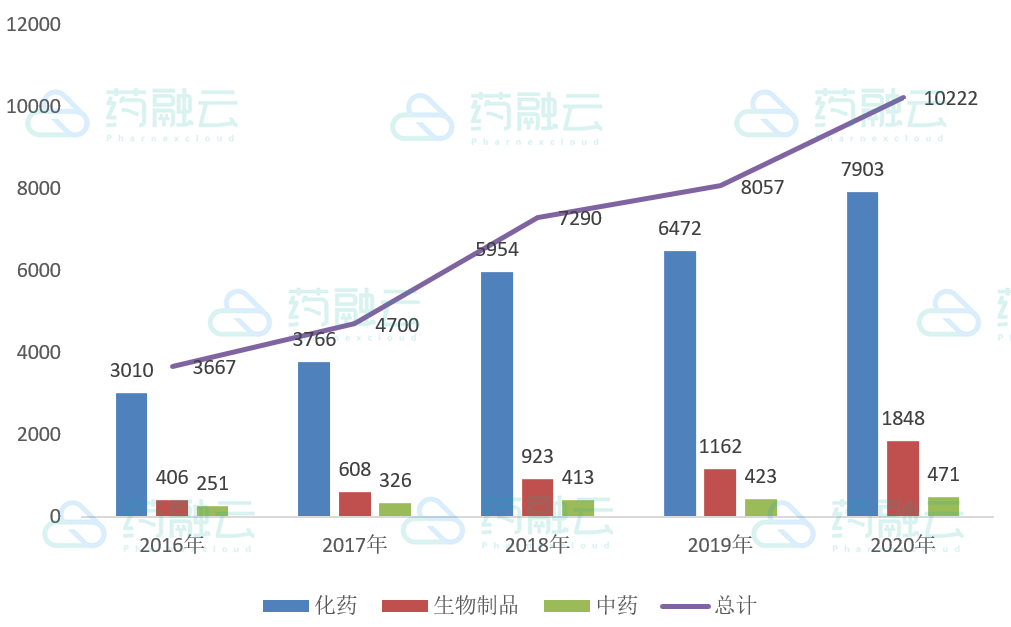
见图1。其中,化药、中药及生物制品共计10222件,化药受理7903件,生物制品1848件,中药受理471件,见图2。
Preview
来源: 药融云
图1:近5年CDE承办的申报审评统计
Preview
来源: 药融云
图2:近五年化药/中药及生物制品承办对比
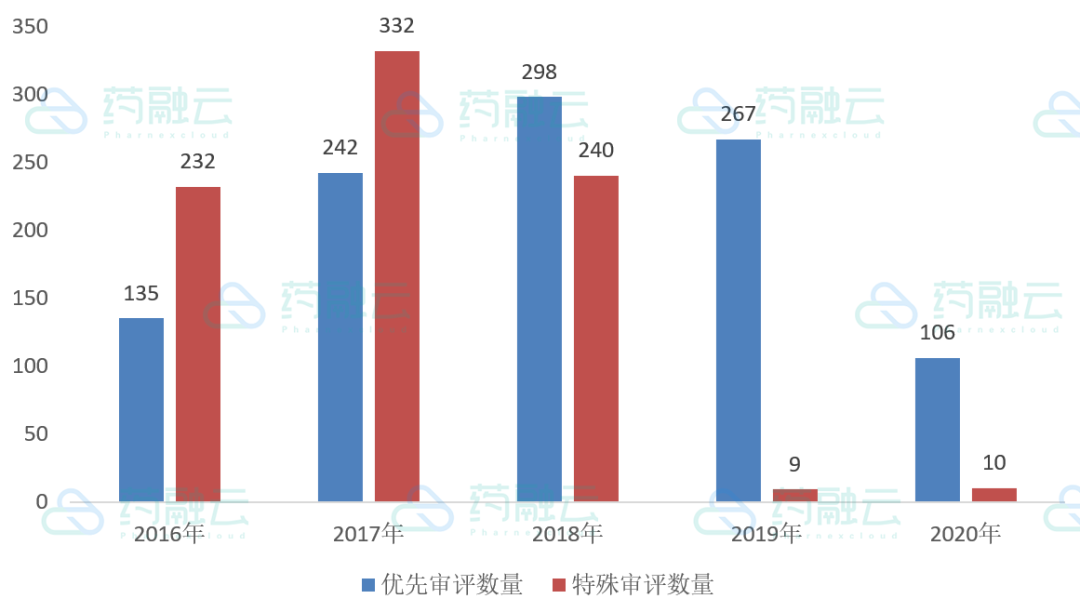
2020年优先审评数量同比呈明显下降趋势,而特殊审评近两年数量出现大幅度下降,维持在年均10个左右,进入特殊审评序列的均为1类新药,见图3。
Preview
来源: 药融云
图3:优先审评及特殊审评统计
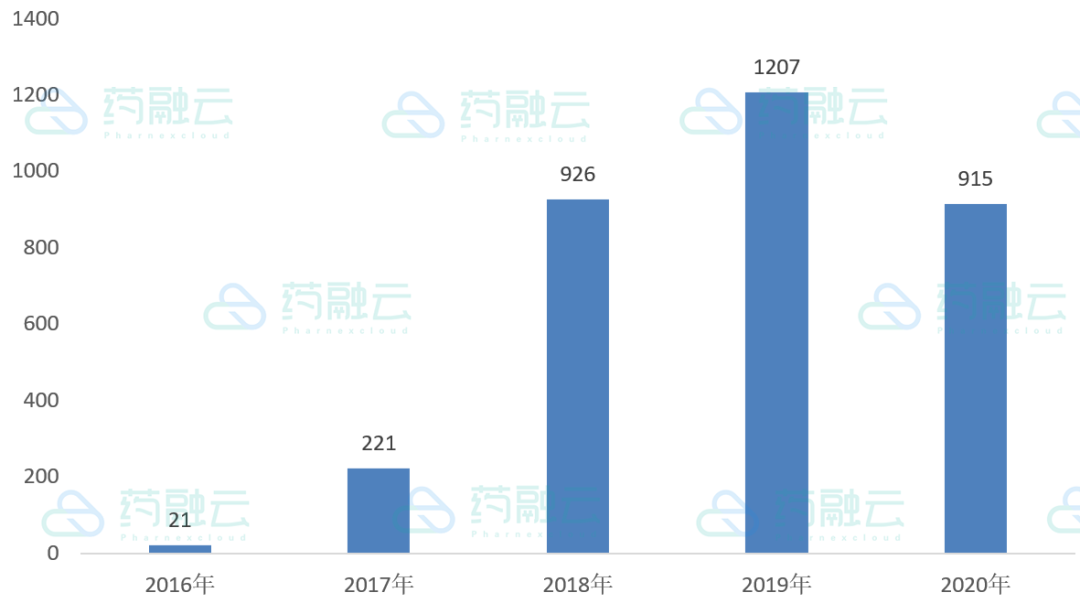
2020年CDE承办的一致性评价申报数量小幅度回落,但仍有915项在审评序列,见图4。通过一致性评价的受理号有20个,视同通过的有3个,见表1。
Preview
来源: 药融云
图4:近5年CDE承办一致性评价统计
表1:2020年通过一致性评价药物信息
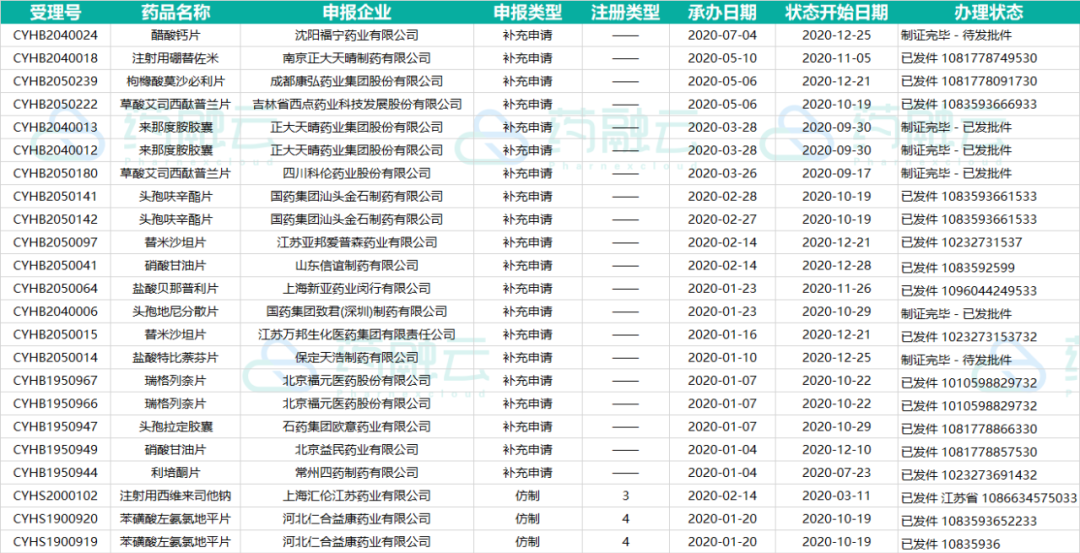
Preview
来源: 药融云
数据来源:药融云中国药品审评数据库
1类新药
2020年CDE共承办1类新药申报1250项,占比总申报数量的12.15%,同比增长74.58%。
1类新药审评序列中,优先审评有26项,特殊审评10项,见图5。
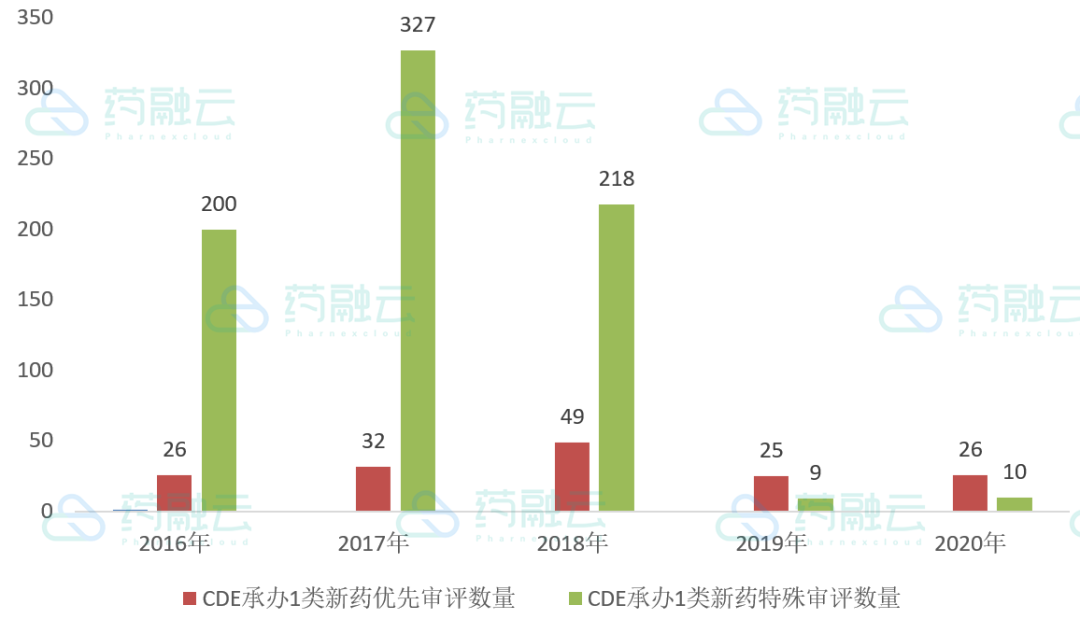
Preview
来源: 药融云
图5:近5年CDE承办的1类新药优先及特殊审评情况
奥布替尼:本品是一种口服BTK抑制剂,与BTK不可逆结合,诱导下游激酶失活和细胞死亡。本次获批的适应症为复发/难治性套细胞淋巴瘤 (MCL),是继用于治疗复发或难治慢性淋巴细胞白血病复发或难治慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)之后的第二个适应症。目前,全球已有3款BTK抑制剂药物获批上市,分别是伊布替尼/强生、阿卡替尼/阿斯利康、泽布替尼/百济神州。
表2:CDE承办的1类新药申报中优先审评的药品情况
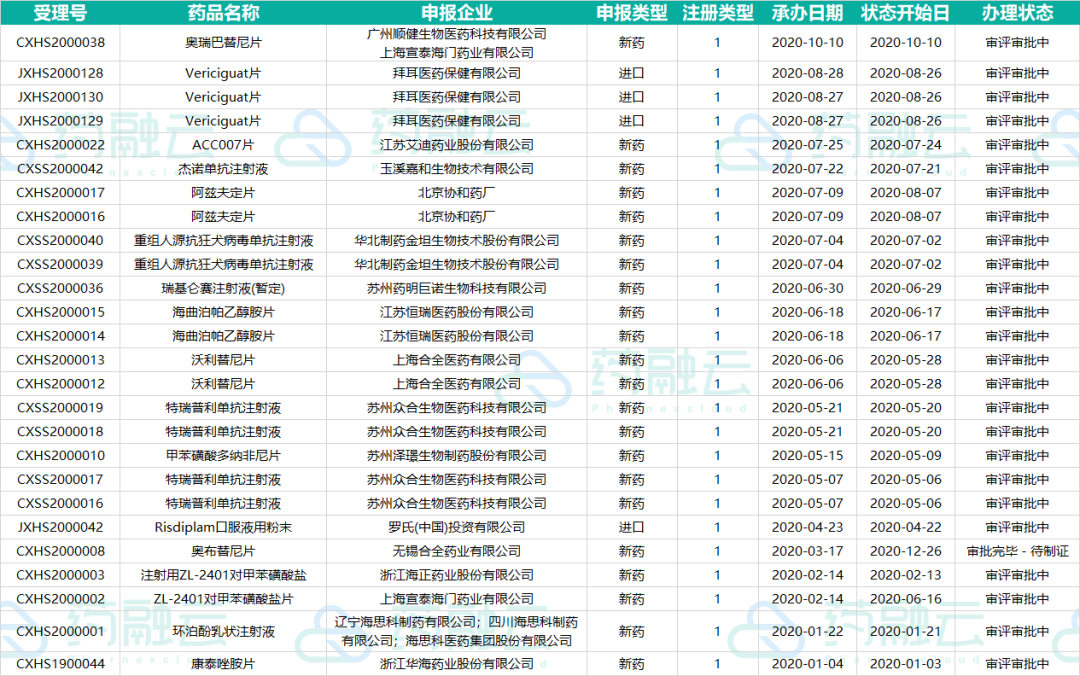
Preview
来源: 药融云
数据来源:药融云数据
截止发稿日,2020年CDE共承办特殊审评申报有10项(按受理号计),申报类型均为1类新药。申报上市药品为:海曲泊帕乙醇胺片、瑞基仑赛注射液(暂定)和替雷利珠单抗注射液。申报临床产品为:注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)、注射用SHR-1806、注射用SHR-A1811品种。目前的办理状态均在审评审批中。
表3:2020年CDE承办的特殊审评信息
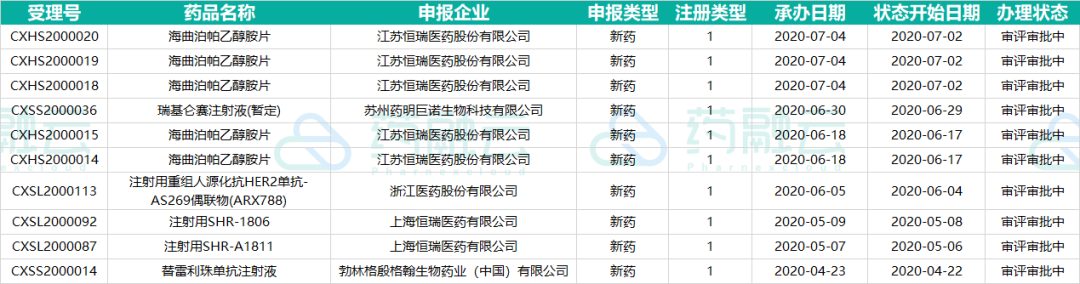
Preview
来源: 药融云
1.海曲泊帕乙醇胺片
2.瑞基仑赛注射液(暂定)
3. 注射用重组人源化抗HER2单抗-AS269偶联药物(ARX788)
:是浙江医药股份开发的治疗HER2阳性局部晚期或转移性乳腺癌HER2阳性局部晚期或转移性乳腺癌的联用组合药物。针对的治疗癌种类为乳腺癌。
4. 注射用SHR-1806
5. 注射用SHR-A1811
6. 替雷利珠单抗注射液:该药物是百济神州全球首款肿瘤免疫治疗药物,也是首款在国内获批上市的自主研发抗癌1类新药,于2019年12月26日获得国家药品监督管理局上市批准,用于至少经过二线系统化疗治疗的复发患者或难治性经典型霍奇金淋巴瘤(R/R cHL)患者。
版权声明:本文转自药融云,如不希望被转载的媒体或个人可与我们联系,我们将立即删除
<END>
【关于药融圈】药融圈围绕我国生物医药产业链,针对生物医药大数据、技术和资本投资、药融园(产业园)等开展系列系统性工作,促进我国生物医药产业健康发展,完善产业链,共同面对全球合作和竞争。

Preview
来源: 药融云

Preview
来源: 药融云
点分享

Preview
来源: 药融云
点点赞点在看
更多内容,请访问原始网站
文中所述内容并不反映新药情报库及其所属公司任何意见及观点,如有版权侵扰或错误之处,请及时联系我们,我们会在24小时内配合处理。
生物医药百科问答
全新生物医药AI Agent 覆盖科研全链路,让突破性发现快人一步
立即开始免费试用!
智慧芽新药情报库是智慧芽专为生命科学人士构建的基于AI的创新药情报平台,助您全方位提升您的研发与决策效率。
立即开始数据试用!
智慧芽新药库数据也通过智慧芽数据服务平台,以API或者数据包形式对外开放,助您更加充分利用智慧芽新药情报信息。





